- 首页 > 正文
醛固酮合酶抑制剂的新纪元:从原发性醛固酮增多症看治疗新曙光
发表时间:2026-03-13 15:22:34
背景:被忽视的醛固酮与现有治疗局限
在肾病学领域,肾素-血管紧张素系统长期受到关注,但其关键的“同源系统”——醛固酮的作用常被忽视。严格来说,应称之为肾素-血管紧张素-醛固酮系统。醛固酮远非单纯的“旁观者”,它在心脏纤维化、血管损伤及肾功能恶化(尤其在蛋白尿性糖尿病肾病中)扮演着重要角色。
目前,盐皮质激素受体拮抗剂(如螺内酯、依普利酮及非奈利酮)已通过临床试验证实其疗效,用于心力衰竭、糖尿病肾病及射血分数保留的心力衰竭。然而,另一种直接阻断醛固酮合成的策略——醛固酮合酶抑制剂——正逐渐进入视野。其研发进程耗时良久,核心原因在于,醛固酮合酶与参与皮质醇合成的11β-羟化酶具有高度同源性,因此,研发醛固酮合酶抑制剂的关键要求,是保证药物对醛固酮合酶的特异性,同时不抑制糖皮质激素的合成。目前多项醛固酮合酶抑制剂的在研注册临床试验中,均纳入了该通路的相关分析
目前有多款醛固酮合酶抑制剂处于研发阶段:
lorundrostat:主要用于未控制的高血压;vicadrostat:针对糖尿病肾病;baxdrostat:同时针对未控制的高血压及糖尿病肾病。
鉴于盐皮质激素受体拮抗剂已在上述疾病中被证实有效,醛固酮合酶抑制剂是否必要?值得注意的是,现有的针对高血压及糖尿病肾病开展的醛固酮合酶抑制剂临床试验,均未将疗效确切且获批适应证的盐皮质激素受体拮抗剂设为活性对照药物。此外,截至目前,我们尚未探讨盐皮质激素受体拮抗剂(或醛固酮合酶抑制剂)的另一项适应证 ——原发性醛固酮增多症。原发性醛固酮增多症:醛固酮合酶抑制剂最具潜力的应用领域
1. 疾病现状:诊疗严重不足
原发性醛固酮增多症是继发性高血压最常见的病因之一(若排除睡眠呼吸暂停、慢性肾脏病等因素导致的继发性高血压排除在外),但其筛查率、诊断率及治疗率极低,针对原发性醛固酮增多症的临床筛查与诊疗工作开展得十分有限。当前,各大高血压诊疗指南均强调了提高原发性醛固酮增多症筛查率的必要性,并简化了筛查流程。
2. 治疗困境与ASI的理论优势
除了筛查层面的问题,仅有少数原发性醛固酮增多症患者为单侧病变,可通过肾上腺切除术治愈或病情缓解。绝大多数患者需长期使用盐皮质激素受体拮抗剂治疗。但在临床实践,许多原发性醛固酮增多症患者所需盐皮质激素受体拮抗剂的剂量极大,例如如螺内酯200mg(或依普利酮 400 mg)或更高剂量,这是因为患者体内醛固酮水平过高,需要大量药物才能实现受体阻断,即便如此,临床仍常无法达到理想的治疗效果。在此背景下,在原发性醛固酮增多症的治疗领域,应用直接抑制醛固酮合成的醛固酮合酶抑制剂显得更为合理,可类比“药物性肾上腺切除术”。
然而,由于原发性醛固酮增多症属于少见病(这一现状很大程度上由其低确诊率导致),很难推动研究者针对该疾病开展规范的药物临床试验。事实上,依普利酮在临床中常被超适应证用于原发性醛固酮增多症的治疗。
baxdrostat在原发性醛固酮增多症的初步证据
baxdrostat针对原发性醛固酮增多症的临床试验的开展,令高血压领域的研究者与临床医师感到振奋。该研究为一项单臂Ⅱ期试验[2],评估了baxdrostat在15例原发性醛固酮增多症患者中长达72周的疗效。治疗初始剂量为 2 mg,连续给药 4 周;后续根据患者的血压应答情况,逐步将剂量上调至 4 mg 及 8 mg(图1)。
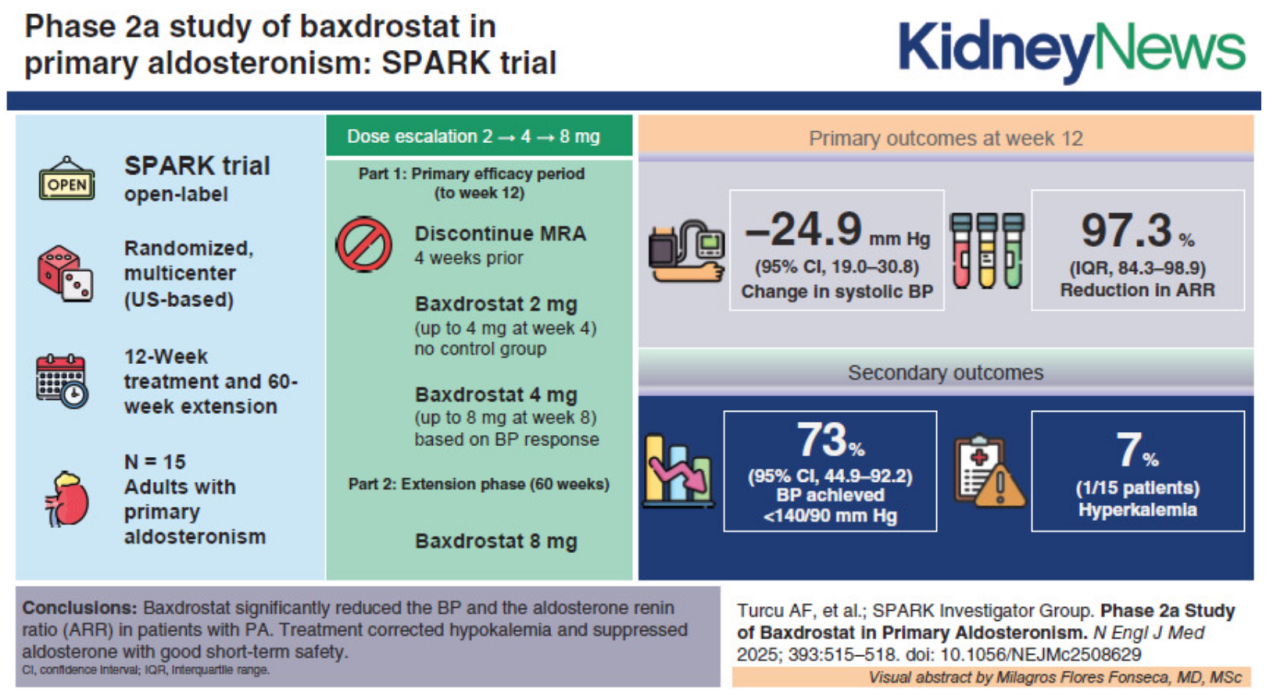
主要发现包括:
血压与生化反应:治疗12周时,患者的平均收缩压较基线水平(约 151 mmHg)下降约 25 mmHg,15 例患者中有10例实现了血清钾水平的正常化(图1)。
激素水平:血浆及24小时尿醛固酮水平急剧下降(降幅达97%),同时血浆肾素活性至72周时逐渐升高6倍。
机制启示与安全性:试验同时观察到患者脱氧皮质酮水平的双相波动(先升高后降低)及血浆皮质醇的轻度升高,其机制与肾上腺皮质生理反馈相关。97%的醛固酮抑制效果,足以让人将其作用与原发性醛固酮增多症的外科治疗相媲美 —— 从某种意义上说,其效果相当于 “药物性肾上腺切除术”。
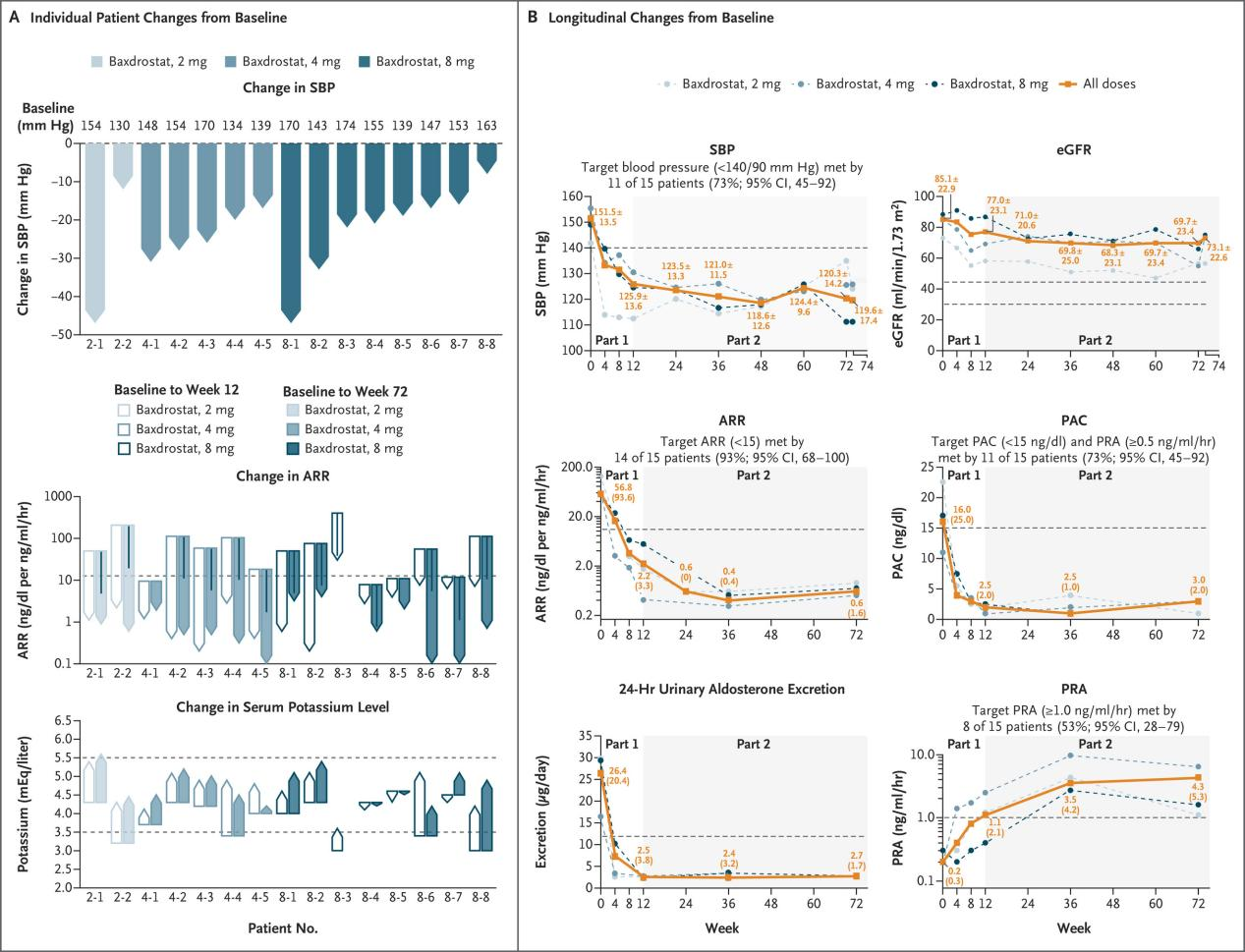
图1. 治疗原发性醛固酮增多症患者的疗效与安全性特征(图A展示了每位患者的收缩压[SBP]、血浆醛固酮 - 肾素比值[ARR]及血清钾水平相较于基线的变化情况;图B展示了SBP、估算肾小球滤过率[eGFR]、ARR、血浆醛固酮浓度[PAC])
展望与挑战
尽管baxdrostat在原发性醛固酮增多症中显示出显著的降压及生化改善效果,但本研究作为一项样本量较小的的Ⅱ期单臂试验,既未设置对照组,也未纳入螺内酯等阳性对照药物,因此结论仍需谨慎解读,目前断言该药物取得 “突破性成功” 还为时过早。
尽管如此,这些试验数据仍具有极高的临床价值与应用前景。相较于在未控制的高血压或蛋白尿性肾病等已有多种治疗方案的领域中应用,醛固酮合酶抑制剂在原发性醛固酮增多症这一治疗需求更迫切的领域可能更具价值。 若后续试验成功,此类药物的上市或许能反向推动目前低迷的原发性醛固酮增多症筛查率。
目前,Ⅲ期临床试验BaxPA(NCT07007793)已启动招募,旨在进一步验证醛固酮合酶抑制剂在原发性醛固酮增多症中的疗效与安全性。醛固酮合酶抑制剂能否开创原发性醛固酮增多症治疗新纪元,值得期待。
参考文献
1.Milagros Flores Fonseca, Cristina Popa and Swapnil Hiremath. The Dawn of the Aldosterone Synthase Inhibitors. KidneyNews Online. Publication Date: 08 Dec 2025. DOI: https://doi.org/10.62716/kn.002222025.2.Turcu AF, et al. Phase 2a study of baxdrostat in primary aldosteronism. N Engl J Med 2025.
- 推荐文章
