- 首页 > 正文
外周血与肾间质T细胞谱:狼疮肾炎治疗反应的关键预测指标
发表时间:2026-04-26 10:56:52
编者按
狼疮肾炎是系统性红斑狼疮最常见且严重的脏器并发症,约30%~40%患者对常规免疫抑制治疗反应不佳,易进展为慢性肾脏病乃至终末期肾病。当前临床缺乏精准预测治疗反应的生物标志物,难以实现个体化分层治疗。南京金陵医院团队基于424例狼疮肾炎患者的回顾性队列研究,系统揭示外周血与肾间质T细胞亚群失衡与治疗缓解的密切关联,证实CD4/CD8比值可作为无创、便捷的疗效预测指标(图1),并阐明肾间质T细胞浸润在全身免疫状态与临床结局间的中介作用,为狼疮肾炎的精准诊疗提供重要循证依据与新靶点思路。
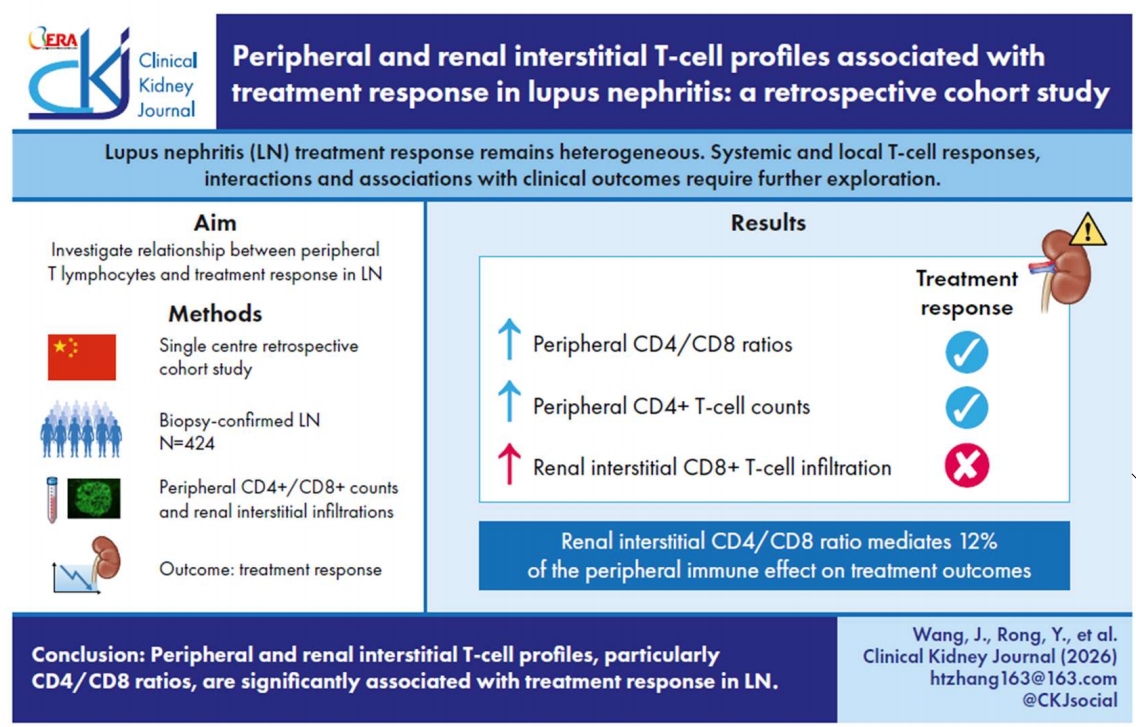
图1. 研究概览
一、研究背景与科学问题
狼疮肾炎(LN)是系统性红斑狼疮(SLE)累及肾脏的炎症性病变,以免疫复合物沉积、肾小球损伤及间质炎症为核心病理特征。临床主流方案为糖皮质激素联合环磷酰胺、吗替麦考酚酯、钙调磷酸酶抑制剂等免疫抑制剂,贝利尤单抗、奥妥珠单抗等生物制剂亦逐步应用于临床。但治疗反应异质性显著,30%~40%患者呈现难治或复发状态,长期预后不佳。
T细胞免疫紊乱是狼疮肾炎发病的核心环节,但特定T细胞亚群的临床意义尚不明确。虽然T细胞可通过直接细胞毒性作用与辅助B细胞活化等途径促进肾损伤,但各亚群的动态变化与疾病的关联仍存在矛盾结论。外周血CD4+/CD8+比值降低与疾病活动度升高相关,CD8+ T细胞的持续存在则可预测免疫抑制治疗耐药。在肾组织中,CD8+ T细胞在所有类型狼疮肾炎的浸润细胞中均占主导地位,且在所有肾实质区域的数量均超过CD4+ T细胞。关键的是,肾内CD8+ T细胞密度与组织学损伤严重程度直接相关,而CD4+ T细胞浸润未显示出此类关联。与此相反,尿液中CD4+/CD8+比值升高与蛋白尿相关。
外周免疫与肾脏局部免疫有何关联?T细胞亚群能否预测治疗反应?肾间质T细胞是否介导全身免疫对临床结局有何影响?这些尚未在大样本队列中系统阐明。
因此,南京金陵医院研究人员以2010~2017年在本院经肾活检确诊的424例狼疮肾炎患者为对象(图2),采用流式细胞术检测外周血T细胞亚群、免疫组化定量肾间质T细胞浸润,探讨T细胞谱与治疗缓解的关系,并开展中介效应分析,旨在发现可用于预后分层的生物标志物,揭示免疫失衡驱动治疗抵抗的机制。
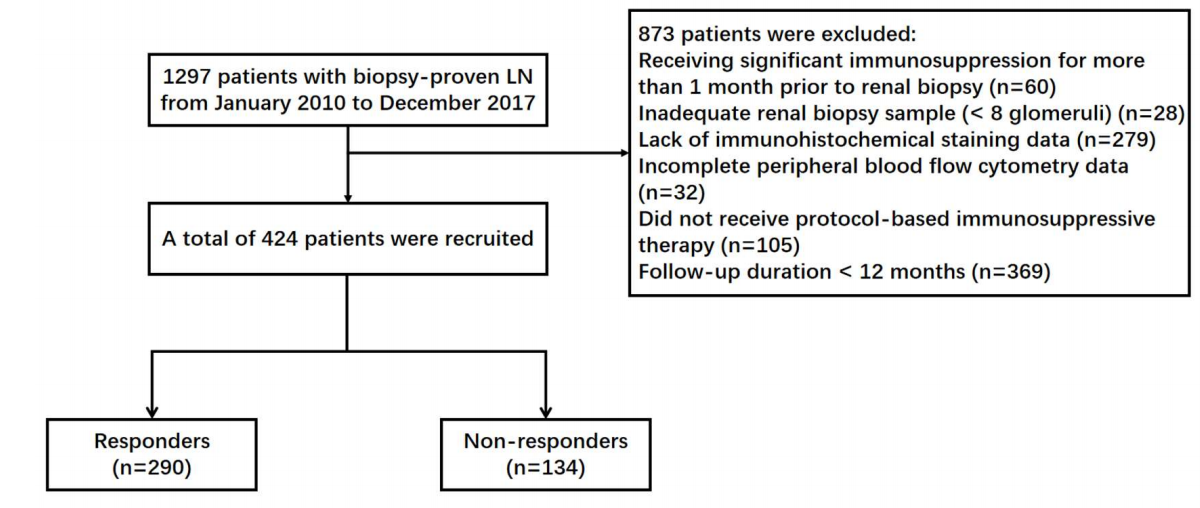
图2. 研究患者入组流程图
本研究中,治疗缓解定义为12个月内达到完全缓解(24小时尿蛋白<0.4 g,血清肌酐正常)或部分缓解(尿蛋白下降≥50%、<3.5 g/24h,白蛋白≥30 g/L,肌酐无明显升高);未达上述标准为非缓解者。
二、核心研究结果
(一)基线特征与治疗缓解分布
424例LN患者中,女性占84.67%,平均年龄为30.37±11.18岁(表1)。
表1. 按免疫抑制治疗反应分层的狼疮肾炎患者基线人口学与临床特征
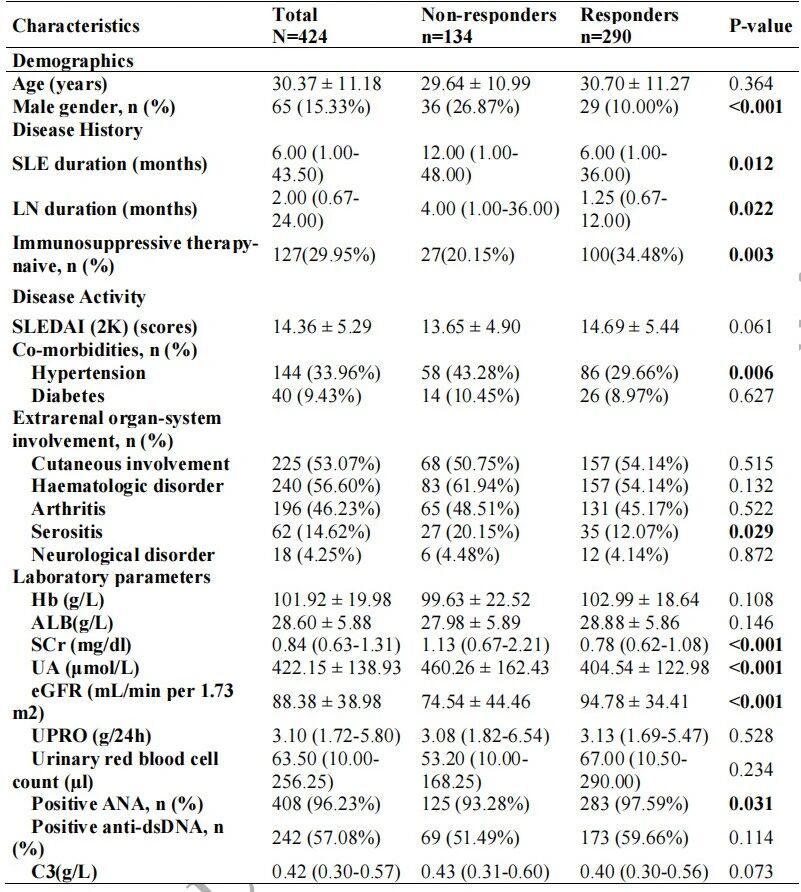
根据肾活检时12个月内的免疫抑制反应,对患者基线特征进行分层分析(表1、表2)。424例患者中,缓解者290例(68.40%),非缓解者134例(31.60%)。缓解组与非缓解组之间存在显著差异:缓解组SLE及狼疮肾炎病程更短,高血压患病率更低,血清肌酐、尿酸水平更低,估算肾小球滤过率更高(表1);病理层面,缓解组慢性指数、全球硬化、节段硬化、新月体形成比例、急性肾小管损伤及间质纤维化程度均显著低于非缓解组(表3)。
治疗方案包括激素联合多靶点治疗(123例,29.01%)、环磷酰胺(110例,25.94%)、吗替麦考酚酯(74例,17.45%)、钙调磷酸酶抑制剂(67例,15.80%)及其他方案(50例,11.79%),各组间治疗方案分布无显著差异(表2)。
表2. 按免疫抑制治疗反应分层的基线治疗方案与T细胞谱特征
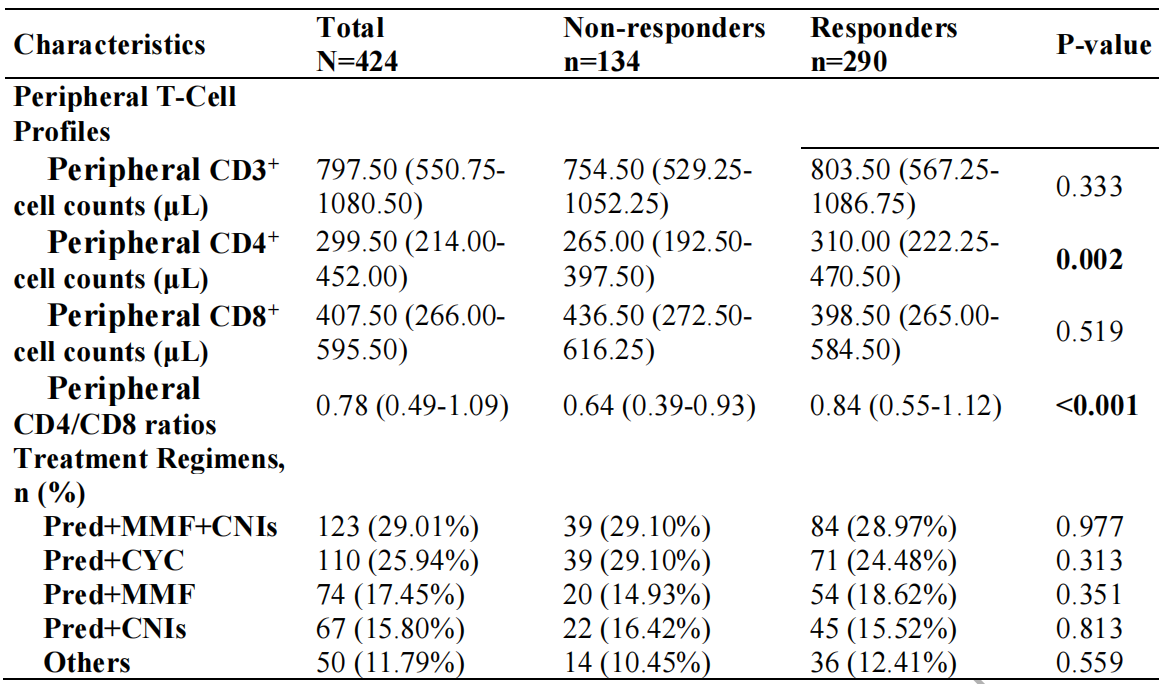
表3. 按免疫抑制治疗反应分层的狼疮肾炎患者病理特征

(二)外周血T细胞谱与治疗反应显著相关
缓解组外周血CD4+ T细胞计数(中位数310 vs. 265/μL,P=0.002)、CD4+/CD8+比值(0.84 vs. 0.64,P<0.001)显著高于非缓解组;CD8+ T细胞计数两组无差异(表2)。
多因素校正后,外周血CD4+ T细胞计数升高与治疗缓解正相关(OR=1.002,95%CI:1.001~1.003);CD4/CD8比值的预测价值更突出,校正后OR=2.462(95%CI:1.414~4.288),经Bonferroni校正后仍具有统计学意义。三分位分析显示,CD4/CD8比值最高组较最低组治疗缓解概率提升2.697倍,呈显著剂量效应关系(表5)。
(三)肾间质T细胞浸润是治疗抵抗的重要标志
非缓解组肾间质CD4+、CD8+ T细胞浸润密度显著高于缓解组(CD4+:136 vs. 80 cells/mm²;CD8+:148 vs. 80 cells/mm²,均P<0.001)。多因素校正后,肾间质CD8+ T细胞密度升高与治疗非缓解密切相关(OR=0.343,95%CI:0.177~0.666);肾间质CD4+/CD8+比值升高则是缓解的强预测因子(OR=8.312,95%CI:2.593~26.645)。
(四)外周血CD4+/CD8+比值提升传统模型预测效能
将外周血CD4+/CD8+比值加入包含SLEDAI、eGFR、24小时尿蛋白、活动指数、慢性指数的基础预测模型,曲线下面积(AUC)由0.678提升至0.711(差异P值为0.022),净重新分类指数与综合判别改善指数均显著提升,提示该指标可独立提升疗效预测准确性。
(五)肾间质CD4+/CD8+比值具有中介效应
中介分析显示,外周血CD4+/CD8+比值通过肾间质CD4+/CD8+比值影响治疗反应,中介效应占比11.97%(间接效应β=0.011,P=0.01)(图3),证实肾脏局部T细胞重塑是全身免疫失衡影响临床结局的重要通路。
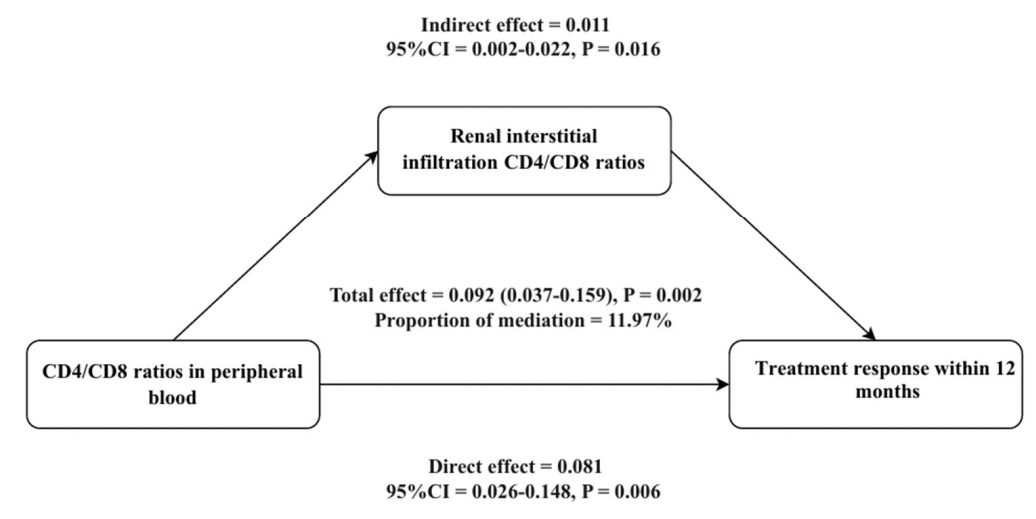
图3. 肾间质CD4/CD8比值介导了外周CD4/CD8比值对治疗反应的影响
(六)外周血CD4+/CD8+比值与长期肾脏预后相关
中位随访6.91年,57例(13.4%)达到肾脏复合终点(肌酐翻倍或终末期肾病)。外周血CD4+/CD8+比值高于中位数者肾脏生存率显著更高(Log?rank P=0.0034);单因素Cox回归显示,高比值组复合终点风险降低56%(HR=0.44,P=0.0043),校正人口学与疾病活动指标后关联仍显著,完全校正后效应减弱但趋势保留。
三、机制阐释与临床意义
(一)T细胞失衡驱动狼疮肾炎治疗抵抗的机制
外周血CD4+ T细胞减少与趋化迁移
缓解者外周血CD4+ T细胞相对充足,非缓解者CD4+ T细胞向肾组织募集,导致外周耗竭、局部过度浸润,放大炎症损伤。
CD8+ T细胞的细胞毒性损伤
肾间质CD8+ T细胞通过释放穿孔素、颗粒酶直接损伤足细胞与肾小管上皮细胞,加重蛋白尿与肾功能下降,是病理损伤与治疗抵抗的关键效应细胞。
Ⅰ型干扰素通路过度激活
非缓解者低CD4+/CD8+比值提示Ⅰ型干扰素信号活化,抑制初始CD4+ T细胞增殖、加剧淋巴细胞减少,介导免疫紊乱与治疗耐药。
(二)临床转化价值
无创生物标志物用于预后分层
外周血CD4/CD8比值检测便捷、可重复,可在肾活检前快速筛选高危难治患者,指导强化治疗或早期切换生物制剂。
肾间质T细胞作为治疗新靶点
以CD8+ T细胞浸润、CD4/CD8失衡为靶点,开发靶向肾脏局部免疫的干预策略,有望改善难治性狼疮肾炎预后。
精准免疫评估优化个体化方案
联合外周与肾组织T细胞谱,比单一指标更准确划分免疫表型,实现“全身—局部”一体化精准诊疗。
四、研究局限性与展望
本研究为单中心回顾性研究,人群以中国年轻女性增殖型狼疮肾炎为主,结论需在其他种族、病理亚型及生物制剂治疗队列中外部验证;未评估治疗对T细胞亚群的动态影响,缺乏感染、年龄相关免疫衰老等混杂因素的系统校正;免疫组化定量存在方法学变异,未来可结合单细胞测序、空间转录组技术深化机制研究。
后续应开展前瞻性队列研究,动态监测外周血CD4/CD8比值变化,探索其指导治疗调整的阈值;针对肾间质CD8+ T细胞开展干预研究,开发靶向肾脏免疫的精准疗法;构建包含T细胞谱的预测模型,实现狼疮肾炎疗效与长期预后的智能化评估。
五、结论
外周血与肾间质T细胞谱,尤其是CD4/CD8比值,是狼疮肾炎治疗反应的重要预测指标。外周血高CD4/CD8比值提示更佳治疗缓解与长期肾脏预后,肾间质高CD8+ T细胞浸润与低CD4/CD8比值则预示治疗抵抗;肾间质CD4/CD8比值部分介导外周免疫状态对临床结局的影响。本研究为狼疮肾炎的免疫分型、疗效预测与个体化治疗提供了高质量临床证据,推动狼疮肾炎从经验治疗向精准免疫诊疗转变。
狼疮肾炎是系统性红斑狼疮最常见且严重的脏器并发症,约30%~40%患者对常规免疫抑制治疗反应不佳,易进展为慢性肾脏病乃至终末期肾病。当前临床缺乏精准预测治疗反应的生物标志物,难以实现个体化分层治疗。南京金陵医院团队基于424例狼疮肾炎患者的回顾性队列研究,系统揭示外周血与肾间质T细胞亚群失衡与治疗缓解的密切关联,证实CD4/CD8比值可作为无创、便捷的疗效预测指标(图1),并阐明肾间质T细胞浸润在全身免疫状态与临床结局间的中介作用,为狼疮肾炎的精准诊疗提供重要循证依据与新靶点思路。

图1. 研究概览
一、研究背景与科学问题
狼疮肾炎(LN)是系统性红斑狼疮(SLE)累及肾脏的炎症性病变,以免疫复合物沉积、肾小球损伤及间质炎症为核心病理特征。临床主流方案为糖皮质激素联合环磷酰胺、吗替麦考酚酯、钙调磷酸酶抑制剂等免疫抑制剂,贝利尤单抗、奥妥珠单抗等生物制剂亦逐步应用于临床。但治疗反应异质性显著,30%~40%患者呈现难治或复发状态,长期预后不佳。
T细胞免疫紊乱是狼疮肾炎发病的核心环节,但特定T细胞亚群的临床意义尚不明确。虽然T细胞可通过直接细胞毒性作用与辅助B细胞活化等途径促进肾损伤,但各亚群的动态变化与疾病的关联仍存在矛盾结论。外周血CD4+/CD8+比值降低与疾病活动度升高相关,CD8+ T细胞的持续存在则可预测免疫抑制治疗耐药。在肾组织中,CD8+ T细胞在所有类型狼疮肾炎的浸润细胞中均占主导地位,且在所有肾实质区域的数量均超过CD4+ T细胞。关键的是,肾内CD8+ T细胞密度与组织学损伤严重程度直接相关,而CD4+ T细胞浸润未显示出此类关联。与此相反,尿液中CD4+/CD8+比值升高与蛋白尿相关。
外周免疫与肾脏局部免疫有何关联?T细胞亚群能否预测治疗反应?肾间质T细胞是否介导全身免疫对临床结局有何影响?这些尚未在大样本队列中系统阐明。
因此,南京金陵医院研究人员以2010~2017年在本院经肾活检确诊的424例狼疮肾炎患者为对象(图2),采用流式细胞术检测外周血T细胞亚群、免疫组化定量肾间质T细胞浸润,探讨T细胞谱与治疗缓解的关系,并开展中介效应分析,旨在发现可用于预后分层的生物标志物,揭示免疫失衡驱动治疗抵抗的机制。

图2. 研究患者入组流程图
本研究中,治疗缓解定义为12个月内达到完全缓解(24小时尿蛋白<0.4 g,血清肌酐正常)或部分缓解(尿蛋白下降≥50%、<3.5 g/24h,白蛋白≥30 g/L,肌酐无明显升高);未达上述标准为非缓解者。
二、核心研究结果
(一)基线特征与治疗缓解分布
424例LN患者中,女性占84.67%,平均年龄为30.37±11.18岁(表1)。
表1. 按免疫抑制治疗反应分层的狼疮肾炎患者基线人口学与临床特征

根据肾活检时12个月内的免疫抑制反应,对患者基线特征进行分层分析(表1、表2)。424例患者中,缓解者290例(68.40%),非缓解者134例(31.60%)。缓解组与非缓解组之间存在显著差异:缓解组SLE及狼疮肾炎病程更短,高血压患病率更低,血清肌酐、尿酸水平更低,估算肾小球滤过率更高(表1);病理层面,缓解组慢性指数、全球硬化、节段硬化、新月体形成比例、急性肾小管损伤及间质纤维化程度均显著低于非缓解组(表3)。
治疗方案包括激素联合多靶点治疗(123例,29.01%)、环磷酰胺(110例,25.94%)、吗替麦考酚酯(74例,17.45%)、钙调磷酸酶抑制剂(67例,15.80%)及其他方案(50例,11.79%),各组间治疗方案分布无显著差异(表2)。
表2. 按免疫抑制治疗反应分层的基线治疗方案与T细胞谱特征

表3. 按免疫抑制治疗反应分层的狼疮肾炎患者病理特征

(二)外周血T细胞谱与治疗反应显著相关
缓解组外周血CD4+ T细胞计数(中位数310 vs. 265/μL,P=0.002)、CD4+/CD8+比值(0.84 vs. 0.64,P<0.001)显著高于非缓解组;CD8+ T细胞计数两组无差异(表2)。
多因素校正后,外周血CD4+ T细胞计数升高与治疗缓解正相关(OR=1.002,95%CI:1.001~1.003);CD4/CD8比值的预测价值更突出,校正后OR=2.462(95%CI:1.414~4.288),经Bonferroni校正后仍具有统计学意义。三分位分析显示,CD4/CD8比值最高组较最低组治疗缓解概率提升2.697倍,呈显著剂量效应关系(表5)。
(三)肾间质T细胞浸润是治疗抵抗的重要标志
非缓解组肾间质CD4+、CD8+ T细胞浸润密度显著高于缓解组(CD4+:136 vs. 80 cells/mm²;CD8+:148 vs. 80 cells/mm²,均P<0.001)。多因素校正后,肾间质CD8+ T细胞密度升高与治疗非缓解密切相关(OR=0.343,95%CI:0.177~0.666);肾间质CD4+/CD8+比值升高则是缓解的强预测因子(OR=8.312,95%CI:2.593~26.645)。
(四)外周血CD4+/CD8+比值提升传统模型预测效能
将外周血CD4+/CD8+比值加入包含SLEDAI、eGFR、24小时尿蛋白、活动指数、慢性指数的基础预测模型,曲线下面积(AUC)由0.678提升至0.711(差异P值为0.022),净重新分类指数与综合判别改善指数均显著提升,提示该指标可独立提升疗效预测准确性。
(五)肾间质CD4+/CD8+比值具有中介效应
中介分析显示,外周血CD4+/CD8+比值通过肾间质CD4+/CD8+比值影响治疗反应,中介效应占比11.97%(间接效应β=0.011,P=0.01)(图3),证实肾脏局部T细胞重塑是全身免疫失衡影响临床结局的重要通路。

图3. 肾间质CD4/CD8比值介导了外周CD4/CD8比值对治疗反应的影响
(六)外周血CD4+/CD8+比值与长期肾脏预后相关
中位随访6.91年,57例(13.4%)达到肾脏复合终点(肌酐翻倍或终末期肾病)。外周血CD4+/CD8+比值高于中位数者肾脏生存率显著更高(Log?rank P=0.0034);单因素Cox回归显示,高比值组复合终点风险降低56%(HR=0.44,P=0.0043),校正人口学与疾病活动指标后关联仍显著,完全校正后效应减弱但趋势保留。
三、机制阐释与临床意义
(一)T细胞失衡驱动狼疮肾炎治疗抵抗的机制
外周血CD4+ T细胞减少与趋化迁移
缓解者外周血CD4+ T细胞相对充足,非缓解者CD4+ T细胞向肾组织募集,导致外周耗竭、局部过度浸润,放大炎症损伤。
CD8+ T细胞的细胞毒性损伤
肾间质CD8+ T细胞通过释放穿孔素、颗粒酶直接损伤足细胞与肾小管上皮细胞,加重蛋白尿与肾功能下降,是病理损伤与治疗抵抗的关键效应细胞。
Ⅰ型干扰素通路过度激活
非缓解者低CD4+/CD8+比值提示Ⅰ型干扰素信号活化,抑制初始CD4+ T细胞增殖、加剧淋巴细胞减少,介导免疫紊乱与治疗耐药。
(二)临床转化价值
无创生物标志物用于预后分层
外周血CD4/CD8比值检测便捷、可重复,可在肾活检前快速筛选高危难治患者,指导强化治疗或早期切换生物制剂。
肾间质T细胞作为治疗新靶点
以CD8+ T细胞浸润、CD4/CD8失衡为靶点,开发靶向肾脏局部免疫的干预策略,有望改善难治性狼疮肾炎预后。
精准免疫评估优化个体化方案
联合外周与肾组织T细胞谱,比单一指标更准确划分免疫表型,实现“全身—局部”一体化精准诊疗。
四、研究局限性与展望
本研究为单中心回顾性研究,人群以中国年轻女性增殖型狼疮肾炎为主,结论需在其他种族、病理亚型及生物制剂治疗队列中外部验证;未评估治疗对T细胞亚群的动态影响,缺乏感染、年龄相关免疫衰老等混杂因素的系统校正;免疫组化定量存在方法学变异,未来可结合单细胞测序、空间转录组技术深化机制研究。
后续应开展前瞻性队列研究,动态监测外周血CD4/CD8比值变化,探索其指导治疗调整的阈值;针对肾间质CD8+ T细胞开展干预研究,开发靶向肾脏免疫的精准疗法;构建包含T细胞谱的预测模型,实现狼疮肾炎疗效与长期预后的智能化评估。
五、结论
外周血与肾间质T细胞谱,尤其是CD4/CD8比值,是狼疮肾炎治疗反应的重要预测指标。外周血高CD4/CD8比值提示更佳治疗缓解与长期肾脏预后,肾间质高CD8+ T细胞浸润与低CD4/CD8比值则预示治疗抵抗;肾间质CD4/CD8比值部分介导外周免疫状态对临床结局的影响。本研究为狼疮肾炎的免疫分型、疗效预测与个体化治疗提供了高质量临床证据,推动狼疮肾炎从经验治疗向精准免疫诊疗转变。
- 推荐文章
ERA专家访谈丨顾乐怡教授:补体相关肾病治疗格局的范式跃迁,口服盐酸兰诺可泮治疗lgA肾病12周尿蛋白达标率高达40%
ERA中国之声 | 东南大学肾内科团队多项研究揭秘急性肾损伤全新作用机制
ERA中国之声丨UMOD H36Y突变如何通过代谢重编程加速肾小管衰老?
ERA专家访谈丨马坤岭教授:补体靶向治疗的“靶点前移”与“近端阻断”,口服盐酸兰诺可泮治疗IgA肾病12周尿蛋白达标率高达40%
ERA中国之声 | 重磅临床发现:抑酸药使用量与腹膜透析患者骨折风险呈梯度相关
ERA中国之声丨Dotinurad通过Nrf2介导的线粒体质量控制发挥直接肾小管保护作用,且该效应不依赖URAT1抑制
2026 ERA研究揭示从认知革新到实践破局的全球图景
江苏省中医院双项成果亮相ERA大会:靶向CTRP1-SGLT2与O-GlcNAc-FAO代谢记忆轴,破解糖尿病肾病发病新机制
ERA专家访谈丨路万虹教授:补体抑制剂助力IgA肾病早期、精准缓解,口服盐酸兰诺可泮治疗12周尿蛋白达标率高达40%
ERA中外专家研讨|聚焦IgA肾病前沿进展,解析临床对因治疗新看点
ERA 2026 | Crovalimab治疗成人及儿童aHUS:COMMUTE-a与COMMUTE-p Ⅲ期研究均达主要终点
ERA 2026 | 12周尿蛋白达标率高达40%,UPCR降幅51.8%!口服补体抑制剂盐酸兰诺可泮IgAN Ⅱ期高影响力研究数据全球首发
AI时代下聚焦批判性思维、技术创新与人文关怀!第63届ERA圆满闭幕,下一站鹿特丹
会议报道:从临床痛点出发,探寻IgA肾病长期管理最优解丨“肾英无界・中外IgA肾病学术前沿对话”成都站圆满收官
ERA 中国之声 | 华西医院30余项研究入选大会交流,4项研究上榜“青年作者优秀摘要”
全球首个APRIL靶向生物制剂斯贝利单抗在华获批,用于治疗IgA肾病
ERA 2026十佳摘要丨已用SGLT2i的2型糖尿病患者,联用GLP-1RA可再降27%肾病进展风险,全肾功能区间获益一致
ERA 2026前沿:三大新机制破局,CKD诊疗格局迎关键转折
ERA 2026重磅研究 | ALIGN试验2.5年eGFR结果:阿曲生坦治疗IgA肾病可显著、持续延缓肾功能下降
ERA 2026|9个月应答不佳仍具长期肾保护,NefIgArd亚组分析为IgA肾病对因治疗决策提供重磅证据【锁定今晚直播,洞悉2026 KDIGO更新要点】
ERA2026重磅研究丨FLOW试验最新数据:司美格鲁肽改善慢性肾脏病合并2型糖尿病患者生活质量
ERA 2026前沿 | 突破诊疗壁垒,迈向全程管理:构建以SGLT2i为核心的CKD早筛早诊早治新格局
ERA 2026十佳摘要丨中国台湾长庚医院单细胞图谱揭秘多囊肾发病源头,锁定全新靶向治疗靶点
ERA 2026丨突破9个月疗程,布地奈德肠溶胶囊长程治疗,为IgA肾病患者带来持久肾功能保护
ERA 2026 | 香港大学研究揭示:脂联素经线粒体重塑途径改善糖胖病相关肾损伤
杨淑敏教授:被忽视的20%——内分泌性高血压筛查专家共识解读
ERA 2026格拉斯哥正式启幕!以开放思维锚定肾病未来,《柳叶刀》重磅数据敲响CKD全球防控警钟
ERA 2026重磅丨IgA肾病尽早对因治疗:锚定蛋白尿≥0.5 g/d肾病进展风险人群,早用早达标、护肾更及时
ERA 2026前沿 | 突破“5.0时代”,迈向长期管理:真实世界研究驱动高钾血症诊疗变革
血液透析患者高血压管理的十个核心建议:基于ERA共识的临床实践指导
陈莉明教授:糖尿病慢性肾脏病的修正策略——从流行病学到多靶点治疗 | PUDF 2026
会议报道:聚焦临床痛点 共谋全程管理丨“肾英无界”中外IgA肾病学术前沿对话北京站成功举办
从AI到异种移植:ERA 2026最值得关注的五大未来技术
CIC 2026 | 任景怡教授:醛固酮介导心衰进展,nsMRA带来全新突破——从机制到临床的精准制导
ERA 2026三大临床试验专场:IgA肾病、CKD与罕见肾病治疗格局或将迎来新变化
何娅妮教授:糖尿病肾病治疗策略新进展——GDMT四大支柱筑牢心肾防线
Vadadustat(每周三次)对比不同基线剂量的甲氧基聚乙二醇促红素β治疗透析依赖型慢性肾病贫血患者的疗效与安全性分析
CCBPC 2026|涂晓文教授:血浆净化技术及其临床应用新进展
ERA 2026开幕在即!“Open your mind”背后,肾脏病学正在发生哪些改变?
ERA 2026|布地奈德肠溶胶囊23项全新研究闪耀登场,多维夯实对因、尽早、长期治疗临床证据体系
“生命之河”堵塞,肾脏告急!警惕“堵”出来的肾病——梗阻性肾病
中美双队列研究:不合并ASCVD的CKD患者,他汀治疗降低死亡风险26%~39%
会议报道:开放视野 探索前沿丨“肾英无界”中外IgA肾病学术前沿对话上海站圆满落幕
学术纵横丨常染色体显性多囊肾病(ADPKD)最新学术进展:风险评估、人群特征与创新药物探索
病例分享 | 血糖不高却频发酮症!这例糖尿病背后藏着双重隐秘病因,解密糖尿病胃轻瘫与肾糖阈减低的恶性循环
张宏教授:立足机制,解析B细胞靶向治疗IgA肾病的最新进展
肾移植术后膜性肾病研究:首个覆盖复发、未复发与新发类型的系统回顾与Meta分析核心结论与临床启示
压力与心血管疾病:成人期的隐形杀手
周晓霜教授:临床常规代谢指标与IgA肾病肾功能及病理损伤程度显著相关
非典型溶血尿毒综合征(aHUS)多学科诊疗专家共识要点,补体抑制剂为一线首选治疗
崔兆强教授:从“单纯降压”到“综合获益”——深度解析高血压治疗新趋势
以问破局 以共识远——《IgA肾病临床实践60问(2026版)》重磅发布,直击临床痛点,全面解锁IgA肾病对因治疗
开放思维,共探肾学前沿——第63届ERA大会即将启幕!26项中国研究入选最佳/优秀摘要
孙宁玲教授:破局“高容量”——从评估到干预,高血压管理如何走出困境?
CCBPC 2026|马坤岭教授:肠道菌群介导DKD肾损伤机制及转化应用新进展
