- 首页 > 正文
WCN 2026丨ISN-ISGD联合会议聚焦足细胞损伤精准诊疗前沿进展:从自身抗体内型分型到全新靶点突破
发表时间:2026-04-26 09:04:50
编者按
长期以来,肾小球疾病的诊疗面临“同病异治、异病同治”的经验性治疗局限,而足细胞作为肾小球疾病损伤的核心靶点,其相关机制与转化研究始终是领域的核心热点。2026年3月29日,世界肾脏病学大会(WCN 2026)大会上,国际肾脏病学会(ISN)与国际肾小球疾病学会(ISGD)联合专场带来了肾小球疾病诊疗的一系列颠覆性成果。全球顶尖肾病学者围绕原发性肾病综合征、足细胞病的发病机制、精准分型、生物标志物与靶向治疗进展展开深度分享。本文基于本场重磅学术报告,系统梳理前沿进展,为肾小球疾病的精准分型与靶向干预提供了重要学术参考。

一、原发性肾病综合征中靶向足细胞特异性抗原的自身抗体
来自德国汉堡大学医学中心的Tobias B. Huber教授首先描述了ISGD的愿景与使命,指出当前肾小球疾病的传统诊断长期依赖临床表现与描述性组织学特征,将微小病变(MCD)、局灶节段性肾小球硬化(FSGS)等归为独立疾病类型,但这种组织学分型无法揭示疾病的潜在病理生理机制,难以实现精准的个体化药物选择与通路靶向治疗[1]。Huber教授强调,肾小球疾病的分类应向内型(endotype)转变,即基于病因学的分类策略,涵盖自身免疫、遗传、适应性、感染性及药物/毒素相关等多种致病机制[2]。
随后,Huber教授重点阐述了抗nephrin自身抗体在MCD及特发性肾病综合征(INS)中的研究进展。Nephrin是足细胞裂孔隔膜的关键组成蛋白,早期研究已证实其缺失可导致先天性肾病综合征。抗nephrin自身抗体可与足细胞足突上的nephrin结合,导致裂孔隔膜磷酸化和内吞,引发白蛋白尿和足突融合,定义了一种新的疾病内型——抗nephrin足细胞病[3,4](图1)。
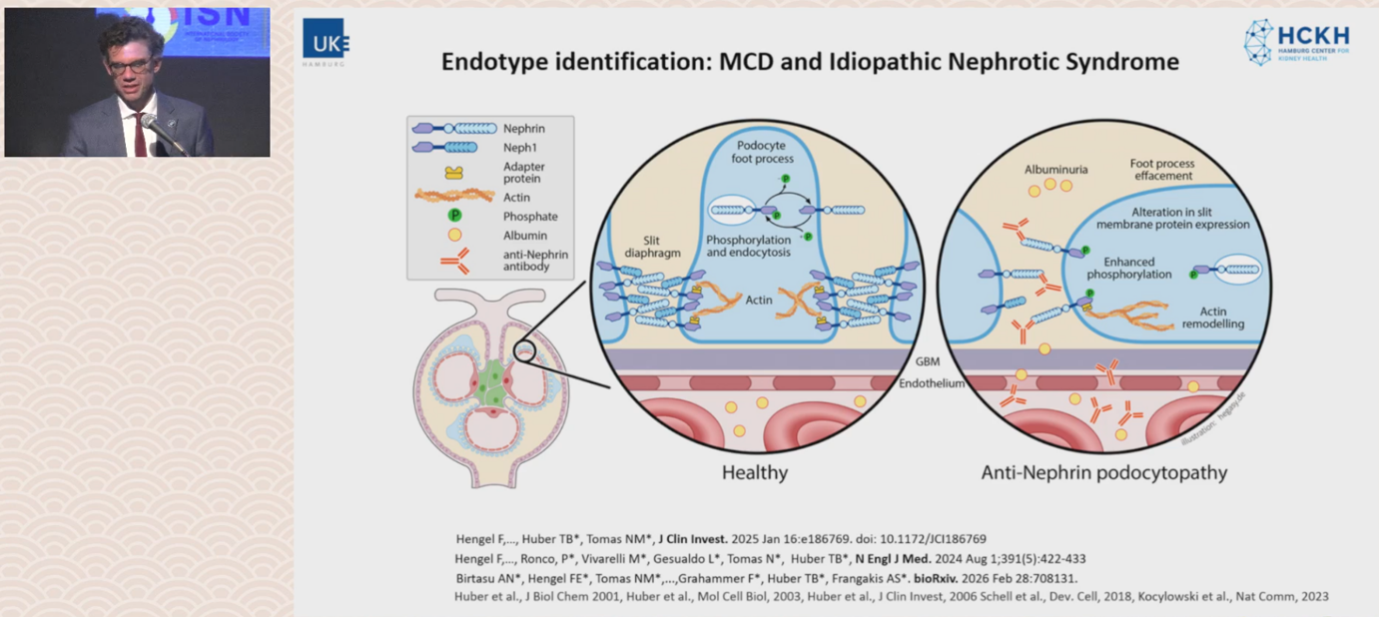
图1. MCD/INS的内型识别:抗Nephrin 介导足细胞病的致病机制
流行病学数据显示,抗nephrin自身抗体在多重耐药-激素耐药肾病综合征(MDR-SRNS)的MCD患者中阳性率极高,成人患者达70%,儿童患者更是高达90%,而在遗传性SRNS患者中阳性率极低,提示该抗体是特定肾病内型的核心致病因子[5]。抗nephrin自身抗体滴度与患者疾病活动度、蛋白尿水平显著相关,可有效预测患者对治疗的应答情况与FSGS复发风险。针对抗nephrin抗体灵敏度不足的问题,Huber教授团队开发了生物素-链霉亲和素增强ELISA、免疫沉淀-ELISA杂交检测体系[4](图2)。
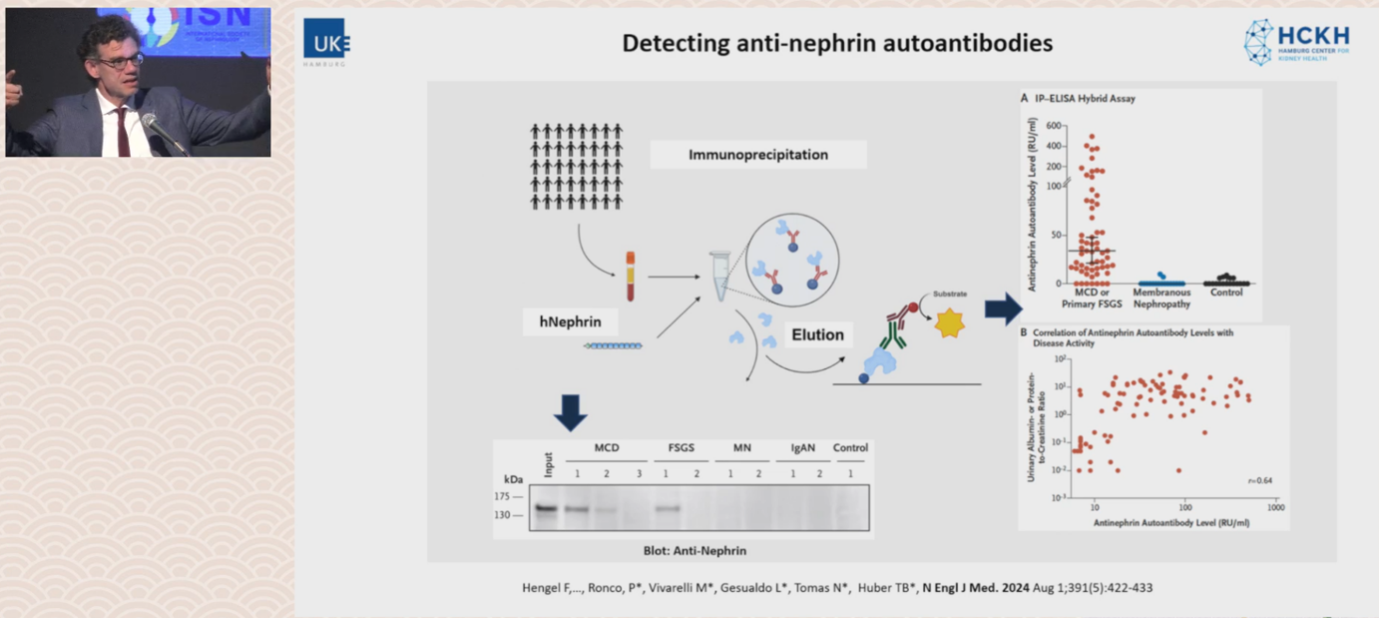
图2. 抗Nephrin自身抗体的检测体系建立与临床应用验证
治疗层面,研究发现激素治疗可显著下调抗nephrin阳性患者的浆母细胞水平,而利妥昔单抗等B细胞清除治疗可有效降低抗体滴度并诱导疾病缓解[6]。值得注意的是,在FSGS肾移植复发队列(TANGO联盟)中也检测到抗nephrin抗体,提示该抗体可能预测移植后复发。Huber教授还介绍了无创诊断的初步探索:对于不能或不愿接受肾活检的患者,通过检测循环中抗nephrin抗体亚类即可辅助诊断并启动治疗[7]。
二、NEPTUNE与CureGN队列研究的最新进展
精准医学的核心是实现“机制与患者的精准匹配”,而高质量的临床队列与生物样本库是肾病靶点发现、药物研发与临床试验设计的核心基础。美国迈阿密大学米勒医学院Alessia Fornoni教授介绍了两大北美肾小球疾病队列研究——肾病综合征研究网络(NEPTUNE)和治愈肾小球肾炎(CureGN)项目的最新成果与转化应用。
NEPTUNE(肾病综合征研究网络)队列于2009年正式建立,覆盖北美32个临床招募中心,核心纳入FSGS、MCD、膜性肾病(MN)、Alport综合征等肾小球疾病患者,建立了超25.8万份生物样本库,整合临床随访、肾脏活检组学、全基因组测序等多维数据,核心用于精准分型、靶点发现与临床试验患者分层[8](图3)。
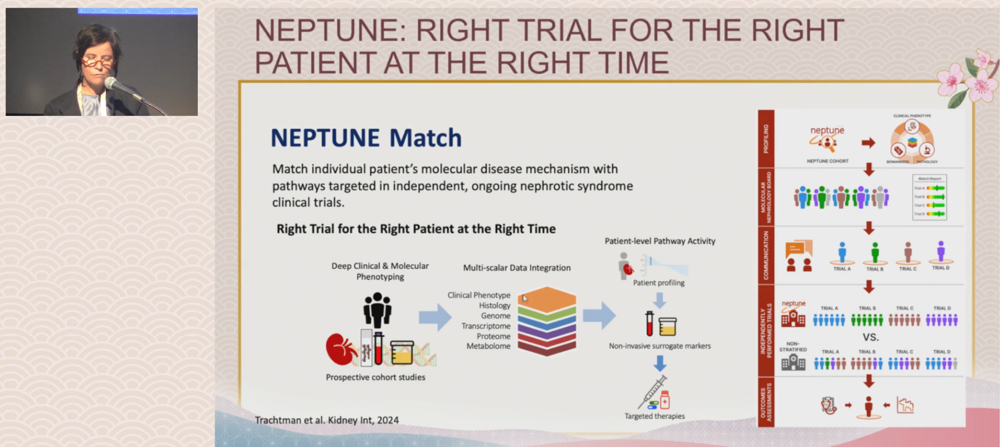
图3. NEPTUNE Match 平台:肾病综合征精准临床试验匹配体系
CureGN由美国国家糖尿病、消化和肾脏疾病研究所(NIDDK)资助,自2014年起在65个中心招募,覆盖MCD、FSGS、MN和IgA肾病四种疾病,旨在整合多维数据阐明病理通路、优化分型、诊断、预后与治疗。该队列积累了完整纵向表型数据,并参与PARASOL全球数据聚合计划(779例),以建立适用于全年龄段与疾病分期的通用替代终点[9]。
基于两大队列的多组学数据,团队实现了从“床边到bench”的靶点发现与转化。搭建NEPTUNE Match精准匹配平台,整合临床与分子表型实现患者与靶向临床试验的精准匹配,破解了既往全人群入组导致的临床试验失败难题[10]。此外,研究发现并验证了多个肾病关键靶点,足细胞特异性的APOM可通过调控脂质代谢发挥肾保护作用,是极具潜力的治疗靶点,同时基于队列锁定的ABCA1通路相关药物R3R01(NCT05267262)已进入II期临床试验。
三、足细胞导向的FSGS和DKD肾损伤进展机制
美国西奈山医学院John Cijiang He教授围绕足细胞在FSGS和糖尿病肾病(DKD)中的核心损伤角色展开报告。足细胞丢失广泛见于DKD和FSGS等肾小球疾病,足细胞密度降低是进展性DKD最强的独立预测因子,其丢失源于细胞脱落、死亡与去分化,且足细胞增殖再生能力极有限[11]。He教授指出,当前FSGS的治疗(糖皮质激素、免疫抑制剂)和DKD的治疗(RAS阻断剂、SGLT2抑制剂等)均无法直接靶向足细胞损伤,仍存在显著的残余风险,亟需开发足细胞特异性新疗法。
He教授重点介绍了其团队在视黄酸受体应答基因1(RARRES1)方面的创新研究。RARRES1是一种生长停滞基因,利用NEPTUNE队列数据对肾小球基因表达谱分析发现,50%的视黄酸相关基因在肾小球内差异表达,其中RARRES1在进展者与非进展者之间存在显著差异上调[12]。进一步研究证实,RARRES1表达与eGFR斜率呈正相关,且高表达者肾脏存活率显著低于低表达者[13]。RARRES1在足细胞中高度富集,DKD患者肾组织中RARRES1表达较对照组显著升高[14,15](图4)。
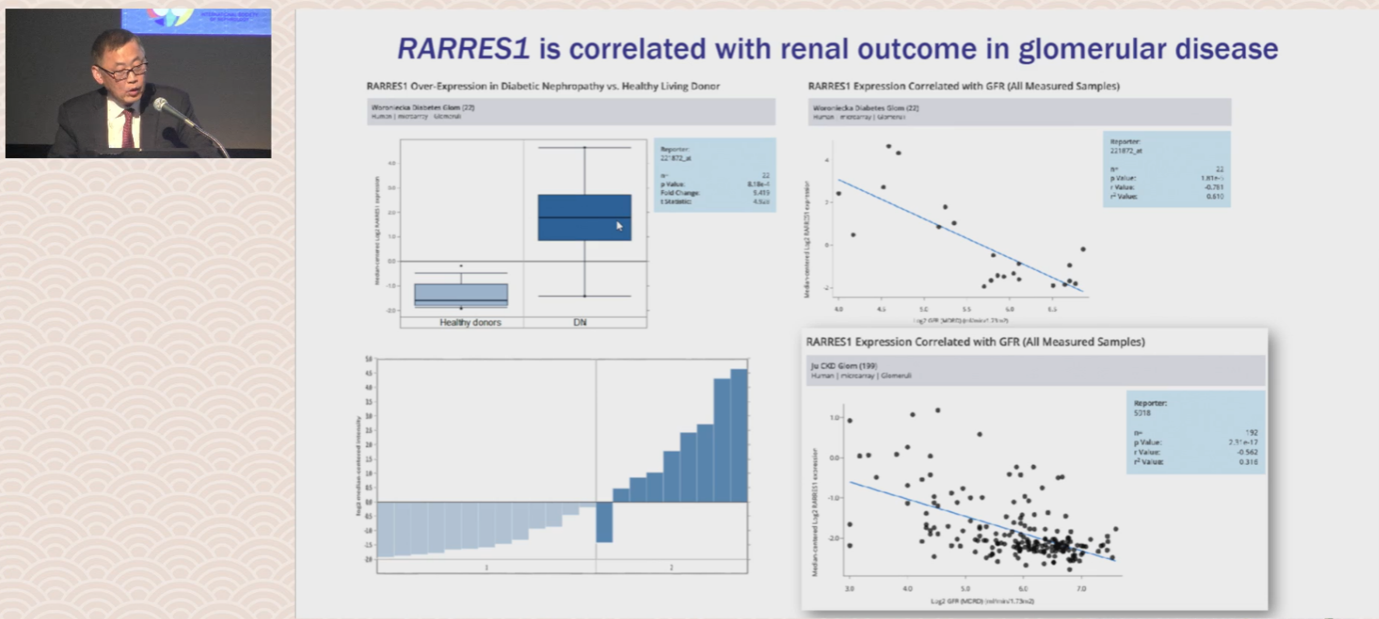
图4. 下调可溶性 RARRES1(sRARRES1)对阿霉素肾病模型足细胞损伤的保护作用
机制方面,RARRES1经MMP裂解产生的可溶性片段sRARRES1,通过激活p53促凋亡通路、抑制NOX-1促生存通路的双重机制驱动足细胞损伤,同时可介导足细胞-肾小管串话诱发小管脂毒性损伤,是肾病进展的核心致病因子。多种体内模型证实,下调sRARRES1可显著减轻足细胞损伤、蛋白尿与肾小球硬化,过表达野生型RARRES1则加重肾损伤[13,14]。
治疗转化方面,He教授团队筛选出调控RARRES1裂解的关键分子MMP23,其抑制剂可有效阻断RARRES1致病过程,减轻模型动物肾损伤。He教授总结,足细胞是FSGS与DKD的核心损伤靶细胞,RARRES1是极具潜力的新型治疗靶点,足细胞特异性药物递送系统的开发具有重要临床价值[15]。
总结
本次ISN-ISGD联合专场的三项重磅报告,从自身抗体介导的足细胞病内型分型、大队列驱动的精准靶点发现与转化、足细胞损伤核心机制与新型治疗靶点三个维度,全面展现了肾小球疾病诊疗从经验性治疗向机制驱动的精准医学的跨越式发展。未来,基于疾病内型的精准诊断分型、多中心大队列支撑的靶点验证、足细胞特异性的靶向治疗,将成为肾小球疾病诊疗的核心发展方向,为延缓肾病进展、改善患者长期预后提供关键支撑。
参考文献
[1] Romagnani P, et al. Nat Rev Dis Primers. 2025;11:87.
[2] Meyer-Schwesinger C, et al. Brenner & Rector's The Kidney. 2026.
[3] Hengel FE, et al. J Clin Invest. 2025;135 (5):e186769.
[4] Hengel FE, et al. N Engl J Med. 2024 Aug;391 (5):422-433.
[5] Hengel FE, et al. Kidney Int. 2025 Feb;107 (6):1099-1103.
[6] Hengel FE, et al. Kidney Int Rep. 2026 Jan;11 (4):103794.
[7] Hengel FE, et al. Kidney Int Rep. 2025;10 (8):2800-2804.
[8] NEPTUNE Study. https://www.neptune-study.org
[9] Courtesy of Laura Mariani and Zubin Modi.
[10] Trachtman H, et al. Kidney Int. 2024;105 (2):218-230.
[11] Yin L, et al. Front Cell Dev Biol. 2021 Nov;9:771931.
[12] Agrawal S, et al. Nat Rev Nephrol. 2021;17 (3):185-204.
[13] Chen A, et al. J Clin Invest. 2020;130 (10):5523-5535.
[14] Feng Y, et al. Kidney Int. 2024;106 (1):50-66.
[15] Meliambro K, et al. Nat Rev Nephrol. 2024;20 (10):643-658.
长期以来,肾小球疾病的诊疗面临“同病异治、异病同治”的经验性治疗局限,而足细胞作为肾小球疾病损伤的核心靶点,其相关机制与转化研究始终是领域的核心热点。2026年3月29日,世界肾脏病学大会(WCN 2026)大会上,国际肾脏病学会(ISN)与国际肾小球疾病学会(ISGD)联合专场带来了肾小球疾病诊疗的一系列颠覆性成果。全球顶尖肾病学者围绕原发性肾病综合征、足细胞病的发病机制、精准分型、生物标志物与靶向治疗进展展开深度分享。本文基于本场重磅学术报告,系统梳理前沿进展,为肾小球疾病的精准分型与靶向干预提供了重要学术参考。

一、原发性肾病综合征中靶向足细胞特异性抗原的自身抗体
来自德国汉堡大学医学中心的Tobias B. Huber教授首先描述了ISGD的愿景与使命,指出当前肾小球疾病的传统诊断长期依赖临床表现与描述性组织学特征,将微小病变(MCD)、局灶节段性肾小球硬化(FSGS)等归为独立疾病类型,但这种组织学分型无法揭示疾病的潜在病理生理机制,难以实现精准的个体化药物选择与通路靶向治疗[1]。Huber教授强调,肾小球疾病的分类应向内型(endotype)转变,即基于病因学的分类策略,涵盖自身免疫、遗传、适应性、感染性及药物/毒素相关等多种致病机制[2]。
随后,Huber教授重点阐述了抗nephrin自身抗体在MCD及特发性肾病综合征(INS)中的研究进展。Nephrin是足细胞裂孔隔膜的关键组成蛋白,早期研究已证实其缺失可导致先天性肾病综合征。抗nephrin自身抗体可与足细胞足突上的nephrin结合,导致裂孔隔膜磷酸化和内吞,引发白蛋白尿和足突融合,定义了一种新的疾病内型——抗nephrin足细胞病[3,4](图1)。

图1. MCD/INS的内型识别:抗Nephrin 介导足细胞病的致病机制
流行病学数据显示,抗nephrin自身抗体在多重耐药-激素耐药肾病综合征(MDR-SRNS)的MCD患者中阳性率极高,成人患者达70%,儿童患者更是高达90%,而在遗传性SRNS患者中阳性率极低,提示该抗体是特定肾病内型的核心致病因子[5]。抗nephrin自身抗体滴度与患者疾病活动度、蛋白尿水平显著相关,可有效预测患者对治疗的应答情况与FSGS复发风险。针对抗nephrin抗体灵敏度不足的问题,Huber教授团队开发了生物素-链霉亲和素增强ELISA、免疫沉淀-ELISA杂交检测体系[4](图2)。

图2. 抗Nephrin自身抗体的检测体系建立与临床应用验证
治疗层面,研究发现激素治疗可显著下调抗nephrin阳性患者的浆母细胞水平,而利妥昔单抗等B细胞清除治疗可有效降低抗体滴度并诱导疾病缓解[6]。值得注意的是,在FSGS肾移植复发队列(TANGO联盟)中也检测到抗nephrin抗体,提示该抗体可能预测移植后复发。Huber教授还介绍了无创诊断的初步探索:对于不能或不愿接受肾活检的患者,通过检测循环中抗nephrin抗体亚类即可辅助诊断并启动治疗[7]。
二、NEPTUNE与CureGN队列研究的最新进展
精准医学的核心是实现“机制与患者的精准匹配”,而高质量的临床队列与生物样本库是肾病靶点发现、药物研发与临床试验设计的核心基础。美国迈阿密大学米勒医学院Alessia Fornoni教授介绍了两大北美肾小球疾病队列研究——肾病综合征研究网络(NEPTUNE)和治愈肾小球肾炎(CureGN)项目的最新成果与转化应用。
NEPTUNE(肾病综合征研究网络)队列于2009年正式建立,覆盖北美32个临床招募中心,核心纳入FSGS、MCD、膜性肾病(MN)、Alport综合征等肾小球疾病患者,建立了超25.8万份生物样本库,整合临床随访、肾脏活检组学、全基因组测序等多维数据,核心用于精准分型、靶点发现与临床试验患者分层[8](图3)。

图3. NEPTUNE Match 平台:肾病综合征精准临床试验匹配体系
CureGN由美国国家糖尿病、消化和肾脏疾病研究所(NIDDK)资助,自2014年起在65个中心招募,覆盖MCD、FSGS、MN和IgA肾病四种疾病,旨在整合多维数据阐明病理通路、优化分型、诊断、预后与治疗。该队列积累了完整纵向表型数据,并参与PARASOL全球数据聚合计划(779例),以建立适用于全年龄段与疾病分期的通用替代终点[9]。
基于两大队列的多组学数据,团队实现了从“床边到bench”的靶点发现与转化。搭建NEPTUNE Match精准匹配平台,整合临床与分子表型实现患者与靶向临床试验的精准匹配,破解了既往全人群入组导致的临床试验失败难题[10]。此外,研究发现并验证了多个肾病关键靶点,足细胞特异性的APOM可通过调控脂质代谢发挥肾保护作用,是极具潜力的治疗靶点,同时基于队列锁定的ABCA1通路相关药物R3R01(NCT05267262)已进入II期临床试验。
三、足细胞导向的FSGS和DKD肾损伤进展机制
美国西奈山医学院John Cijiang He教授围绕足细胞在FSGS和糖尿病肾病(DKD)中的核心损伤角色展开报告。足细胞丢失广泛见于DKD和FSGS等肾小球疾病,足细胞密度降低是进展性DKD最强的独立预测因子,其丢失源于细胞脱落、死亡与去分化,且足细胞增殖再生能力极有限[11]。He教授指出,当前FSGS的治疗(糖皮质激素、免疫抑制剂)和DKD的治疗(RAS阻断剂、SGLT2抑制剂等)均无法直接靶向足细胞损伤,仍存在显著的残余风险,亟需开发足细胞特异性新疗法。
He教授重点介绍了其团队在视黄酸受体应答基因1(RARRES1)方面的创新研究。RARRES1是一种生长停滞基因,利用NEPTUNE队列数据对肾小球基因表达谱分析发现,50%的视黄酸相关基因在肾小球内差异表达,其中RARRES1在进展者与非进展者之间存在显著差异上调[12]。进一步研究证实,RARRES1表达与eGFR斜率呈正相关,且高表达者肾脏存活率显著低于低表达者[13]。RARRES1在足细胞中高度富集,DKD患者肾组织中RARRES1表达较对照组显著升高[14,15](图4)。

图4. 下调可溶性 RARRES1(sRARRES1)对阿霉素肾病模型足细胞损伤的保护作用
机制方面,RARRES1经MMP裂解产生的可溶性片段sRARRES1,通过激活p53促凋亡通路、抑制NOX-1促生存通路的双重机制驱动足细胞损伤,同时可介导足细胞-肾小管串话诱发小管脂毒性损伤,是肾病进展的核心致病因子。多种体内模型证实,下调sRARRES1可显著减轻足细胞损伤、蛋白尿与肾小球硬化,过表达野生型RARRES1则加重肾损伤[13,14]。
治疗转化方面,He教授团队筛选出调控RARRES1裂解的关键分子MMP23,其抑制剂可有效阻断RARRES1致病过程,减轻模型动物肾损伤。He教授总结,足细胞是FSGS与DKD的核心损伤靶细胞,RARRES1是极具潜力的新型治疗靶点,足细胞特异性药物递送系统的开发具有重要临床价值[15]。
总结
本次ISN-ISGD联合专场的三项重磅报告,从自身抗体介导的足细胞病内型分型、大队列驱动的精准靶点发现与转化、足细胞损伤核心机制与新型治疗靶点三个维度,全面展现了肾小球疾病诊疗从经验性治疗向机制驱动的精准医学的跨越式发展。未来,基于疾病内型的精准诊断分型、多中心大队列支撑的靶点验证、足细胞特异性的靶向治疗,将成为肾小球疾病诊疗的核心发展方向,为延缓肾病进展、改善患者长期预后提供关键支撑。
参考文献
[1] Romagnani P, et al. Nat Rev Dis Primers. 2025;11:87.
[2] Meyer-Schwesinger C, et al. Brenner & Rector's The Kidney. 2026.
[3] Hengel FE, et al. J Clin Invest. 2025;135 (5):e186769.
[4] Hengel FE, et al. N Engl J Med. 2024 Aug;391 (5):422-433.
[5] Hengel FE, et al. Kidney Int. 2025 Feb;107 (6):1099-1103.
[6] Hengel FE, et al. Kidney Int Rep. 2026 Jan;11 (4):103794.
[7] Hengel FE, et al. Kidney Int Rep. 2025;10 (8):2800-2804.
[8] NEPTUNE Study. https://www.neptune-study.org
[9] Courtesy of Laura Mariani and Zubin Modi.
[10] Trachtman H, et al. Kidney Int. 2024;105 (2):218-230.
[11] Yin L, et al. Front Cell Dev Biol. 2021 Nov;9:771931.
[12] Agrawal S, et al. Nat Rev Nephrol. 2021;17 (3):185-204.
[13] Chen A, et al. J Clin Invest. 2020;130 (10):5523-5535.
[14] Feng Y, et al. Kidney Int. 2024;106 (1):50-66.
[15] Meliambro K, et al. Nat Rev Nephrol. 2024;20 (10):643-658.
- 推荐文章
肾例明鉴 | 一场普通感冒后,她的肌酐飙升至583μmol/L!医生:警惕药物埋下的肾损伤陷阱
新月体性IgA肾病合并无肾小球基底膜线性免疫荧光的抗GBM肾炎:首例病例报道
当狼疮“突袭”肾与脑:多学科协作成功救治一例重症系统性红斑狼疮活动发作
肾域华章 | 真实世界研究REVEAL重磅发布:司维拉姆显著降低ND-CKD患者透析与心血管事件风险
2026 AACE年会公布重要研究:恩格列净相较于达格列净,可降低2型糖尿病患者心肾事件风险
FDA受理奥妥珠单抗治疗系统性红斑狼疮的补充生物制剂许可申请
重磅!瑞利珠单抗两月一针,治疗IgA肾病Ⅲ期I CAN研究中期分析圆满达标
一“比”了然:高血清IgA/C3比值意味着更差的蛋白尿控制
议通知 | 4月24—26日:2026年第二十五届北京肾脏病学术会议
联合用药亦稳定:非奈利酮持续降低2型糖尿病合并CKD患者尿白蛋白——FIVE‑STAR试验二次分析
狼疮肾炎临床缓解期无症状血清学复阳:预防性强化免疫抑制治疗还是观察等待?
限盐也能预防心衰?证据来了!
外周血与肾间质T细胞谱:狼疮肾炎治疗反应的关键预测指标
运动使死亡风险降低46%!82项RCT的荟萃分析证实体育锻炼对CKD的7大获益
初夏相约,共赴京华——北大医院肾脏病精准医学学术会议第一轮通知
超1.5亿人受累!中国30年慢性肾脏病负担特征与变迁给未来防控带来哪些启示
中国台湾IgA肾病患者经扁桃体切除联合激素冲击治疗实现尿学缓解一例
指南共识丨ERA提出急性肾损伤患者出院后管理的十大核心建议
意外发现:常见心脏标志物BNP,竟是糖尿病患者肾脏功能下降的“预警信号”
秉持以心肾结局为中心的治疗策略:一例蛋白尿明显好转但肾功能持续下降DKD患者的诊疗启示
肾域华章丨中山医院丁小强团队真实世界研究:泰它西普联合糖皮质激素治疗IgA肾病,降蛋白尿效果更优
里程碑式突破:FDA批准司帕生坦用于FSGS,开启非免疫抑制治疗新纪元
第十六届东方肾脏病学会议(OCN 2026)第一轮通知
IgA肾病治疗新抉择:同步联合还是序贯递进?
北大医院肾脏内科吕继成教授团队研究成果发表于JASN:揭示ERA与SGLT2抑制剂在IgA肾病中的独立降蛋白作用及联合治疗潜力
补水干预未能降低肾结石复发率,个体化预防已成行业新共识
精准靶向,迭代前行——KDIGO指南专家组解读IgA肾病补体抑制剂与B细胞调节剂的治疗定位
2026年第一季度国际肾脏病学领域进展回顾
【CKM精品课】张春教授:CKM管理的理念革新——从“治病”到“救人”的本质跨越
WCN 2026丨Brad Rovin教授:奥妥珠单抗提供肾小球疾病领域内首个可诱导肾脏组织学缓解并深度清除肾内B细胞的证据
【会议预告】北大医院肾脏病精准医学学术会议
全球首款IgA肾病基因疗法Sefaxersen 70mg:每月一次,PK/PD特征明确、无种族差异,全力推进Ⅲ期IMAGINATION研究丨WCN 2026
丁小强教授主持国际专题研讨会,聚焦AKI全球负担、创新治疗、康复策略丨WCN 2026
赵占正/张军军教授领衔国内多中心回顾研究证实:泽贝妥单抗治疗膜性肾病安全有效,6个月缓解率超六成丨WCN中国之声
突破传统认知,吕继成教授课题组联合国内多家中心发现IgA2亚型在IgA肾病中同样扮演关键致病角色
【CKM精品课】黄恺教授:破局“甜蜜危机”,中国居民糖代谢负担现状与精准分型
WCN中国之声丨浙大一院张萍教授:全球首创双靶点激动剂MT1013治疗SHPT Ⅱ期研究取得积极结果
WCN 2026丨ISN-ISGD联合会议聚焦足细胞损伤精准诊疗前沿进展:从自身抗体内型分型到全新靶点突破
高血压精准管理新动向:关注难治性高血压患者中皮质醇增多症的筛查丨ACC.26
WCN中国之声丨赵明辉教授:可伐利单抗可持续缓解PHN疲劳症状,患者接受度高达96%,aHUS Ⅲ期试验同步推进
WCN 2026丨菲泽妥单抗IGNAZ研究最新结果解读:IgA肾病精准靶向与免疫安全并进
WCN 2026丨CKD-MBD前沿进展:成人骨代谢新认知与儿童临床管理共识
WCN 2026重磅丨2026版KDIGO AKI/AKD指南更新核心要点全解
WCN 2026丨拨开肠-肾轴的迷雾,揭晓CKD与AKI的多器官串扰新机制
中美双队列研究:不合并ASCVD的CKD患者,他汀治疗降低死亡风险26%~39%
WCN 2026丨靶向肠道,直击源头——重塑IgA肾病治疗新理念直播峰会圆满举行
WCN中国之声丨王丽华教授:类风湿关节炎患者血清胱抑素C水平与亚临床肾功能损害及疾病活动度显著正相关
ACC 2026大咖视角 | 黄榕翀教授:ASCVD合并CKD患者临床管理的现状挑战与未来启示
WCN中国之声丨吕继成教授:HSK39297强效抑制AP活性近80%,显著降低IgA肾病蛋白尿约50%
WCN 2026丨临床突破接连落地,B细胞靶向治疗成肾小球疾病治疗核心赛道
每月1针,UPCR降幅可达62%!WCN 2026公布IgA肾病中国队列数据
WCN中国之声丨中山大学附属第三医院彭晖教授团队:AKI-CKD转归与EPS发病机制新突破
心血管代谢联盟——心-肾-代谢综合征(CKM)学术研讨会在武汉圆满落幕
WCN 2026丨Vlado Perkovic教授重磅公布APPLAUSE-IgAN研究最终分析结果,为补体抑制提供了首个长期肾功能保护证据
WCN中国之声丨陈会想教授:痛风患者血尿酸水平与CKD发病风险呈线性剂量反应关系
