- 首页 > 正文
FDA授予阿塞西普优先审评资格,IgA肾病治疗将迎来每周一次皮下注射的突破性新选择
发表时间:2026-03-13 16:08:15
作用机制
IgA肾病是一种严重的进行性自身免疫性肾脏疾病,其发病机制与异常自身抗体产生密切相关,目前针对疾病上游病因的改良疗法严重匮乏,存在极高的未满足医疗需求。临床数据显示,至少50%的IgA肾病患者会进展为终末期肾病或肾衰竭,给患者生活质量带来沉重打击,并伴随显著的疾病负担。阿塞西普作为一款研究性重组融合蛋白,通过特异性结合BAFF和APRIL这两种驱动B细胞存活及自身抗体产生的关键细胞因子,从源头上干预疾病进程,为患者带来全新治疗思路。
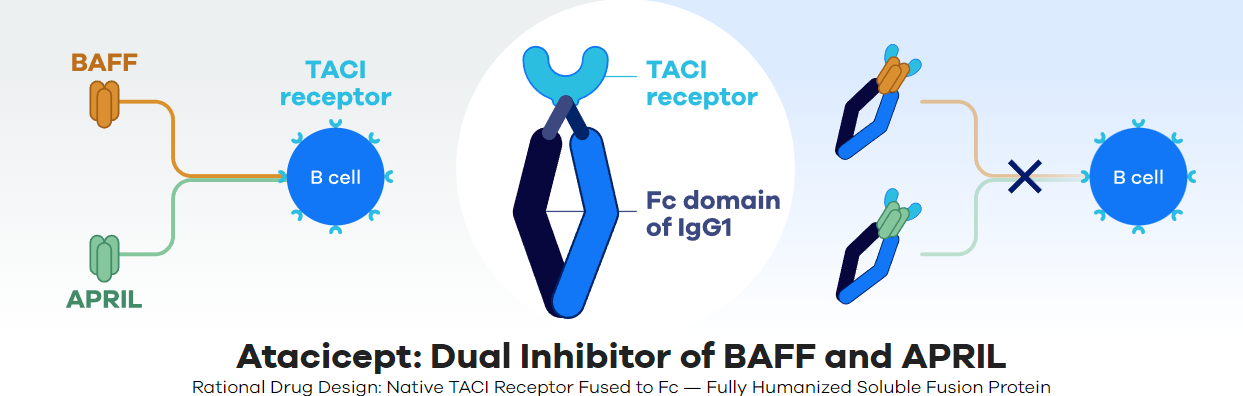
阿塞西普作用机制
关键研究数据
此次BLA申请的核心支持数据来自ORIGIN 3 Ⅲ期临床试验的预设中期分析结果。该试验是一项全球多中心、随机双盲、安慰剂对照研究,共纳入431例成人IgA肾病患者,按1:1比例随机分配至阿塞西普治疗组(150 mg每周一次皮下注射)和安慰剂对照组。结果显示,治疗36周时,阿塞西普组患者的24小时尿蛋白肌酐比(UPCR)较基线降低46%,相较于安慰剂组实现了具有统计学显著性和临床意义的42%降幅(P<0.0001),顺利达成主要疗效终点。同时,阿塞西普在整个ORIGIN临床试验项目中展现出良好的安全性,其安全特征与安慰剂相当。该中期分析结果已作为重磅口头报告在2025年美国肾脏病学会(ASN)的全体会议上公布,并于2025年11月6日发表于《新英格兰医学杂志》。目前,ORIGIN 3试验仍在以双盲安慰剂对照方式持续进行,旨在评估两年内患者的肾功能变化(以eGFR为指标),相关结果预计于2027年公布。
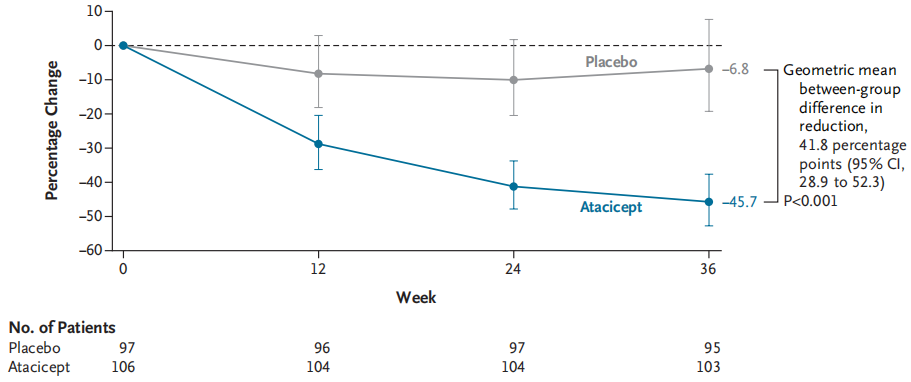
ORIGIN 3研究:UPCR随时间的变化
Vera Therapeutics创始人兼首席执行官Marshall Fordyce博士表示:“阿塞西普通过双重靶向BAFF和APRIL的独特机制,有望在获批后重塑IgA肾病的治疗标准。FDA授予的优先审评资格,凸显了该疾病领域对创新疗法的迫切需求。我们将持续与FDA紧密合作,推动BLA申请的全面审查,以患者急需的紧迫感,尽快将这一潜在疗法带给广大患者。”
值得关注的是,阿塞西普此前已获得FDA授予的突破性疗法认定,这一认定基于其ORIGIN 2b期临床试验的积极结果——该试验不仅达到主要和关键次要终点,显示出显著的蛋白尿降低效果和估算肾小球滤过率(eGFR)稳定作用,其96周长期数据还表明,药物在改善Gd-IgA1水平、血尿和蛋白尿方面持续获益,且eGFR稳定性与无IgA肾病的普通人群相当。(前沿进展|ORIGIN 2期研究结果重磅揭晓:阿塞西普长期治疗IgA肾病有效且安全)。
此外,Vera Therapeutics还通过ORIGIN Extend研究为受试者提供阿塞西普的扩展使用机会,同时收集长期安全性和有效性数据;在PIONEER试验中,该药物还在更多IgA肾病人群、抗PLA2R阳性原发性膜性肾病以及抗nephrin阳性局灶节段性肾小球硬化症(FSGS)和微小病变性肾病(MCD)患者中开展评估。
来源:https://www.globenewswire.com/news-release/2026/01/07/3214426/0/en/Vera-Therapeutics-Announces-U-S-FDA-Granted-Priority-Review-to-Biologics-License-Application-for-Atacicept-for-Treatment-of-Adults-with-IgA-Nephropathy.html
- 推荐文章
