- 首页 > 正文
认知障碍不仅提示脑损伤,还显著增加中年人群肾功能快速下降与新发CKD风险达61%、73%
发表时间:2026-03-13 16:25:19
慢性肾病(CKD)作为全球重大公共卫生问题,其发病机制复杂且危险因素多样。近年来,认知功能与肾脏健康的关联逐渐成为医学研究的热点领域。近期一项研究发现,在5761例基线无CKD的中年受试者中,认知障碍和痴呆与eGFR快速下降(每年≤-5 ml/min/1.73m2)显著相关;同时,认知障碍和痴呆患者新发CKD的风险也显著升高。该研究首次明确,在无基线肾病的中年人群中,早期认知障碍是肾功能快速下降和新发CKD的独立危险因素,为CKD的风险筛查和早期干预提供了新的思路。

肾脏功能随年龄增长呈现自然衰退趋势,正常人群每年eGFR下降约0.75ml/min/1.73m2,而超出预期的快速下降是CKD发生和进展的关键标志。认知障碍与肾脏疾病的关联研究此前多聚焦于CKD对认知功能的影响。晚期CKD和终末期肾病(ESKD)患者认知障碍发生率显著升高,且与不良健康结局相关,可能通过血管损伤、神经炎症、尿毒症毒素蓄积等机制介导。同时,已有研究表明肾功能快速下降与认知功能减退存在关联,即使在早期eGFR下降阶段,也可观察到认知功能异常。然而,这些研究多将CKD作为暴露因素、认知障碍作为结局指标,而关于认知障碍是否可预测中年人群肾脏功能下降的研究尚为缺乏。
认知障碍与心血管疾病、高血压等CKD危险因素存在明确关联,且孟德尔随机化研究提示认知功能与CKD风险可能存在因果关系。但现有研究多集中于65岁以上老年人群,此时神经退行性病变已普遍发生,难以明确认知障碍与肾脏功能下降的时序关系。中年人群作为CKD防控的关键群体,其认知功能与肾脏健康的关联尚未得到充分阐明。基于此,该研究提出假设:在无基线肾病的中年人群中,早期认知障碍与eGFR快速下降及新发CKD风险增加相关,并通过世界贸易中心(WTC)救援人员队列数据验证这一假设。
二、研究方法
研究纳入2015-2022年间至少有2次门诊血清肌酐(SCr)检测记录的受试者。排除基线存在CKD(eGFR<60 ml/min/1.73m2或有ICD-9/10CKD诊断编码)、有ESKD病史(肾移植或透析史)、随访期间死亡以及缺少2次及以上
主要结局指标包括:(1)eGFR年变化率,即基线与末次eGFR差值除以随访年限;(2)eGFR快速下降,定义为年度eGFR变化≤-5 ml/min/1.73m2。次要结局指标为新发CKD,定义为末次随访时eGFR<60 ml/min/1.73m2或出现CKD诊断编码。eGFR采用2021年种族无关的CKD流行病学协作组(CKD-EPI)公式计算。
三、研究结果
(一)受试者基线特征
纳入的5761名受试者平均年龄53.8岁,92%为男性,84%为非西班牙裔白人,基线平均eGFR为91.1 ml/min/1.73m2。其中,25%(1446人)存在基线认知障碍,2%(89人)为痴呆。与无认知障碍者相比,认知障碍患者年龄更大、非白人比例更高、教育程度更低,且糖尿病、抑郁症、创伤后应激障碍(PTSD)的患病率更高(P均<0.05)。随访期间,整体人群eGFR年均下降1.2 ml/min/1.73m2,10%(550人)出现eGFR快速下降,4%(248人)新发CKD。
(二)认知障碍与eGFR年度变化率的关联
单变量分析显示,认知障碍患者eGFR年均下降率(-1.5 ml/min/1.73m2)显著高于无认知障碍者(-1.1 ml/min/1.73m2,P=0.006);痴呆患者下降更为显著(-3.0 ml/min/1.73m2,P=0.002)。多变量线性回归分析校正所有混杂因素后,认知障碍(β=-0.34,95%CI:-0.58~-0.11,P=0.024)和痴呆(β=-1.51,95%CI:-2.36~-0.66,P=0.004)仍与eGFR更快下降显著相关(图1)。
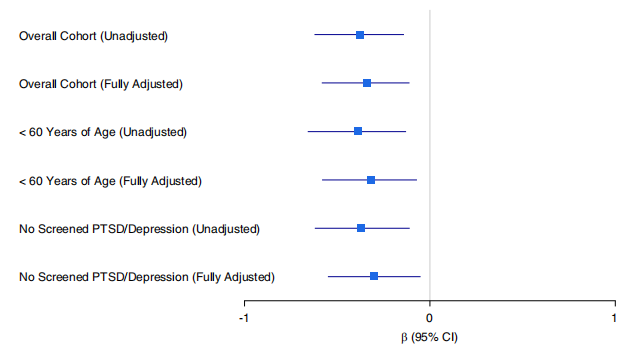
图1. 基线认知障碍与eGFR年变化的相关性
敏感性分析中,倾向评分匹配后,认知障碍患者eGFR年均下降率仍显著高于无认知障碍者(-1.9 vs. -1.1 ml/min/1.73m2,P=0.009);排除60岁以上人群、排除PTSD/抑郁症患者后,认知障碍与eGFR快速下降的关联依然存在(P均<0.05)。
(三)认知障碍与eGFR快速下降的关联
认知障碍患者eGFR快速下降发生率(13%)显著高于无认知障碍者(8%,P<0.001,图2),痴呆患者发生率高达25%(vs. 无痴呆者9%,P<0.001,图3)。多变量Cox回归分析显示,校正所有混杂因素后,认知障碍(aHR=1.61,95%CI:1.32~1.96,P<0.001)和痴呆(aHR=2.40,95%CI:1.46~3.94,P=0.004)与eGFR快速下降风险显著增加相关。
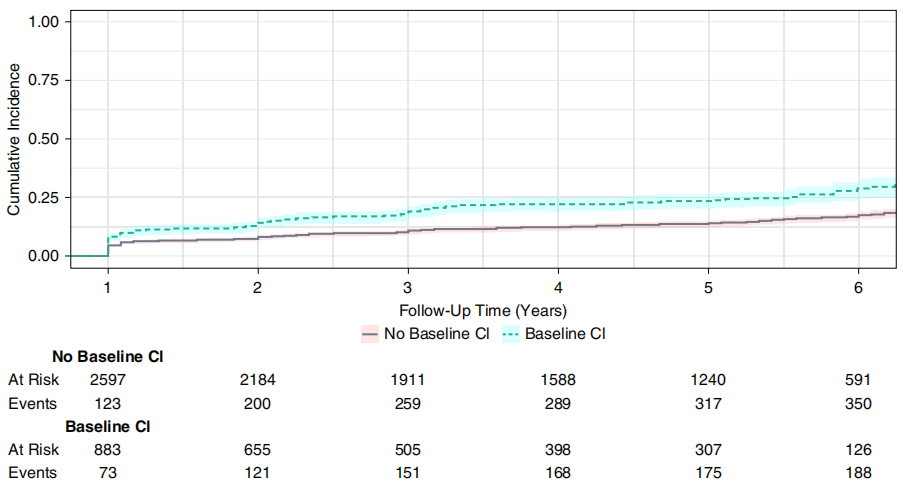
图2. 基线认知障碍或无认知障碍患者eGFR快速下降的发生率
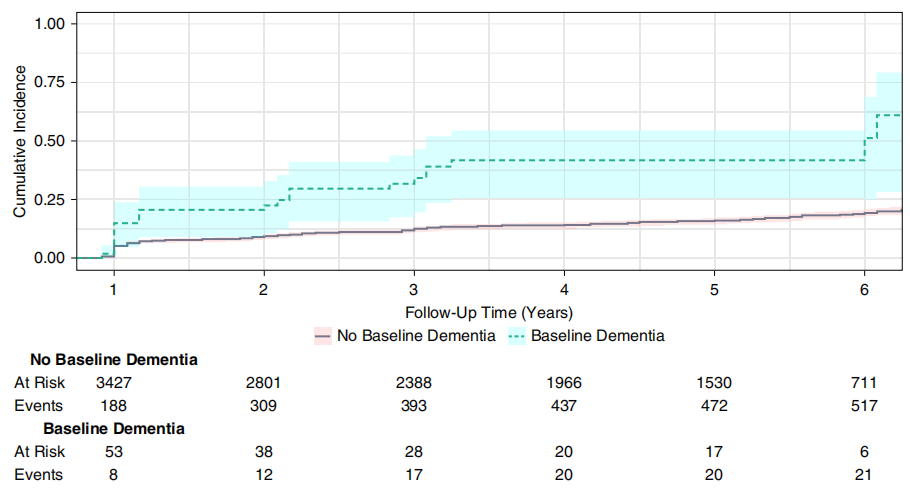
图3. 基线痴呆或无痴呆患者eGFR快速下降的发生率
敏感性分析验证了上述结果的稳健性:倾向评分匹配后,认知障碍患者eGFR快速下降风险仍显著升高(12% vs. 9%,P=0.003);排除60岁以上人群后,认知障碍和痴呆与eGFR快速下降的关联仍具有统计学意义(aHR分别为1.55和2.50,P均<0.05);排除PTSD/抑郁症患者后,上述关联依然存在(aHR分别为1.56和2.68,P均<0.01)。
(四)认知障碍与新发CKD的关联
认知障碍患者新发CKD发生率(6%)显著高于无认知障碍者(4%,P=0.005),痴呆患者发生率为10%(vs. 无痴呆者4%,P=0.007)。多变量Cox回归分析显示,校正混杂因素后,认知障碍(aHR=1.73,95%CI:1.29~2.31,P=0.002)和痴呆(aHR=2.80,95%CI:1.29~6.09,P=0.038)与新发CKD风险显著相关。仅采用eGFR定义新发CKD时,认知障碍的关联仍显著(aHR=1.76,95%CI:1.29~2.40,P=0.003)(图4)。
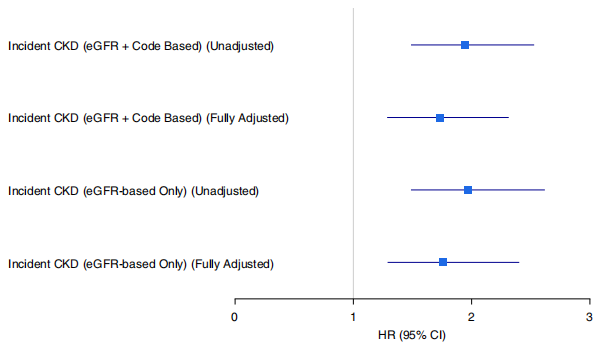
图4. 基线认知障碍显著增加新发CKD风险
此外,轻度认知障碍(MoCA 19~23分)也与eGFR快速下降、新发CKD风险增加显著相关;认知障碍与eGFR快速下降+新发CKD的复合结局风险升高相关(aHR=2.56,95%CI:1.66~3.99,P<0.001)。排除随访期间死亡或基线有卒中/脑外伤/心血管疾病的患者后,上述关联均未发生显著改变。
四、讨论和总结
该研究基于大规模前瞻性队列,首次系统证实了在无基线肾病的中年人群中,早期认知障碍是肾功能快速下降和新发CKD的独立危险因素,且这一关联不受年龄、合并症、精神心理疾病等混杂因素影响。研究结果具有重要的临床意义和公共卫生价值,为CKD的风险分层和早期干预提供了新的生物学标志物。
认知障碍与肾脏功能下降之间的关联可能通过多种机制介导。首先,系统性炎症可能是共同的病理基础。神经炎症是认知障碍(尤其是阿尔茨海默病)的核心病理特征,而炎症同样在CKD的发生发展中发挥关键作用。NLRP3炎症小体作为炎症反应的关键调控因子,已被证实参与阿尔茨海默病和CKD的发病机制,可能是连接两者的重要分子通路。其次,血管功能异常可能协同损伤脑和肾脏。脑和肾脏均为高灌注器官,微血管病变在两者的病理过程中均占据重要地位,内皮功能障碍既与神经退行性疾病相关,也是CKD进展的重要驱动因素。此外,认知障碍患者可能存在“系统性衰老表型”,即多个器官(包括脑和肾脏)的生理衰老进程同步加速,表现为认知功能与肾脏功能平行下降。
认知障碍还可能通过间接途径影响肾脏健康。认知功能受损可能导致健康素养下降,进而影响患者对高血压、糖尿病等危险因素的管理,增加肾脏损伤风险。同时,认知障碍与糖尿病、高血压、心血管疾病等CKD危险因素高度共病,尽管该研究已校正这些因素,但其潜在的交互作用仍可能部分解释观察到的关联。
该研究结果提示,认知障碍应被纳入中年人群CKD风险评估体系。对于存在认知障碍的中年个体,即使肾功能正常,也应加强肾脏功能监测,定期检测eGFR和尿蛋白,同时积极控制糖尿病、高血压等合并症,以延缓肾脏功能下降。此外,临床医生在评估认知障碍患者时,应常规进行肾脏功能筛查,实现脑肾疾病的协同管理。
参考文献:Bano R, et al. Kidney360. 2025; 6: 2130-2144.
- 推荐文章
