- 首页 > 正文
1型原发性高草酸尿症(PH1)首个RNA疗法Lumasiran的5年临床疗效与安全性研究——ILLUMINATE-A Ⅲ期临床试验最终结果分析
发表时间:2026-03-13 16:29:10
1型原发性高草酸尿症(PH1)是一种罕见的常染色体隐性遗传疾病,其核心病理特征为肝脏草酸过量生成,进而引发肾结石、肾钙质沉着,并最终导致进行性肾功能衰退。Lumasiran作为首个美国食品药品监督管理局(FDA)获批用于治疗PH1的RNA干扰(RNAi)疗法,为该疾病的治疗带来了革命性突破。本文基于ILLUMINATE-A Ⅲ期临床试验的60个月最终数据,系统分析Lumasiran在PH1患者中的长期疗效、安全性及临床应用价值。研究结果显示,Lumasiran治疗可使患者24小时尿草酸(UOx)排泄量和血浆草酸(POx)浓度实现持续显著降低,有效维持估算肾小球滤过率(eGFR)稳定,降低肾结石事件发生率,改善肾髓质钙质沉着程度,并展现出良好的安全性和耐受性。
一、研究背景
PH1是由编码丙氨酸:乙醛酸氨基转移酶(AGXT)的基因突变引起的罕见遗传性疾病,全球发病率约为1/100000至1/200000。其病理机制为AGXT酶活性缺陷导致肝脏乙醛酸代谢异常,草酸大量生成并在体内蓄积。草酸与钙结合形成不溶性的草酸钙结晶,沉积于肾脏、视网膜、骨骼、心脏等多个器官,其中肾脏是最主要的受累器官。患者早期常表现为复发性肾结石、肾髓质钙质沉着,随着病情进展,肾功能逐渐恶化,最终可能发展为终末期肾病(ESKD)和全身性草酸沉着症,严重影响患者生活质量并缩短生存期。
在Lumasiran获批之前,PH1的治疗手段极为有限,主要依赖于大量饮水、结晶抑制剂、吡哆醇补充等支持性治疗,对于进展期患者,仅能依靠透析或肝肾联合移植维持生命,但这些治疗方式存在疗效有限、并发症多、医疗负担重等诸多问题。RNAi技术的出现为PH1的靶向治疗提供了新的思路,Lumasiran作为针对PH1的首个RNAi疗法,通过特异性降解编码乙醇酸氧化酶的mRNA,抑制肝脏草酸生成的关键通路,从源头上减少草酸蓄积。
ILLUMINATE-A试验作为Lumasiran关键的Ⅲ期临床试验,采用多中心、随机、双盲、安慰剂对照设计,后续延伸期为所有患者提供Lumasiran治疗,旨在全面评估该药物的长期疗效和安全性。此前公布的36个月中期分析数据已初步证实Lumasiran的短期疗效和安全性,而本次60个月的最终结果为该药物的长期临床应用提供了更全面、更可靠的证据,对于指导PH1的临床治疗具有重要意义。
二、研究方法
(一)研究设计与研究人群
ILLUMINATE-A是一项为期60个月的多中心Ⅲ期临床试验,研究周期从2019年1月(入组开始)至2024年1月,在欧洲、中东、北美等地区的16个研究中心开展。研究设计分为两个阶段:第一阶段为6个月的双盲、安慰剂对照期,患者按随机分配接受Lumasiran或安慰剂治疗;第二阶段为54个月的开放标签延伸期,所有患者均接受Lumasiran治疗。
研究纳入标准为:年龄≥6岁;经基因检测确诊为PH1(AGXT基因突变);估算肾小球滤过率(eGFR)≥30 ml/min/1.73m2;前两次有效24小时尿标本检测显示平均24小时尿草酸排泄量(UOx)≥0.70 mmol/24h/1.73m2。对于正在服用吡哆醇治疗的患者,要求在随机化前保持稳定用药方案≥90天,并同意在首次用药后继续维持该方案12个月。
(二)治疗方案
Lumasiran的给药方案为:负荷剂量3 mg/kg,每月1次,连续3次;之后进入维持治疗阶段,每3个月给药1次,剂量同负荷剂量。安慰剂组在双盲期接受与Lumasiran外观一致的安慰剂注射,延伸期切换为上述Lumasiran治疗方案。
(三)结局指标与评估方法
主要疗效指标为双盲期基线至第6个月24小时尿草酸排泄量(校正体表面积)的百分比变化。次要疗效指标包括延伸期24小时尿草酸排泄量的百分比及绝对变化、血浆草酸浓度的变化、eGFR的变化等。探索性疗效指标包括随机尿草酸/肌酐比值(UOx:Cr)、血浆乙醇酸浓度、肾结石事件发生率、肾髓质钙质沉着分级变化及健康相关生活质量(HRQOL)评分。
安全性指标:包括不良事件(AEs)的发生率、严重程度、与研究药物的相关性;抗药物抗体(ADAs)检测;实验室检查异常等。三、研究结果
(一)研究人群与基线特征
研究共纳入39例PH1患者,其中双盲期随机分配至Lumasiran组(Lumasiran/Lumasiran组)26例,安慰剂组(安慰剂/Lumasiran组)13例。最终24例(92.3%)Lumasiran/Lumasiran组患者和13例(100%)安慰剂/Lumasiran组患者完成了60个月的研究。两组患者基线特征均衡。
(二)疗效结果
尿草酸与血浆草酸水平变化:长期Lumasiran治疗使两组患者的24小时尿草酸排泄量实现持续显著降低。至研究第60个月,Lumasiran/Lumasiran组和安慰剂/Lumasiran组患者的24小时尿草酸排泄量较基线分别平均降低54%和54%(图1A)。两组患者基线24小时尿草酸排泄量分别为1.84 mmol/24h/1.73m2和1.79 mmol/24h/1.73m2,第60个月时分别降至0.75 mmol/24h/1.73m2和0.71 mmol/24h/1.73m2(图1B)。在Lumasiran治疗2-3个月后,两组患者的24小时尿草酸排泄量基本维持在正常上限(ULN:0.514 mmol/24h/1.73m2)至1.5倍正常上限(0.771 mmol/24h/1.73m2)之间。随机尿草酸/肌酐比值(UOx:Cr)也呈现类似的持续降低趋势。
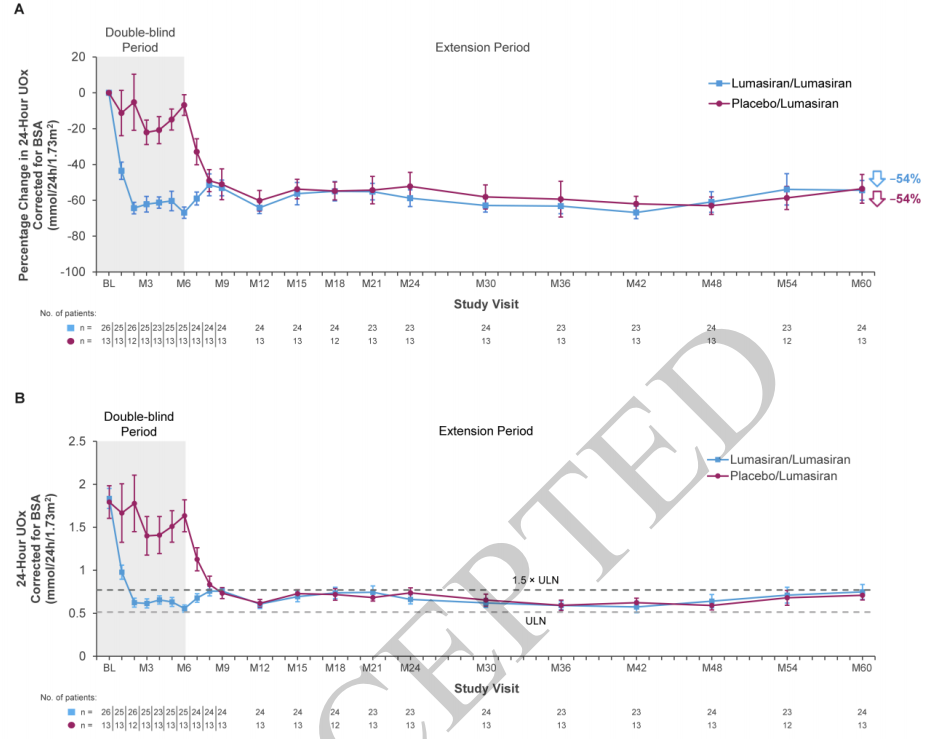
图1. 24小时尿草酸排泄量随时间的变化
血浆草酸浓度同样显著降低。第60个月时,Lumasiran/Lumasiran组和安慰剂/Lumasiran组患者的血浆草酸浓度较基线分别平均降低35%和38%。两组患者基线血浆草酸浓度分别为15.7 μmol/L和17.8 μmol/L,第60个月时分别降至9.8 μmol/L和10.0 μmol/L,且在延伸期内基本维持在正常范围(ULN:12.11 μmol/L)内(图2)。此外,两组患者的血浆乙醇酸浓度在Lumasiran治疗前6个月升高,之后趋于平稳并维持稳定。
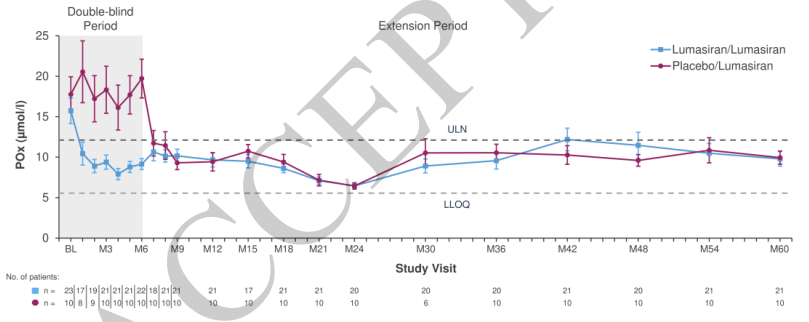
图2. 血浆草酸浓度随时间的变化
肾功能保护效果:Lumasiran/Lumasiran组患者从基线至第60个月的eGFR平均绝对变化为-3.40 ml/min/1.73m2,安慰剂/Lumasiran组为-8.11 ml/min/1.73m2(图3)。所有39例患者在Lumasiran治疗期间的eGFR年下降率仅为-0.6 ml/min/1.73m2,远低于历史数据中PH1患者的预期下降速度(基线慢性肾脏病2、3a、3b期患者的年eGFR下降率分别为-2.3、-5.3和-14.7 ml/min/1.73m2)。个体患者的eGFR变化曲线显示,即使是基线eGFR较低的患者,其肾功能在长期治疗中也未出现明显恶化。
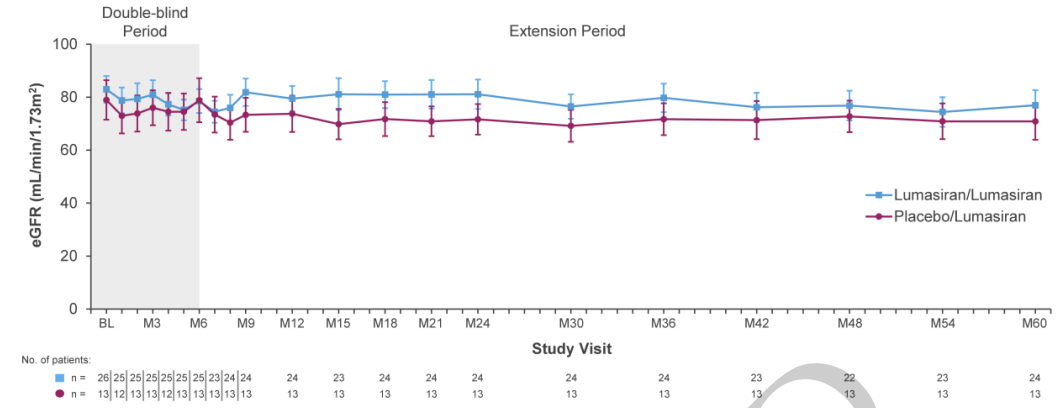
图3. eGFR随时间的变化
肾结石事件与肾髓质钙质沉着改善:研究期间,Lumasiran/Lumasiran组的肾结石事件发生率为0.47(95%CI:0.36-0.62)次/患者-年,安慰剂/Lumasiran组为0.54(95%CI:0.37-0.78)次/患者-年。总体而言,54%的患者在研究期间未发生任何肾结石事件,18%的患者发生1次,28%的患者发生1次以上。安慰剂/Lumasiran组的较高发生率主要由1例基线结石负荷较重的患者所致,其余患者的结石事件较为罕见。
肾髓质钙质沉着改善显著:基线时37例患者接受了肾脏超声检查,其中28例存在肾髓质钙质沉着。至研究结束时,28例基线存在肾髓质钙质沉着的患者中,21例(75%)的钙质沉着分级得到改善,16例(57%)完全缓解(分级降至0级)。随着治疗时间的延长,达到0级肾髓质钙质沉着的患者比例逐渐增加。对于基线无肾髓质钙质沉着的患者,治疗期间未出现明显的钙质沉着进展。
健康相关生活质量:两组患者在治疗期间的健康相关生活质量保持稳定或有所改善。Lumasiran/Lumasiran组患者第60个月的EQ-5D视觉模拟量表(VAS)评分较基线平均变化为1.8,安慰剂/Lumasiran组为-4.3。成人和儿童患者的EQ-5D VAS评分、EQ-5D-5L指数均维持稳定。此外,Lumasiran/Lumasiran组患者在KDQOL问卷的症状/问题、肾脏疾病影响、肾脏疾病负担等维度的评分均较基线有所提高,儿童患者的PedsQL总评分较基线平均提高9.39(SD18.60),提示患者的生活质量得到改善。
(三)安全性结果
两组不良反应发生率相当,大多数是轻重度。最常见的不良事件(发生率≥15%)为注射部位反应(36%)、腹痛(23%)、新型冠状病毒感染(21%)、头痛(18%)和鼻咽炎(15%)。其中,注射部位反应均为暂时性、轻度,且无需特殊处理即可缓解,与此前2期临床试验结果一致。所有39例患者的基线抗药物抗体检测均为阴性。研究期间未发现新的安全性信号。
四、讨论与总结
ILLUMINATE-A Ⅲ期临床试验的60个月最终结果为Lumasiran治疗PH1的长期疗效和安全性提供了强有力的证据。作为首个针对PH1的RNAi疗法,Lumasiran通过特异性抑制肝脏草酸生成的关键酶,实现了尿草酸和血浆草酸水平的持续显著降低,这一核心疗效指标在长达5年的治疗中保持稳定,证实了该药物作用机制的有效性和持久性。
肾功能保护是PH1治疗的核心目标,该研究结果显示Lumasiran治疗能有效维持PH1患者的eGFR稳定,年下降率仅为-0.6 ml/min/1.73m2,远低于历史数据中PH1患者的自然病程进展速度。这一结果具有重要的临床意义,意味着Lumasiran可能延缓甚至阻断PH1患者的肾功能衰退进程,减少终末期肾病的发生风险,从而显著改善患者的长期预后。此外,Lumasiran治疗还显著降低了肾结石事件发生率,改善了肾髓质钙质沉着程度,这些均是PH1患者肾功能恶化的重要危险因素,其改善进一步佐证了Lumasiran对肾脏的保护作用。
健康相关生活质量的改善是评估慢性疾病治疗效果的重要维度。PH1患者由于反复的肾结石发作、肾功能不全及长期治疗负担,其生活质量通常较低。该研究中,患者的EQ-5D系列评分、KDQOL评分及PedsQL评分均维持稳定或有所改善,这进一步凸显了Lumasiran在改善患者整体健康状况方面的价值。
安全性方面,Lumasiran在60个月的治疗中展现出良好的耐受性。最常见的不良事件为轻度注射部位反应,严重不良事件发生率低且与药物无关,无新的安全性信号出现。
总体而言,ILLUMINATE-A Ⅲ期临床试验的60个月最终结果表明,Lumasiran治疗1型原发性高草酸尿症(PH1)具有显著且持久的疗效,能够持续降低患者尿草酸和血浆草酸水平,有效维持肾功能稳定,减少肾结石事件发生,改善肾髓质钙质沉着,并提高患者的健康相关生活质量。同时,Lumasiran在长期治疗中展现出良好的安全性和耐受性,无新的安全性信号出现。这些结果进一步巩固了Lumasiran作为PH1标准治疗方案的地位,为PH1患者的长期疾病管理提供了可靠的治疗选择。
参考文献:Frishberg Y, et al. Clin J Am Soc Nephrol . 2025 Dec 4. doi: 10.2215/CJN.0000000916. Online ahead of print.
- 推荐文章
