- 首页 > 正文
北大医院赵明辉/崔昭团队专题综述:Hippo通路——新月体肾小球肾炎免疫治疗的潜在靶点
发表时间:2026-03-15 10:06:46
新月体肾小球肾炎(cGN)是一种以病理上广泛的新月体形成为特征的快速进展性肾小球损伤,通常导致终末期肾病。根据发病机制和免疫荧光模式,主要分为抗肾小球基底膜病、抗中性粒细胞胞质抗体相关性血管炎和免疫复合物介导的cGN三类。尽管病因各异,但最终均导致以增生性壁层上皮细胞为主构成的新月体。
解剖学上,新月体位于足细胞相关的滤过屏障与静止的壁层上皮细胞构成的鲍曼囊之间。足细胞与壁层上皮细胞具有共同发育起源,空间邻近,提示两者间的“对话”可能是cGN发病的共同下游机制。Turinsky等人的研究证实,足细胞特异性Hippo-YAP信号通过与壁层上皮细胞的交互作用,在cGN发病中扮演关键角色。
一、Hippo通路的核心信号机制
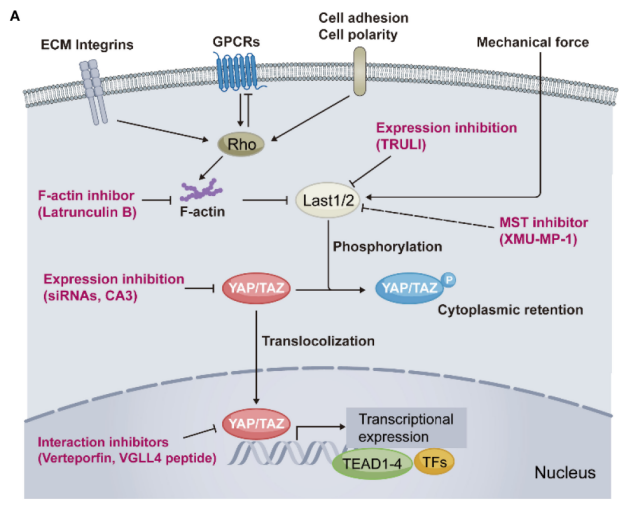
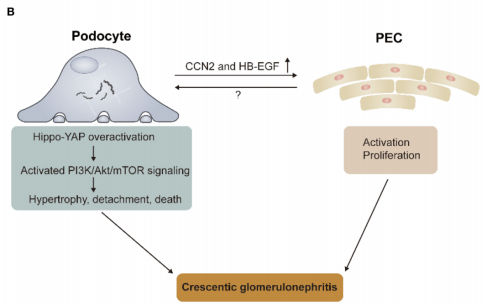
图1. Hippo通路中的核心信号及Hippo-YAP过度活化在新月体肾小球肾炎发病机制中的作用(图A:Hippo通路整合多种上游信号以调控YAP/TAZ活性;图B:关于YAP过度激活如何将足细胞损伤与其与部分上皮细胞(PECs)的交叉对话联系起来并导致新月体肾小球肾炎的关键发现示意图)
二、Hippo通路在肾脏生理与病理中的作用
在哺乳动物中,Hippo通路参与胚胎肾脏发育、肾纤维化过程以及足细胞稳态的维持。与位于肾小球外围鲍曼囊的静止壁层上皮细胞不同,足细胞位于肾小球毛细血管袢,持续承受生理性滤过机械力,因而更易在损伤时受到Hippo通路的调控。研究证实,足细胞上调控YAP/TAZ活性的整合素α3β1和αvβ5对维持其正常功能至关重要,表明由细胞黏附驱动的Hippo-YAP信号激活参与足细胞损伤。此外,在糖尿病肾病中,足细胞YAP磷酸化通过降低转录因子WT1及其调控蛋白(如nephrin、podocalyxin)的表达参与发病;而肾小管上皮细胞YAP激活则参与间质纤维化。
三、Hippo-YAP通路过度激活在cGN中的作用及机制
Turinsky等学者通过一系列体内外实验,首次揭示了足细胞特异性Hippo-YAP通路过度激活在cGN发病中的关键作用,其核心研究结果如下:
(一)cGN模型中足细胞特异性YAP激活的证实
研究团队首先利用肾毒性血清(NTS)诱导的小鼠肾炎模型(经典实验性cGN模型,广泛用于探索cGN的免疫发病机制),证实了cGN中足细胞特异性YAP激活:与对照组相比,NTS处理后的小鼠足细胞中核定位YAP表达显著增加,其下游靶基因(如CCN1、CCN2)的表达水平也明显上调。时间序列分析显示,这些基因表达变化早于新月体病变的出现,提示足细胞Hippo-YAP信号过度激活可能参与新月体形成的起始过程。
(二)足细胞特异性YAP激活介导cGN发病的直接证据
为明确足细胞YAP激活与cGN发病的因果关系,研究者构建了足细胞特异性YAP持续激活的小鼠模型(P-YAP5SA小鼠)——通过突变足细胞中YAP的所有磷酸化位点,使YAP持续滞留于细胞核内并保持活性。令人意外的是,未接受NTS处理的P-YAP5SA小鼠随时间推移出现快速进展的肾脏表型,其特征与人类cGN高度相似:①蛋白尿进行性加重;②因肾功能快速丧失导致累积死亡;③肾小球内大量细胞性新月体形成及炎症细胞浸润。
由于P-YAP5SA小鼠病情进展迅速,难以捕捉精确的病理生理变化,研究者进一步构建了诱导型足细胞YAP激活小鼠模型(Pi-YAP5SA小鼠),其表型严重程度与足细胞YAP激活程度相关,病情相对缓和。利用该模型,研究团队发现了两个时间依赖性病理事件:早期毛细血管外细胞肥大和晚期细胞增生。深入机制研究表明:①足细胞肥大及细胞自主性丢失是YAP过度激活后的初始应答;②活化PECs的增殖是足细胞特异性YAP过度激活引发的非细胞自主性应答,二者共同推动新月体形成。(三)YAP过度激活介导cGN的分子机制
为解析上述病理过程的分子机制,研究者在条件永生化分化的人类足细胞中构建了诱导型YAP激活模型(YAP5SA足细胞),并结合RNA测序及生物信息学分析,发现YAP5SA足细胞在生物学及分子水平的多项改变可解释Pi-YAP5SA小鼠的病理表型:①发育程序重新激活导致细胞骨架与极性重构,对应Pi-YAP5SA小鼠足细胞足突融合损伤及细胞丢失;②肾小球基底膜(GBM)相关ECM基因(Col4a3、Col4a4、Lama4、Nid2等)表达上调,对应小鼠模型中GBM增厚现象。此外,研究证实磷脂酰肌醇3激酶-蛋白激酶B-雷帕霉素靶蛋白(PI3K/Akt/mTOR)通路激活是Hippo-YAP过度激活后的关键下游机制,介导足细胞损伤。
值得注意的是,模型中观察到的足细胞丢失后PECs非自主性增殖提示二者存在交叉对话。进一步研究发现,分泌型分子CCN2和肝素结合表皮生长因子样生长因子(HB-EGF)可能是介导这一交叉对话的关键分子,上述“干实验”结果均通过YAP5SA足细胞及Pi-YAP5SA小鼠模型的“湿实验”得到验证。
(四)临床样本验证与同期研究支持
为明确研究结果的临床转化价值,研究者检测了cGN患者(包括抗GBM病、狼疮性肾炎及ANCA相关血管炎)的肾组织样本,发现这些患者足细胞中YAP及其下游靶基因CCN2的表达水平显著高于非新月体性肾小球肾炎患者,与实验动物模型的结果一致,证实Hippo-YAP通路过度激活在人类cGN中普遍存在。
有趣的是,在同一期Science Translational Medicine中,He等学者发表的同期研究也证实,足细胞特异性YAP/TAZ过度激活及其上游LATS1/2缺陷,可促进塌陷性肾小球病(以足细胞损伤和PECs增殖为特征)及ANCA相关血管炎的发病,进一步支持了Hippo-YAP通路在cGN中的关键作用。
四、结论与未来展望
cGN作为最严重的肾小球疾病类型,预后极差,尽管采用积极的非特异性免疫抑制治疗,多数患者仍难以避免进展至终末期肾病。其根本原因在于对发病机制的理解不足,导致缺乏针对性的治疗手段。Turinsky等与He等学者的研究共同揭示了Hippo通路介导的足细胞损伤通过与PECs交叉对话,最终导致cGN新月体病变的新型发病机制(图1B),不仅拓展了我们对Hippo-YAP信号在足细胞功能调控中作用的认识,更为cGN的治疗提供了全新的潜在靶点。
尤为重要的是,Hippo通路过度激活在所有类型cGN中均存在,提示其可能是cGN发病的共同下游效应机制。这意味着,针对Hippo通路的靶向治疗有望突破现有治疗依赖病因分类的局限,像补体抑制治疗一样,为不同病因的cGN患者提供统一的治疗策略。未来,亟需开展针对Hippo通路的药理学抑制临床前研究,例如小分子药物维替泊芬(verteporfin)通过抑制YAP-TEAD相互作用发挥作用的有效性验证,以明确其转化应用价值。
同时,该研究也提出了多个值得进一步探索的科学问题:①静息状态的PECs在cGN中虽未显示YAP/TAZ过度激活(可能与远离免疫损伤中心有关),但在其增殖活化过程中,是否存在Hippo通路过度激活以进一步加重新月体病变?②除了介导足细胞损伤的PI3K/Akt/mTOR通路及介导足细胞-PECs交叉对话的CCN2、HB-EGF外,YAP过度激活后是否存在其他未知通路参与cGN的关键病理过程?③研究者在YAP5SA足细胞中观察到补体级联反应激活,而此前研究表明Hippo通路可受补体受体C3ar1(参与足细胞损伤)等GPCRs调控,因此补体激活是否作为cGN的另一下游效应机制,与YAP/TAZ过度激活相互作用参与疾病发病?这些问题的解答将为cGN的机制研究与治疗策略优化提供更深入的理论支持。
来源:Front Immunol. 2025 Sep 11:16:1672128. doi: 10.3389/fimmu.2025.1672128. eCollection 2025.
- 推荐文章
