- 首页 > 正文
JASN:Farabursen通过抑制miR-17恢复多囊蛋白表达,显著延缓ADPKD患者肾脏体积增长
发表时间:2026-01-28 11:20:24
引言:常染色体显性多囊肾病(ADPKD)是最常见的遗传性肾病,全球发病率约1/1000,由PKD1或PKD2基因杂合失活突变引起,导致肾小管上皮细胞过度增殖、囊腔形成,最终进展为终末期肾病。目前临床唯一获批的特异性治疗药物托伐普坦(Tolvaptan)仅通过选择性拮抗血管加压素V2受体(AVPR2),从而抑制囊腔内液体分泌、降低囊肿内压和减缓囊肿体积扩张,延缓病程,且肝毒性限制了其广泛应用。因此,开发靶向疾病根源的新型药物仍是亟待满足的临床需求。
一、研究背景与机制
微小RNA-17(miR-17)家族可结合PKD1与PKD2的3' 非翻译区,抑制多囊蛋白-1(PC1)和多囊蛋白-2(PC2)的翻译。PC1/PC2复合体是肾小管上皮细胞感知管腔流量的关键结构,其缺失会触发细胞增殖、囊性变。临床前模型证实,阻断miR-17可解除对PKD1/2的抑制,恢复PC1/PC2水平,减缓囊肿扩张。Farabursen(RG-012)是一种抗miR-17寡核苷酸,皮下给药后可高效富集于肾脏,理论上可“上游”修正ADPKD的分子缺陷。
二、研究设计
一项随机、双盲、安慰剂对照的Ⅱ期试验共纳入68例Mayo影像分级1C–1E、估算肾小球滤过率(eGFR)30~90 ml·min-1·1.73 m-2的ADPKD成人患者。受试者按体重随机分配至1 mg/kg、2 mg/kg、3 mg/kg三个剂量组,并增设300 mg 固定剂量开放标签组;安慰剂组10例。主要给药方案为皮下注射,每两周一次(Q2W),连续12周(共7剂),随后4周随访。
主要终点:安全性及24小时尿液中PC1、PC2较基线变化;关键次要终点:MRI 测得的身高校正总肾体积(htTKV)变化百分比。
三、研究结果
安全性:Farabursen总体耐受良好,不良反应多为轻中度局部注射反应或头痛,未出现严重肝毒性、免疫复合物疾病或肾功能急性恶化。
多囊蛋白恢复:2 mg/kg、3 mg/kg及300 mg固定剂量组12周后,尿PC1与PC2均较安慰剂显著升高(p<0.05),呈现剂量依赖性。
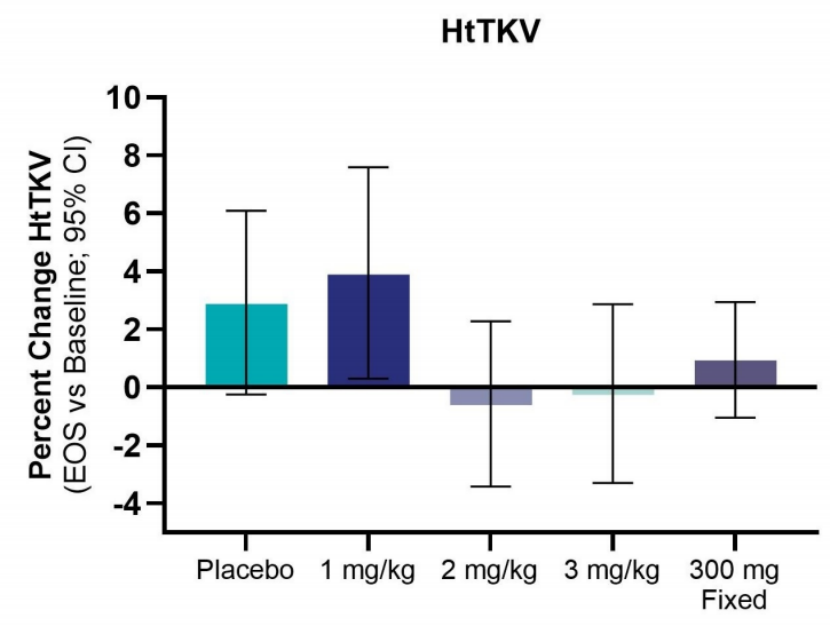
肾体积控制:单剂量组层面,2 mg/kg及以上组htTKV增长幅度均低于安慰剂;预设的2 mg/kg及以上剂量汇总分析显示,12周htTKV平均增幅仅0.24%,而安慰剂组达2.85%,绝对差异2.61%(图1)。该效应独立于PKD1/PKD2突变类型及Mayo分级,提示在疾病不同遗传背景和进展阶段均可获益。
四、临床意义与展望
在仅3个月的治疗周期内,Farabursen即可显著抑制htTKV增长,相当于将年增长率从约12 %降至不足1 %,效果与托伐普坦1年观察数据相当,且未见明显肝毒性。鉴于肾体积增速是ADPKD进展的替代终点并与eGFR下降密切相关,这一结果令人鼓舞。现已计划启动全球Ⅲ期注册试验,进一步验证Farabursen对肾脏硬终点(eGFR斜率、ESKD发生率)的长期影响。若后续研究成功,抗miR-17策略有望成为ADPKD病因治疗的新支柱,为广大患者提供更安全、有效且可长期使用的精准疗法。
Yu Alan S.L, et al. 36:10.1681/ASN.202527ntvtc3, October 2025.doi: 10.1681/ASN.202527ntvtc3
一、研究背景与机制
微小RNA-17(miR-17)家族可结合PKD1与PKD2的3' 非翻译区,抑制多囊蛋白-1(PC1)和多囊蛋白-2(PC2)的翻译。PC1/PC2复合体是肾小管上皮细胞感知管腔流量的关键结构,其缺失会触发细胞增殖、囊性变。临床前模型证实,阻断miR-17可解除对PKD1/2的抑制,恢复PC1/PC2水平,减缓囊肿扩张。Farabursen(RG-012)是一种抗miR-17寡核苷酸,皮下给药后可高效富集于肾脏,理论上可“上游”修正ADPKD的分子缺陷。
二、研究设计
一项随机、双盲、安慰剂对照的Ⅱ期试验共纳入68例Mayo影像分级1C–1E、估算肾小球滤过率(eGFR)30~90 ml·min-1·1.73 m-2的ADPKD成人患者。受试者按体重随机分配至1 mg/kg、2 mg/kg、3 mg/kg三个剂量组,并增设300 mg 固定剂量开放标签组;安慰剂组10例。主要给药方案为皮下注射,每两周一次(Q2W),连续12周(共7剂),随后4周随访。
主要终点:安全性及24小时尿液中PC1、PC2较基线变化;关键次要终点:MRI 测得的身高校正总肾体积(htTKV)变化百分比。
三、研究结果
安全性:Farabursen总体耐受良好,不良反应多为轻中度局部注射反应或头痛,未出现严重肝毒性、免疫复合物疾病或肾功能急性恶化。
多囊蛋白恢复:2 mg/kg、3 mg/kg及300 mg固定剂量组12周后,尿PC1与PC2均较安慰剂显著升高(p<0.05),呈现剂量依赖性。
肾体积控制:单剂量组层面,2 mg/kg及以上组htTKV增长幅度均低于安慰剂;预设的2 mg/kg及以上剂量汇总分析显示,12周htTKV平均增幅仅0.24%,而安慰剂组达2.85%,绝对差异2.61%(图1)。该效应独立于PKD1/PKD2突变类型及Mayo分级,提示在疾病不同遗传背景和进展阶段均可获益。

四、临床意义与展望
在仅3个月的治疗周期内,Farabursen即可显著抑制htTKV增长,相当于将年增长率从约12 %降至不足1 %,效果与托伐普坦1年观察数据相当,且未见明显肝毒性。鉴于肾体积增速是ADPKD进展的替代终点并与eGFR下降密切相关,这一结果令人鼓舞。现已计划启动全球Ⅲ期注册试验,进一步验证Farabursen对肾脏硬终点(eGFR斜率、ESKD发生率)的长期影响。若后续研究成功,抗miR-17策略有望成为ADPKD病因治疗的新支柱,为广大患者提供更安全、有效且可长期使用的精准疗法。
Yu Alan S.L, et al. 36:10.1681/ASN.202527ntvtc3, October 2025.doi: 10.1681/ASN.202527ntvtc3
- 推荐文章
涂晓文教授:中晚期糖尿病肾脏疾病临床关注问题
Sparsentan在FSGS患者中的蛋白尿管理新证据——基于DUPLEX研究2项分析的解读 | NKF SCM 2026
轻松应对,安全无虞!非奈利酮与SGLT2i同步起始,如何化解临床顾虑?
罗洋教授:慢性肾脏病铁代谢紊乱的诊疗进展
伊普可泮治疗IgA肾病:APPLAUSE-IgAN 24个月最终结果与美国真实世界应用现状丨NKF SCM 2026
牛津团队领衔,中国医学科学院阜外医院参与!《柳叶刀》发表最新研究:慢性肾脏病患者全程降压,心血管获益同样显著
北大陈旻教授:补体系统失调在DKD发病机制的全新认知与潜在治疗靶点|WCN中国之声
梅奥诊所Farabursen临床研究:可增加尿多囊蛋白水平并减缓ADPKD患者肾脏体积增长,具有全球首创疾病修饰治疗的潜力丨WCN 2026
【会议预热】“和Fogo一起CPC”第三期:一场跨越中美、连接全球肾脏病理顶尖力量的学术对话即将开启!
全球顶尖肾病临床研究团队——Emerald Clinical(原乔治临床)权威专家阵容
热点辩论:异种器官移植与干细胞疗法能否替代人体器官捐献?|WCN 2026
达格列净进军ADPKD领域:1年临床研究证实显著延缓肾囊肿进展、保护肾功能丨WCN 2026
KI Report首次证实:早期B细胞亚群可预测膜性肾病患者利妥昔单抗治疗后的复发风险
常染色体显性多囊肾病精准治疗与研究范式正在革新中|WCN 2026
学术纵横|11项高质量研究展示2026年初狼疮肾炎领域最新进展
最新研究:UACR在预测儿童肾脏病进展方面优于UPCR
致敬传奇!原研司美格鲁肽登陆中国5周年,持续领跑,不断突破!
Jonathan Barratt教授专访:B细胞疗法兴起,生物标志物赋能肾小球疾病精准诊疗
2025版ISN全球肾脏健康地图(ISN-GKHA)重磅更新:从数据追踪到公平诊疗的行动之路|WCN 2026
阿塞西普每周一次皮下注射治疗IgAN疗效显著,PIONEER研究则进一步探索其在自身免疫性肾小球疾病中的价值|WCN 2026
肾例明鉴 | 一场普通感冒后,她的肌酐飙升至583μmol/L!医生:警惕药物埋下的肾损伤陷阱
新月体性IgA肾病合并无肾小球基底膜线性免疫荧光的抗GBM肾炎:首例病例报道
当狼疮“突袭”肾与脑:多学科协作成功救治一例重症系统性红斑狼疮活动发作
肾域华章 | 真实世界研究REVEAL重磅发布:司维拉姆显著降低ND-CKD患者透析与心血管事件风险
2026 AACE年会公布重要研究:恩格列净相较于达格列净,可降低2型糖尿病患者心肾事件风险
FDA受理奥妥珠单抗治疗系统性红斑狼疮的补充生物制剂许可申请
重磅!瑞利珠单抗两月一针,治疗IgA肾病Ⅲ期I CAN研究中期分析圆满达标
一“比”了然:高血清IgA/C3比值意味着更差的蛋白尿控制
议通知 | 4月24—26日:2026年第二十五届北京肾脏病学术会议
联合用药亦稳定:非奈利酮持续降低2型糖尿病合并CKD患者尿白蛋白——FIVE‑STAR试验二次分析
狼疮肾炎临床缓解期无症状血清学复阳:预防性强化免疫抑制治疗还是观察等待?
限盐也能预防心衰?证据来了!
外周血与肾间质T细胞谱:狼疮肾炎治疗反应的关键预测指标
运动使死亡风险降低46%!82项RCT的荟萃分析证实体育锻炼对CKD的7大获益
初夏相约,共赴京华——北大医院肾脏病精准医学学术会议第一轮通知
超1.5亿人受累!中国30年慢性肾脏病负担特征与变迁给未来防控带来哪些启示
中国台湾IgA肾病患者经扁桃体切除联合激素冲击治疗实现尿学缓解一例
指南共识丨ERA提出急性肾损伤患者出院后管理的十大核心建议
意外发现:常见心脏标志物BNP,竟是糖尿病患者肾脏功能下降的“预警信号”
秉持以心肾结局为中心的治疗策略:一例蛋白尿明显好转但肾功能持续下降DKD患者的诊疗启示
肾域华章丨中山医院丁小强团队真实世界研究:泰它西普联合糖皮质激素治疗IgA肾病,降蛋白尿效果更优
里程碑式突破:FDA批准司帕生坦用于FSGS,开启非免疫抑制治疗新纪元
第十六届东方肾脏病学会议(OCN 2026)第一轮通知
IgA肾病治疗新抉择:同步联合还是序贯递进?
北大医院肾脏内科吕继成教授团队研究成果发表于JASN:揭示ERA与SGLT2抑制剂在IgA肾病中的独立降蛋白作用及联合治疗潜力
补水干预未能降低肾结石复发率,个体化预防已成行业新共识
精准靶向,迭代前行——KDIGO指南专家组解读IgA肾病补体抑制剂与B细胞调节剂的治疗定位
2026年第一季度国际肾脏病学领域进展回顾
【CKM精品课】张春教授:CKM管理的理念革新——从“治病”到“救人”的本质跨越
WCN 2026丨Brad Rovin教授:奥妥珠单抗提供肾小球疾病领域内首个可诱导肾脏组织学缓解并深度清除肾内B细胞的证据
【会议预告】北大医院肾脏病精准医学学术会议
全球首款IgA肾病基因疗法Sefaxersen 70mg:每月一次,PK/PD特征明确、无种族差异,全力推进Ⅲ期IMAGINATION研究丨WCN 2026
丁小强教授主持国际专题研讨会,聚焦AKI全球负担、创新治疗、康复策略丨WCN 2026
赵占正/张军军教授领衔国内多中心回顾研究证实:泽贝妥单抗治疗膜性肾病安全有效,6个月缓解率超六成丨WCN中国之声
突破传统认知,吕继成教授课题组联合国内多家中心发现IgA2亚型在IgA肾病中同样扮演关键致病角色
