- 首页 > 正文
CCSN 2025|马坤岭教授:腹膜透析患者糖脂代谢紊乱的治疗策略
发表时间:2026-01-31 10:38:21
引言
腹膜透析(PD)是慢性肾脏病(CKD)终末期患者的一种重要治疗方式。然而,PD患者常伴有糖脂代谢紊乱,这不仅影响患者的生活质量,还可能加速心血管疾病等并发症的发生。在中华医学会肾脏病学分会第二十八届学术年会(CCSN 2025)上,浙江大学医学院附属第二医院马坤岭教授深入解析了PD患者糖脂代谢紊乱的机制,并提供了有效的治疗策略。

专家简介

浙江大学医学院附属第二医院肾内科主任
英国伦敦大学医学博士,主任医师,教授,博士生导师
浙江省预防医学会理事、肾脏病预防与控制专委会主任委员
中国医师协会整合医学专业委员会委员
中国药理学会肾脏药理专委会常务委员
中国病理生理学会肾脏病理生理专委会委员
中国生理学会肾脏生理专委会委员
中国生物化学与分子生物学会脂质与脂蛋白专业委员会委员
中国老年医学会肾脏病学分会常务委员
中华医学会肾脏病专科分会第10届青年委员
国家自然科学基金通讯评议专家,教育部学位论文评审专家,科技部项目评审专家,Cardiovascular Diabetology杂志副主编
主要从事糖、脂代谢紊乱介导靶器官损害的基础与临床研究,近年来先后主持国家自然科学基金6项,省部级课题7项,获教育部自然科学奖一等奖、教育部科技进步奖二等奖、中华医学科技奖三等奖、华夏医学科技奖三等奖、浙江省科技进步奖一等奖、江苏省科技进步奖二等奖等成果奖励9项。以第一或通讯作者在Hepatology、J Am Soc Nephrol、Cell Death Differ、Cardiovasc Res等国际知名杂志累计发表SCI收录论文49篇。
一、腹膜的结构与功能
腹膜是人体内一个重要的天然半透膜,其面积与成人体表总面积相近,约为1~2 m²。腹膜由间皮细胞、基底膜和腹膜微血管组成,具有完整性,能够进行物质交换[1](图1)。在PD过程中,腹膜作为透析膜,负责清除体内的代谢废物和多余的水分。然而,传统的葡萄糖腹透液对腹膜功能有显著影响,主要包括高糖、高渗、低pH、乳酸盐、葡萄糖降解产物(GDPs)和晚期糖基化终末产物(AGEs)等,这些因素均导致腹膜生物相容性差,会损伤腹膜间皮细胞,引发腹膜纤维化和功能障碍。
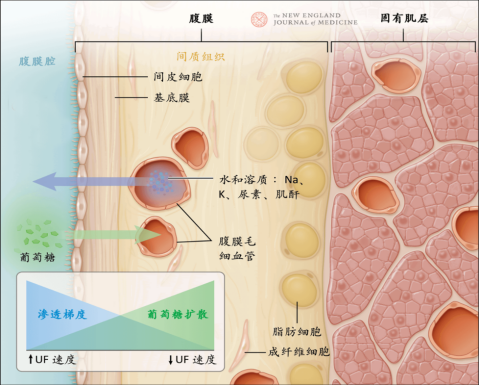
图1. 腹膜的结构和组成
二、尿毒症毒素对糖脂代谢及腹膜功能的影响
(一)诱导全身糖、脂代谢紊乱
尿毒症毒素是导致PD患者糖脂代谢紊乱的重要因素。这些毒素包括吲哚酚硫酸盐(IS)、对甲酚硫酸盐(PCS)和甲状旁腺激素(PTH)等,它们通过多种机制干扰正常的代谢过程。
尿毒症毒素能够干扰胰岛素信号通路,例如抑制PI3K/Akt通路,导致肌肉、脂肪和肝脏对胰岛素不敏感,从而引发胰岛素抵抗。此外,尿毒症毒素还会导致脂代谢障碍。它们抑制脂蛋白脂酶(LPL)的活性,阻碍富含甘油三酯的脂蛋白的清除,导致高甘油三酯血症。同时,肝脏合成极低密度脂蛋白(VLDL)增加也会加重脂代谢紊乱。同时,尿毒症毒素还会刺激免疫细胞释放炎症因子,如TNF-α和IL-6,进一步加重胰岛素抵抗和炎症状态。
(二)直接损害腹膜细胞与功能
尿毒症毒素对腹膜细胞具有直接的毒性作用。IS和PCS等蛋白结合毒素可以直接诱导腹膜间皮细胞的凋亡、衰老和功能障碍。这些毒素还能刺激间皮细胞和皮下的成纤维细胞转化为活化的肌成纤维细胞,启动纤维化进程,导致腹膜纤维化和增厚。此外,毒素与炎症共同作用,上调血管内皮生长因子(VEGF)等表达,促进腹膜新生血管增生,进一步损害腹膜功能。
三、糖脂代谢紊乱对腹膜结构和功能的影响
糖脂代谢紊乱对腹膜结构和功能有显著的破坏作用。高血脂和高血糖环境会加剧腹膜炎症和氧化应激损伤。脂毒性作用下,游离脂肪酸和致动脉粥样硬化脂蛋白浸润腹膜组织,诱导内质网应激和线粒体功能障碍,直接导致间皮细胞凋亡和炎症因子释放。胰岛素抵抗也会影响腹膜细胞的代谢和修复能力,进一步加重腹膜损伤。
腹膜纤维化是糖脂代谢紊乱对腹膜结构的主要影响之一。成纤维细胞的激活和细胞外基质的增生导致腹膜增厚,影响其透析功能。AGEs的沉积与细胞外基质交联,降低腹膜的顺应性,并激活信号通路,进一步加重纤维化。
糖脂代谢紊乱还会导致腹膜功能的改变,如超滤衰竭。有效表面积的增加和渗透剂的快速吸收,以及淋巴吸收的增加,导致水通道蛋白功能受损,影响溶质清除功能。小分子溶质清除率增高,而大中分子溶质清除障碍,进一步加重了患者的代谢紊乱。
四、PD对糖脂代谢的影响
PD本身也会对患者的糖脂代谢产生影响。传统的含糖腹透液在透析过程中会导致大量葡萄糖经腹膜腔吸收,每日可达100~300 g[2]。这种高糖负荷会进一步加重糖代谢紊乱。此外,腹膜转运类型也会影响腹膜腔葡萄糖的吸收,高转运能力患者更容易出现糖代谢异常。
(一)营养状况
PD患者中约30%~50%存在营养不良状况。炎症、慢性代谢性酸中毒、营养物质摄入不足和疾病的高代谢性等因素导致患者长期处于低蛋白状态。传统的腹膜透析液(低pH值和高浓度葡萄糖)会改变腹膜的完整性,促进高转运状态的转换,导致大量蛋白质在透析液中丢失,进一步加重低白蛋白血症[3]。这些均会加剧代谢紊乱。
(二)甲状旁腺功能亢进
甲状旁腺激素水平升高会导致白色脂肪增加、褐色脂肪减少,促进胰岛素抵抗。此外,高磷血症也会通过激活血管平滑肌细胞的SCAP-SREBP2通路,增加内源性胆固醇的合成,促进动脉粥样硬化[4]。
(三)活性维生素D缺乏
活性维生素D缺乏也是PD患者常见的问题。维生素D被证实可以影响脂肪生成、脂肪细胞凋亡、脂肪分解、产热和炎症。缺乏活性维生素D会促进胰岛素抵抗,进一步加重糖脂代谢紊乱[5]。
(四)微炎症状态
微炎症状态是PD患者常见的病理状态。慢性炎症会诱导脂质从血液向组织的重分布,促进动脉粥样硬化和血管钙化[6]。炎症还会诱导心脏血管内皮-间充质转化,促进心肌纤维化形成,进一步加重患者的代谢紊乱[7]。
五、PD患者糖脂代谢紊乱的防治策略
针对PD患者的糖脂代谢紊乱,需要综合考虑多种因素,制定全面的防治策略。
(一)血糖管理
KDIGO 2020指南建议[8],使用糖化血红蛋白(HbA1c)监测PD患者的血糖,每年检测2次,糖尿病PD患者至少每3个月检测一次。当HbA1c与直接测量的血糖水平或临床症状不一致时,可使用连续血糖监测(CGM)。
对于合并糖尿病的PD患者,建议每日一次使用艾考糊精作为长期透析液。首选DPP4抑制剂、胰岛素、噻唑烷二酮类(TZD)药物降糖治疗,可选α-葡萄糖苷酶抑制剂、磺酰脲类药物。
(二)血脂管理
首次诊断的PD患者,建议评估血脂组套(总胆固醇、LDL - C、HDL-C、甘油三酯)。在随访中,血脂不被要求作为主要监测指标。接受透析治疗的CKD患者不建议启动他汀治疗,开始透析时已使用他汀的患者可继续使用他汀。对于空腹血清甘油三酯水平高(>5.65 mmol/L)的患者,建议采用药物治疗。
(三)营养状态评估
建议在PD开始后6~8周内评估营养状况,并至少每4~6个月定期监测一次。通过营养评估,可以及时发现营养不良,调整饮食和治疗方案。
(四)炎症防治
对于C反应蛋白持续升高的PD患者,建议进一步查因,以发现任何可治疗的炎症病因。通过控制炎症,可以减轻代谢紊乱,改善患者预后。
六、总结
PD患者常伴有糖脂代谢紊乱,这不仅影响患者的生活质量,还可能加重心血管疾病等并发症的发生。尿毒症毒素、传统的葡萄糖腹透液、营养不良、甲状旁腺功能亢进、活性维生素D缺乏和微炎症状态等因素均会影响患者的糖脂代谢。因此,需要综合考虑多种因素,制定全面的防治策略,包括改变生活方式、血糖管理、血脂管理、营养状态评估和炎症防治等。通过这些措施,可以改善患者的代谢状况,延缓并发症的发生,提高患者的生活质量。
参考文献
1. Teitelbaum I. N Engl J Med. 2021;385(19):1786-1795.
2. Wang IK, Lin CL, etal. Nephrol Dial Transplant. 2018 Apr 1;33(4):670-675.
3. Kiebalo T, etal. Nutrients. 2020 Jun 8;12(6):1715.
4. Kidney Int. 2021 Jun;99(6):1342-1353.
5. Szymczak-Pajor I, etal. Int J Mol Sci. 2020 Sep 11;21(18):6644.
6. Ma KL, et al. Hepatology. 2008; 48 (3):770-81.
7. Ma KL, et al. Int J Med Sci. 2013;10(4): 420-426.
8. KDIGO Clinical Practice Guideline for Lipid Management in Chronic Kidney Disease.
- 推荐文章
