- 首页 > 正文
DMX-200在原发性局灶节段性肾小球硬化症中的研究进展:ACTION2 Ⅱ期临床试验结果解读
发表时间:2026-02-02 12:03:24
局灶节段性肾小球硬化症(FSGS)是一种以肾小球节段性硬化和显著蛋白尿为特征的疾病,是成人及儿童肾病综合征的重要病因之一。现有治疗手段包括ACEI/ARB及免疫抑制药物,但疗效有限且副作用明显,临床亟需新型治疗方案。DMX-200是一种新型C-C趋化因子受体2(CCR2)通路抑制剂,通过靶向炎症和纤维化通路,为FSGS的治疗提供了新思路。近期,DMX-200的Ⅱ期ACTION2试验结果发表于Kidney International Reports。探讨CCR2通路抑制剂DMX-200联合ARB治疗FSGS的安全性及潜在疗效。
一、研究背景
FSGS是一种病因复杂的肾小球疾病,年发病率约(0.2~2.5)/10万。其发病机制涉及遗传、免疫及外界因素共同诱导的足细胞损伤和硬化进展。约50%的患者在诊断后10年内进展至终末期肾病。尽管目前常规治疗包括血管紧张素转换酶抑制剂(ACEI)或血管紧张素Ⅱ受体拮抗剂(ARB)、糖皮质激素及免疫抑制剂,但蛋白尿完全缓解率不高,且长期应用免疫抑制药物常伴严重不良反应。
CCR2受体及其配体CCL2在FSGS患者肾小球中高表达,可促进巨噬细胞募集及炎症纤维化进程。实验研究显示,CCR2抑制或基因敲除可显著减少蛋白尿并改善肾小球损伤。此外,CCR2与血管紧张素Ⅱ 1型受体(AT1R)在足细胞上共表达,两者形成的功能复合体可能增强受体信号传导,加速肾损伤。
DMX-200(repagermanium)是一种CCR2通路抑制剂,在体外可抑制单核细胞趋化,在动物模型中减轻肾脏炎症与纤维化反应。此前的研究提示,当DMX-200与ARB联合应用时,可在部分肾损伤模型中协同减少蛋白尿及巨噬细胞浸润。因此,本研究旨在验证CCR2与AT1R双通路联合阻断在FSGS患者中的安全性及抗蛋白尿潜力。
二、研究设计与方法
ACTION2为随机、双盲、交叉设计的Ⅱ期临床试验,共纳入8例原发性FSGS患者。所有受试者均接受稳定剂量ARB治疗(厄贝沙坦300 mg),并随机分配至“DMX-200→安慰剂”或“安慰剂→DMX-200”两组,每个治疗周期16周,中间设6周洗脱期(图1)。主要观察终点为药物安全性与耐受性,次要终点为蛋白尿变化;探索性终点包括尿液炎症标志物CCL2及肾功能指标(eGFR)变化。
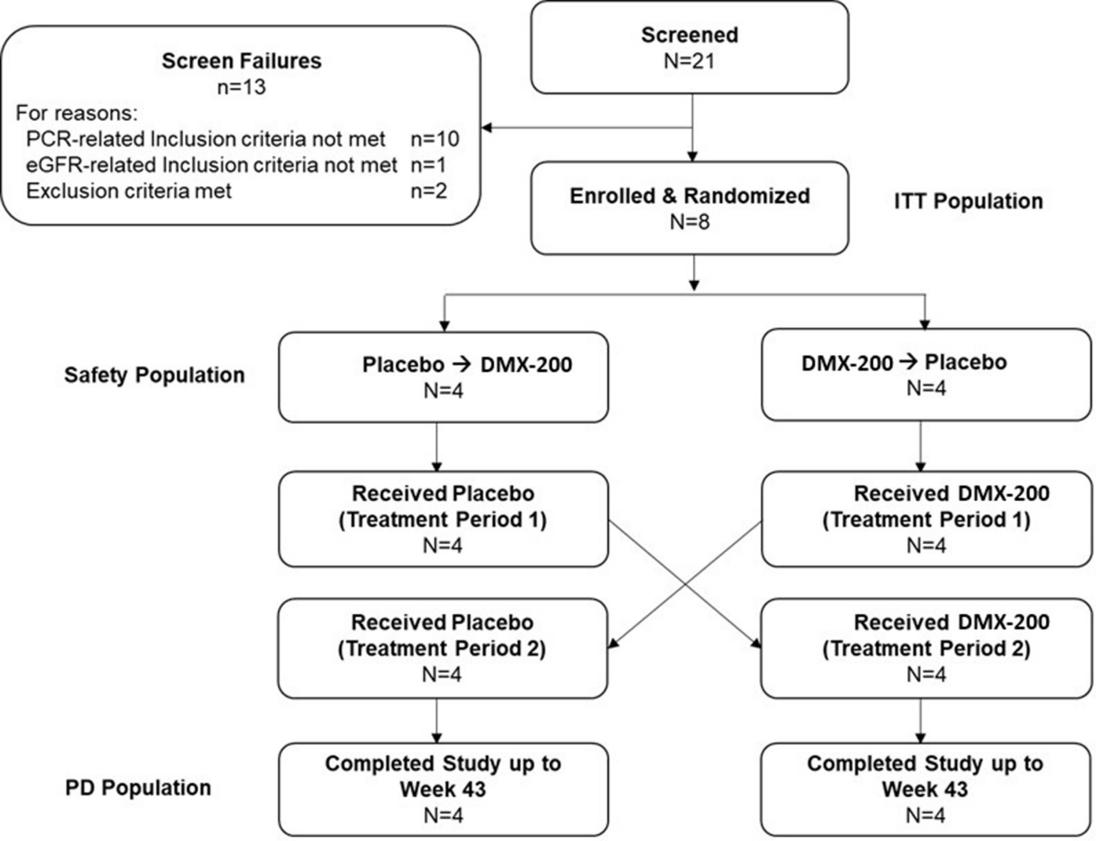
图1. ACTION2试验研究设计
三、主要研究结果
1.患者特征
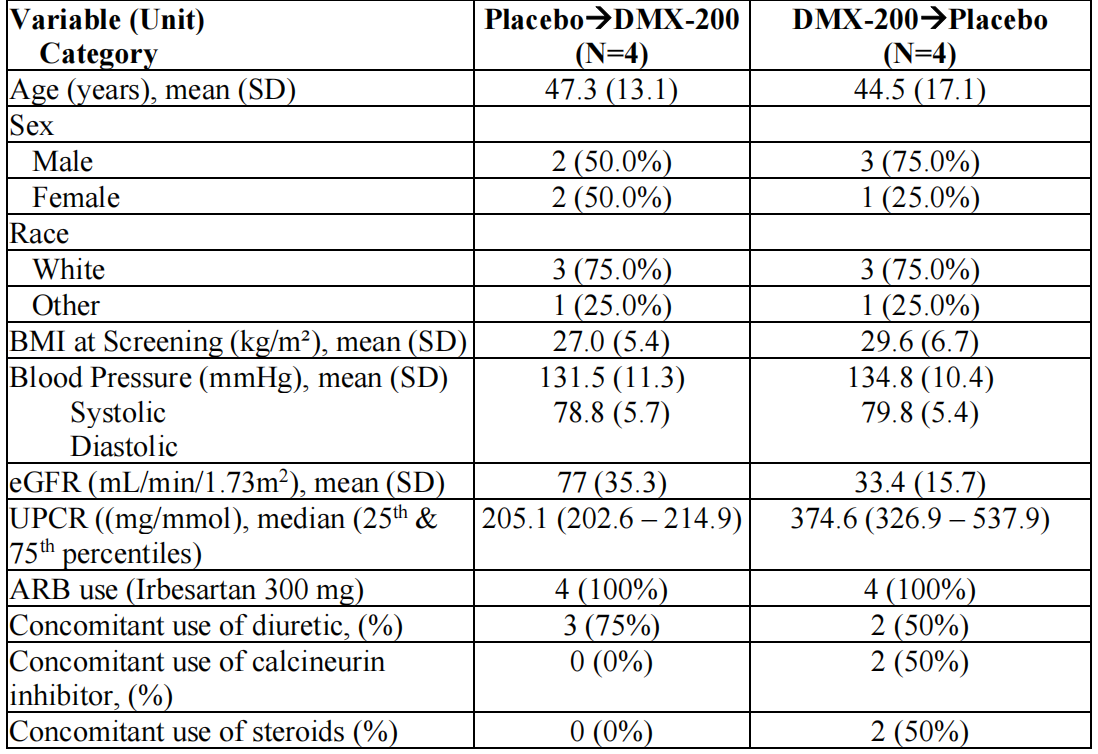
两组患者在年龄、性别、种族、体重指数(BMI)、血压、eGFR和UPCR方面均较为均衡(表1)。所有患者均接受ARB治疗,部分患者同时使用利尿剂、钙调神经磷酸酶抑制剂或糖皮质激素。尽管DMX-200→安慰剂组的基线UPCR较高(中位数374.6 mg/mmol),但两组其他指标无显著差异,保证了研究结果的可比性。
表1. 基线人口统计学特征
2.安全性与耐受性
DMX-200在FSGS患者中表现出良好的安全性和耐受性。安慰剂组和DMX-200组分别有6例(75%)和7例(87.5%)患者报告不良事件(AEs),发生率相近。绝大多数AEs为轻度,仅4例为中度,未出现因治疗相关AEs导致的停药。唯一报告的严重不良事件为肌腱炎,经评估与研究药物无关。实验室参数、生命体征和心电图结果均未发现具临床意义的异常。
3.蛋白尿变化
尽管本研究为探索性试验,未对疗效终点进行统计学显著性检验,但通过几何均值比和95%置信区间(CI)提供了疗效趋势分析。根据符合方案分析(per-protocol analysis),DMX-200治疗16周后,DMX-200治疗后的UPCR几何均值比为0.80(95%CI:0.59~1.07),相当于蛋白尿较基线降低20%;安慰剂组的UPCR几何均值比为0.91(95%CI:0.67~1.22),相当于蛋白尿降低9%。两组间差异为12%(几何均值比0.88,95%CI:0.63~1.22)。尽管结果未达显著性,但整体趋势显示DMX-200有潜在抗蛋白尿作用。
此外,预设的敏感性分析和事后分析均显示,DMX-200在所有预设亚组中均呈现降低蛋白尿的趋势,但意向治疗人群未达到统计学显著性。
4.生物标志物变化
生物标志物分析显示,DMX-200组尿液CCL2浓度的几何均值比为0.83(95%CI:0.60~1.17),较基线降低17%;安慰剂组为1.11(95%CI:0.79~1.56),较基线增加11%。两组间相对变化为25%(几何均值比0.75,95%CI:0.47~1.21),提示DMX-200可能抑制炎症细胞活化与肾脏募集。
四、讨论
伴有蛋白尿的FSGS患者进展为肾衰竭的风险较高,目前尚无获批的治疗方案。对于表现为肾病综合征的患者,临床通常将大剂量全身用糖皮质激素作为经验性一线治疗,而非甾体类免疫抑制剂仅用于持续存在肾病综合征的患者。这类药物的疗效个体差异显著,且鉴于FSGS患者的高发病率及通常较快的疾病进展速度,目前迫切需要一种经证实有效、耐受性良好,且能降低蛋白尿、延缓肾功能进展的治疗方案。
本研究的主要终点是DMX-200在FSGS患者中的安全性与耐受性,研究设计未考虑对次要(有效性)终点、三级终点或生物标志物终点进行统计学检验。局限性包括:样本量较小、治疗持续时间相对较短、疗效反应存在固有变异,以及交叉设计中可能存在的残余治疗效应,这些均限制了对有效性结果的解读。需开展更大样本量、更长随访时间的研究,以明确DMX-200抗蛋白尿效应的强度,及其在延缓FSGS患者肾小球滤过率下降方面的潜在作用。
在整个临床研发过程中,DMX-200联合ARB治疗的耐受性均良好。在已完成的3项Ⅱ期研究(n=80,含本研究结果)中,DMX-200组与安慰剂组报告的治疗期间出现的不良事件(TEAE)在发生率、性质及严重程度上均相近。目前显示的DMX-200安全性和耐受性特征,使其有望成为慢性FSGS患者长期治疗的候选方案。
机制上,DMX-200通过阻断CCR2,可减少炎症介导的足细胞损伤,同时减轻足细胞自身表达的CCR2激活所导致的足细胞损伤。值得注意的是,本研究中DMX-200降低了尿CCL2生物标志物的浓度,提示炎症细胞激活及向肾脏的募集减少。但由于本研究样本量小且未进行统计学检验,这些无显著差异的观察结果需进一步验证。
DMX-200联合ARB治疗的依据来源于:细胞药理学研究显示该联合方案可增强对CCR2信号通路的抑制作用;在FSGS大鼠模型(亚全肾切除模型,STNx)的在体研究中,与溶媒对照组或单独使用任一拮抗剂相比,DMX-200联合ARB能更显著地降低蛋白尿、减少巨噬细胞浸润及足细胞丢失。已知AT1R和CCR2在肾纤维化进展中均具有独立作用,而同时阻断这两种受体的协同效应,为本次Ⅱ期试验采用联合治疗方案提供了充分的治疗学依据。
五、研究意义与展望
作为一项概念验证研究,小样本、短疗程的ACTION2研究显示,DMX-200联合稳定剂量ARB治疗在FSGS患者中显示出良好的耐受性,从而奠定了CCR2抑制策略在FSGS中的临床基础。
鉴于FSGS新治疗方案的临床需求尚未满足,这些数据结合DMX-200现有的全部临床前和临床数据,支持开展更大规模的研究,以探索DMX-200在降低FSGS患者蛋白尿及延缓eGFR下降方面的长期疗效(临床试验编号:NCT05183646/ACTION3)。若结果积极,DMX-200联合ARB可能成为继糖皮质激素和免疫抑制剂之后,FSGS治疗的新型非免疫靶向方案,为难治性蛋白尿及慢性肾功能下降患者提供新的希望。
来源:Heerspink, Hiddo J.L. et al. DMX-200 in Patients with Primary Focal Segmental Glomerulosclerosis: Results of the Phase 2 ACTION2 Trial. Kidney International Reports. https://www.kireports.org/article/S2468-0249(25)00619-9/fulltext
- 推荐文章
