- 首页 > 正文
指南共识|《中国成人IgA肾病及IgA血管炎肾炎临床实践指南(2025)》要点一览
发表时间:2026-02-02 13:29:25
编者按
近日,《中国成人IgA肾病及IgA血管炎肾炎临床实践指南(2025)》正式见刊,旨在为中国成年IgA肾病和IgA血管炎肾炎患者提供基于循证医学证据的诊断、风险分层和治疗建议,以规范和优化临床诊疗实践,改善患者预后。本文整理核心内容,以飨读者。
一、IgA肾病诊断、危险分层、预后评估
临床实践要点:肾脏病理是诊断IgA肾病的金标准。
1. 建议对临床怀疑IgA肾病、蛋白尿≥0.5 g/d(或同等水平)并且没有肾穿刺禁忌的人群进行肾活检,以确保IgA肾病患者的早期诊断和获得及时治疗。
2.目前缺乏被广泛证实的可以用于IgA肾病诊断的血清和/或尿液生物标志物。
3. 推荐应用牛津病理MEST-C评分系统对IgA肾病进行病理分型,对节段硬化病变是否伴足细胞病变进行描述,可同时应用Haas及Lee氏病理分级或其他分级系统。
4.建议关注IgA肾病光镜下肾小动脉微血管病变及电镜下的基底膜病变。
5.建议关注细胞/细胞纤维新月体病变是提示糖皮质激素治疗获益的病理指标。
6.需评估并排除继发性IgA肾病(图1)。
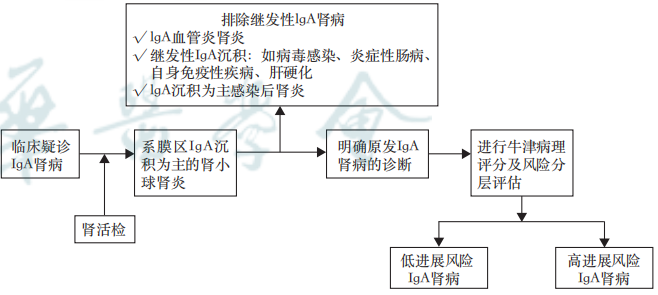
图1. IgA肾病患者初步评估和管理
临床实践要点:所有原发IgA肾病患者均应进行肾脏预后的评估。
1.蛋白尿、估算的肾小球滤过率(eGFR)及血压是评估IgA肾病肾脏进展风险的重要指标。
2.建议应用24 h尿蛋白总量或者尿蛋白/肌酐比值(UPCR)评估蛋白尿程度,蛋白尿缓解可以显著改善患者肾脏预后。
3.建议监测血尿的程度及持续的时间。
4.没有证据支持应用除蛋白尿及eGFR以外的血清和尿液生物标志物对IgA肾病进行预后危险分层。
5.建议应用国际IgA肾病预测工具或其他经过外部独立验证的IgA肾病预后预测工具评估肾功能进展的风险。
临床实践要点:明确存在肾功能丧失风险患者的治疗目标及预测治疗效果的指标。
1.eGFR的每年下降速率小于1 ml·min-1·1.73 m-2。
2. 24 h尿蛋白应当控制在0.5 g/d以内,最好控制在0.3 g/d以内。
3. 牛津病理分型的细胞/细胞纤维新月体病变是提示糖皮质激素治疗获益的病理指标。
4. 目前缺乏足够证据支持应用血清和尿液生物标志物预测治疗效果。
二、治疗总体策略
指南提出IgA肾病分层(针对免疫损伤和慢性肾脏病进展)和分阶段治疗(诱导缓解治疗和维持治疗)的综合治疗理念(图2),诱导缓解阶段治疗需要综合应用针对降低致病性IgA、抑制炎症和延缓慢性肾脏病进展的措施,已达到快速蛋白尿缓解和肾功能稳定的短期目标(图3);维持阶段治疗需要考虑安全且有效的重复或小剂量特异性维持治疗策略,最终达到IgA肾病患者每年eGFR下降速率低于1 ml·min-1·1.73 m-2的长期治疗目标。
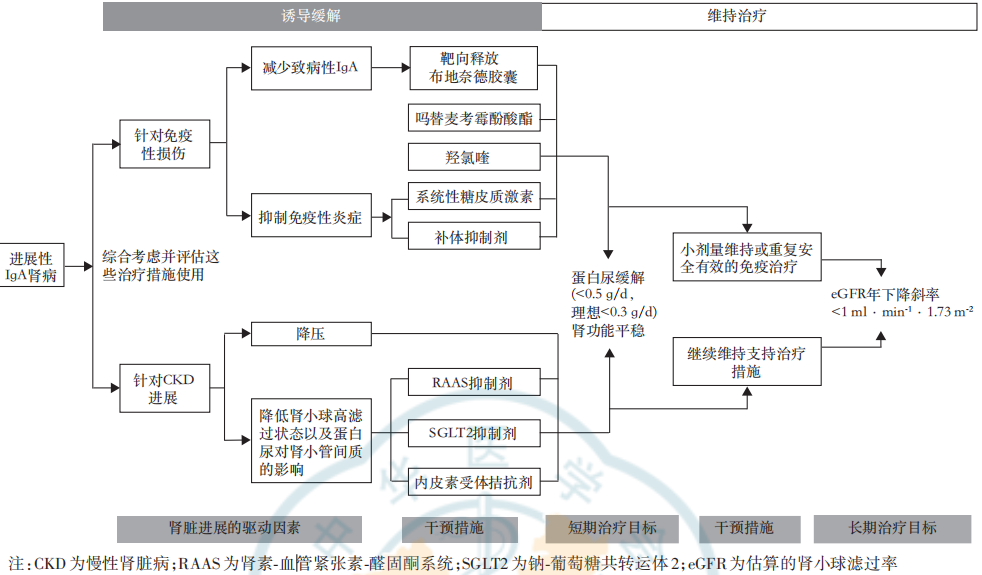
图2. IgA肾病治疗策略图
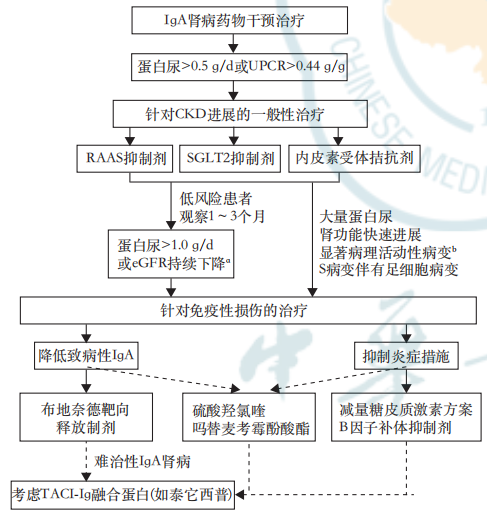
图3. IgA肾病诱导缓解治疗药物干预流程图
三、支持治疗策略
支持治疗措施包括优化生活方式和药物治疗措施,主要的治疗目标是控制血压、改善肾小球高滤过状态、降低蛋白尿以及由此带来肾小管萎缩和间质纤维化;除此以外,还需要控制心血管危险因素,降低未来心血管疾病并发症。对患者采取综合治疗策略,以降低IgA肾病进展及其相关并发症的风险。
推荐意见1:建议患者进行中等强度的体育活动,每周至少累积150 min,或达到与其心血管和身体耐受性相适应的水平(证据级别:Ⅳ级;弱推荐)
推荐意见2:建议患者每天的钠摄入量<2 g(或<90 mmol氯化钠,或<5 g氯化钠)(证据级别:Ⅳ级;弱推荐)
推荐意见3:建议G3~G5期成年患者保持低蛋白饮食,蛋白摄入量≤0.8 g·kg-1·d-1(证据级别:Ⅳ级;弱推荐)
临床实践要点:
1.G3~G5期的IgA肾脏病患者应保持低蛋白饮食,推荐≤0.8 g·kg-1·d-1的蛋白质摄入量。
2.存在进展风险或已经肾功能不全的患者,如果一般情况能耐受,在补充必需氨基酸的前提下尝试更低蛋白饮食(≤0.6 g·kg-1·d-1),需要严密监测营养指标,以避免营养不良。
推荐意见4:推荐IgA肾病患者控制血压< 130/80 mmHg(1 mmHg=0.133 kPa)(证据级别:Ⅱ级;弱推荐)
临床实践要点:对于身体虚弱、跌倒和骨折的高风险、老年且预期寿命非常有限或有症状性体位性低血压的患者,应考虑较少强化的降压治疗。
推荐意见5:推荐尿蛋白>0.5 g/d、G1~G4期的IgA肾病患者,使用RAASi[包括血管紧张素转化酶抑制剂(ACEi)或血管紧张素Ⅱ受体拮抗剂(ARB)]作为一线治疗,尽量达到最大耐受剂量或者说明书推荐的最大剂量(证据级别:Ⅱ级;强推荐) 临床
实践要点:
1.应在RAASi剂量开始或增加后的2~4周内,进行血压、血清肌酐和血清钾的变化检查,具体情况取决于当前的eGFR和血清钾。并根据变化情况,合理调整使用剂量。2. 长期服用RAASi患者,即使eGFR<30 ml?min-1·1.73 m-2,也不建议停用ACEi或ARB。
3. 使用RAASi相关的高钾血症通常可以通过采取措施降低血清钾水平来控制,而不是减少剂量或停止RAASi。
4. 在低血压或无法控制的高钾血症情况下考虑减少剂量或停止ACEi或ARB。
5.不建议联合使用ACEi和ARB或者肾素抑制剂的治疗。
推荐意见6:推荐蛋白尿大于0.5 g/d且eGFR≥20 ml·min-1·1.73 m-2的IgA肾病患者使用SGLT2i进行治疗(证据级别:Ⅱ级;弱推荐)
临床实践要点:
1.对于使用SGLT2i治疗IgA肾病时需要考虑: 在EMPA-KIDNEY和DAPA-CKD试验中,并没有要求患者使用3个月优化的最大耐受剂量RAASi才能被纳入研究;根据患者随机分组时的年龄和eGFR推测EMPA-KIDNEY和DAPA-CKD试验中纳入的IgA肾病患者可能患有IgA肾病病程已经很长;因此,对于eGFR相对代偿较好(>60 ml·min-1·1.73 m-2)的IgA肾病患者,SGLT2i的效果尚缺乏证据。
2. 一旦启动SGLT2i治疗 ,即使eGFR低于20 ml·min-1·1.73 m-2,继续应用SGLT2i也是合理的,除非不能耐受或启动肾脏替代治疗。
3. 在长时间禁食、手术或严重疾病(可能有更大的酮症风险)时,停用SGLT2i是合理的。
4. 即使停用SGLT2i,其保护作用可能仍持续存在。
推荐意见7:建议对有进行性肾功能下降风险的IgA肾病患者使用内皮素受体拮抗剂(ERA) 包括斯帕森坦(sparsentan)或阿曲生坦进行治疗(证据级别:Ⅱ级;弱推荐)
临床实践要点:
1.除了斯帕森坦或阿曲生坦以外,其他ERA目前仍在研究中,可能有效。
2.应用ERA需要注意是否有低血压和水钠潴留,并可以滴定加量。
3.ERA和SGLT2i联合治疗,有可能减轻水钠潴留,同时促进蛋白尿的减少。
4.女性患者胎儿毒性风险增加,需要避孕,并定期进行妊娠检测。
四、抑制肾小球炎症治疗策略
推荐意见8:对于eGFR≥30 ml·min-1·1.73 m-2经过充分支持治疗仍然存在高风险进展的IgA肾病,在充分考虑风险和获益后,建议6~9个月减量糖皮质激素方案治疗,同时需要考虑预防感染(证据级别:Ⅱ级;弱推荐)
临床实践要点:
1. 这一决策需要充分考虑治疗带来的获益和风险,并与患者进行充分沟通。在评估风险时不仅仅依赖于患者是否持续性蛋白尿>1 g/d,而更重要是评估患者进展的风险(eGFR下降速率或肾衰竭的风险),风险越大的人可能越得益于糖皮质激素治疗。
2. 除了肾病综合征或急进性肾小球肾炎(RPGN)的IgA肾病,考虑到足量糖皮质激素治疗的风险,建议应用减量糖皮质激素方案。
3. 建议糖皮质激素治疗时需要评估预防耶氏肺孢子菌肺炎(PJP)治疗,以及胃黏膜保护和骨质疏松预防措施。
4. 除了急性肾损伤外,目前缺乏eGFR低于30 ml·min-1·1.73 m-2应用糖皮质激素获益的证据。
推荐意见9:对于充分支持治疗后仍然存在进展风险的IgA肾病患者,补体旁路途径B因子阻断药物伊普可泮可以显著降低蛋白尿,对于经过常规治疗后仍然持续蛋白尿患者可以考虑使用(证据级别:Ⅱ级;弱推荐)
临床实践要点:
参照中国2024年补体相关性肾病诊断和治疗专家共识建议,在药物使用前2周接种脑膜炎球菌疫苗和肺炎球菌疫苗。紧急情况下需要即刻应用的可以考虑疫苗接种同时抗生素预防感染直至2周以后。
1.脑膜炎球菌疫苗:(1)接种时间:建议在补体抑制剂治疗前至少2周接种。(2)疫苗类型:可选择ACYW135 群脑膜炎球菌多糖疫苗(MPV-ACYW),或ACYW135群脑膜炎球菌多糖结合疫苗(MPCV-ACYW)。(3)接种剂次:1剂次。(4)复种:根据补体抑制剂治疗需求,多糖疫苗可3年后复种1剂次,结合疫苗可5年后复种1剂次。
2. 肺炎球菌疫苗:(1)接种起始时间:建议在补体抑制剂治疗前至少2周接种;(2)疫苗类型:可选择13价肺炎球菌结合疫苗(PCV13)和23价肺炎球菌多糖疫苗(PPV23);(3)接种剂次:2 剂次;(4)免疫程序:首剂次接种选择 PCV13,12 个月后再接种1剂次PPV23。
推荐意见10:建议经过支持治疗后仍然存在进展风险的IgA肾病患者,可以接受 9个月的靶向释放布地奈德胶囊治疗(证据级别:Ⅱ级;弱推荐)
推荐意见11:如果有可能,可以让IgA肾病患者加入疾病登记系统和考虑参加临床试验(证据级别:Ⅳ级;弱推荐)
临床实践要点:
1.相较于传统系统糖皮质激素治疗,靶向释放布地奈德胶囊实现了高效局部抗炎、靶向递送、持续治疗效果及良好安全性,为IgA肾病患者提供了一种新的治疗选择。靶向释放布地奈德胶囊适用于进展风险的IgA肾病,其人群获益大于风险,但对于个体而言仍需要个体化使用并监测副作用。2. 靶向释放布地奈德胶囊用于具有进展风险的原发性IgA肾病成人患者,可考虑给予 16 mg/d,持续9个月时间,由于是对因治疗,起效比较慢,如果已经用药,足疗程用完 1 个周期再评估效果,后续逐渐停药。推荐意见12:对于中国IgA肾病患者,在经过充分支持治疗和常规免疫抑制治疗后,若仍存在高风险进展或表现为难治性IgA肾病,可考虑应用泰它西普作为新的治疗选择(证据级别:Ⅱ级;弱推荐)。
推荐意见13:对于中国IgA肾病患者经过充分支持治疗仍然存在高风险进展的患者,建议可以加用吗替麦考酚酯(MMF)或MMF联合减量糖皮质激素治疗(证据级别:Ⅱ级,弱推荐)
推荐意见14:对于中国IgA肾病患者经过充分支持治疗后仍然存在持续性蛋白尿的患者,建议考虑加用硫酸羟氯喹治疗(证据级别:Ⅱ级;弱推荐)
六、特殊情况下IgA肾病的处理
(一)IgA肾病合并肾病综合征
临床实践要点:IgA肾病合并肾病综合征是IgA肾病中的少见情况,患者可表现为大量蛋白尿(24 h 尿蛋白定量>3.5 g/d),低蛋白血症(血白蛋白<30 g/L),水肿及高脂血症。肾穿刺病理表现为系膜区IgA沉积,光镜及电镜表现与微小病变肾病一致的患者,考虑为轻微病变型IgA肾病,此类患者可完善nephrin抗体协助诊断,其治疗方案参照微小病变肾病。
(二)IgA肾病合并急性肾损伤
临床实践要点:IgA肾病合并急性肾损伤的患者,若合并肉眼血尿,应予以积极支持治疗。血尿消失2周后肾功能仍不恢复,需考虑重新肾活检。未合并肉眼血尿且排除了肾前性、肾后性及药物肾毒性等可逆性因素后,应尽快肾活检明确是否合并广泛新月体形成、恶性高血压及急性肾小管间质损伤等情况。
(三)IgA肾病合并RPGN
临床实践要点: 1.IgA肾病合并 RPGN的定义为 3个月内eGFR下降≥50%,并且除外了 ANCA 相关性血管炎及抗肾小球基底膜病等其他原因导致的 RPGN,以及肾前性或肾后性等因素所致的快速肾功能进展。 2.表现为RPGN的IgA肾病需要尽快进行肾活检,明确是否存在明确重度系膜增生、毛细血管内增生、广泛新月体形成及纤维素样坏死的病理表现。对于RPGN的IgA肾病患者可参照ANCA相关性血管炎治疗指南,应用糖皮质激素及环磷酰胺治疗,血浆置换及利妥昔单抗治疗的证据不足。
(四)IgA肾病患者的妊娠管理
临床实践要点: 1.建议IgA肾病妊娠患者同时接受肾内科、产科及新生儿科的多学科咨询,IgA肾病患者出现产科及胎儿不良结局风险较普通人群更高,慢性肾脏病3期以下患者存在加快肾脏进展风险。需要充分与患者及其家属沟通,在知情理解相关风险的前提下,依从患者意愿再考虑妊娠决策。 2.RAASi、SGLT2i、靶向释放布地奈德胶囊和斯帕森坦不建议应用于妊娠期及哺乳期IgA肾病患者。硫酸羟氯喹可应用于妊娠期IgA肾病患者。
七、IgA血管炎肾炎(过敏性紫癜肾炎)
(一)成人IgA血管炎和IgA血管炎肾炎的诊断
临床实践要点: 1.成人IgA血管炎可参照儿童IgA血管炎分类标准进行诊断。 2. 建议对尿蛋白≥0.5 g/d 持续超过4周或出现肾功能损害的IgA血管炎患者进行肾活检。
表1. IgA血管炎EULAR/PRINTO/PReS分类标准
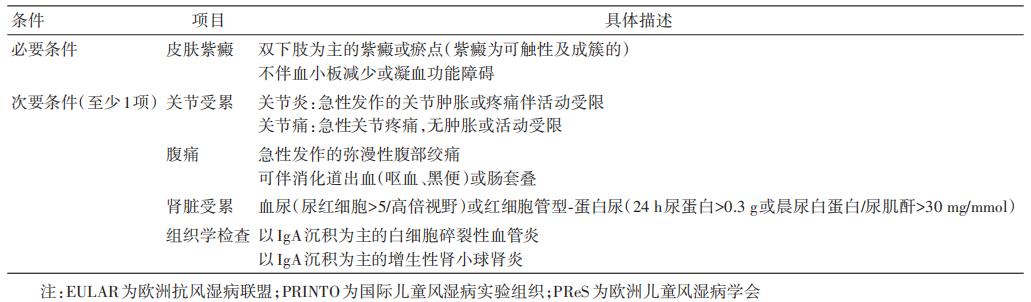
临床实践要点:
1.尿蛋白升高、高血压和诊断时肾功能受损是IgA血管炎肾炎不良结局的风险因素。
2. 可以参照牛津 MEST?C 分类标准对成人IgA血管炎肾炎肾脏病理进行评估,肾小管间质(T)病变和肾脏不良预后相关,内皮病变(E)病变与肾功能经初始改善后逐渐进行性下降这一临床表型存在相关性。
(三)存在肾功能丧失风险患者的定义和治疗目标
临床实践要点:
1. 未经治疗或经过治疗后,24 h 尿蛋白大于0.5 g/d的IgA血管炎肾炎患者为存在肾脏进展风险的IgA血管炎肾炎患者。
2.对于存在肾功能丧失风险的IgA血管炎肾炎患者,eGFR下降率控制目标为<1 ml·min-1·1.73 m-2·年-1,尿蛋白控制目标为小于 0.5 g/d,最好控制于0.3 g/d以下。
(四)IgA血管炎肾炎的治疗
推荐意见15:不建议在没有肾脏受累的IgA血管炎患者中应用系统性糖皮质激素预防肾炎发生(证据级别:Ⅱ级;强推荐)
推荐意见16:参照IgA肾病制定存在肾功能丧失风险的IgA血管炎肾炎患者的治疗策略(证据级别:Ⅳ级,弱推荐)
临床实践要点:
1.存在肾功能丧失风险的IgA血管炎肾炎患者的诱导缓解治疗应同步考虑针对IgA血管炎的免疫性损伤和针对慢性肾脏病进展进行干预,以蛋白尿缓解并维持肾功能稳定为治疗目标。后续的维持治疗应维持充分的支持性治疗措施,并可小剂量维持或重复安全有效的免疫治疗措施,以维持其eGFR下降率控制目标为<1 ml·min-1·1.73 m-2·年-1为治疗目标。
2.存在肾功能丧失风险的IgA血管炎肾炎患者的免疫治疗可参照IgA肾病的系统性糖皮质激素方案,同时应用磺胺甲噁唑-甲氧苄啶预防PJP,并与患者详细讨论潜在风险和获益。
3.IgA血管炎肾炎的支持性治疗包括:生活方式管理,如低盐饮食、戒烟、体重管理和运动指导;控制血压≤130/80 mmHg;可单独或联合使用RAASi和SGLT2i改善肾小球高滤过状态和降低蛋白尿。
4.应重视对IgA血管炎肾炎患者进行心血管疾病风险评估和管理,必要时采取适当的干预措施,如他汀类药物治疗。
5. 建议IgA血管炎肾炎患者参加新药临床研究。
(五)IgA血管炎肾炎特殊情况的治疗
临床实践要点:
1. 表现为RPGN的IgA血管炎肾炎的定义为3个月内eGFR下降≥50%,并且除外了ANCA相关性血管炎及抗肾小球基底膜病等其他原因导致的RPGN以及肾前性或肾后性等因素所致的肾功能进展。
2. 可参照 ANCA 相关性血管炎的免疫抑制治疗方案,对表现为 RPGN 的IgA血管炎肾炎患者进行治疗,包括糖皮质激素冲击治疗和环磷酰胺。
3. 免疫抑制治疗的潜在获益和风险应个体化评估,并与患者进行充分沟通。
4.IgA血管炎肾炎患者可能存在显著的IgA血管炎肾外受累(如:肺、胃肠道和皮肤),免疫抑制治疗方案可能同时取决于肾外脏器受累的严重程度。
5.目前还没有足够的证据证实血浆置换治疗合并RPGN的IgA血管炎肾炎的疗效。
- 推荐文章
