- 首页 > 正文
肾例明鉴|预后更差?家属拒绝行血浆置换?背水一战,成功救治1例狼疮性肾炎合并血栓性微血管病肾损害患者
发表时间:2026-02-03 11:33:47

一、临床资料
女性,23岁。主诉:全身水肿1个月,发热1天。
现病史:患者1个月前无诱因逐渐出现全身水肿,伴尿少。自服“中药”3天后,症状无好转,当地医院查尿常规:蛋白(+++),RBC和WBC均阳性;ALB 27.2g/L,SCr 113.3μmol/L;血常规示三系减少;予甲泼尼龙40mg/d及对症治疗,症状好转。1天前发热,伴咽痛,水肿加重,尿量减少,当地予头孢类抗生素及降温等对症治疗。我院急诊查血常规:WBC 18.9x109/L,PLT 110x109/L,Hb 105g/L,SCr 242μmol/L。患者发病来神清,无皮疹、关节痛、光过敏、口腔溃疡,无口干、眼干。
既往史:无特殊。
入院查体:BP 110/70mmHg,HR 82次/分。全身未见皮疹,浅表淋巴结未触及肿大。颜面、眼睑及双下肢水肿。心肺腹查未见明显异常。辅助检查:血常规:WBC 16.82x109/L,Hb 65g/L,PLT 63x109/L,Ret升高;外周血破碎RBC 1%。尿检:PRO(+++),定量3.59g/d,RBC多数/HP,正常形态为主,WBC 1~5/HP,多形核55%。尿培养(-)。生化:ALT、AST正常,ALB 28.4g/L,SCr 358μmol/L,非结合胆红素24μmol/L,LDH 297IU/L;凝血:D-二聚体7.84mg/L,FDP 160mg/L,余未见异常。免疫学检查:C3 0.42g/L,C4 0.07g/L。ANA(+),抗ds-DNA抗体(+),抗SSA(+),余ENA谱(-),ACL(-)。Coombs试验(-),PAIgG(-)。骨髓穿刺正常。双肾B超基本正常。UCG正常。乙肝五项及丙肝抗体均(-)。
初步诊断:系统性红斑狼疮;狼疮性肾炎;急性肾损伤;贫血、血小板减少原因待查:系统性红斑狼疮?血栓性微血管病?
患者青年女性,急性病程,多系统受累。①肾脏:表现为蛋白尿、非变形血尿、无菌性白细胞尿;在“上感"诱因下,出现急性肾损伤。②血液系统:表现为三系减少,激素治疗后三系均有上升;入院后完善骨穿等检查,无其他病因证据;提示可能存在自身免疫性疾病。
检查发现患者ANA(+),抗ds-DNA抗体(+);结合肾脏及血液系统表现,符合ACR1997年SLE诊断标准,系统性红斑狼疮(SLE)及狼疮肾炎(LN)诊断明确。但是该患者有两点比较特殊:①尿中RBC非变形,目前无泌尿外科疾病证据,当肾小球疾病较为严重例如新月体形成,或者血管病变时可出现非变形RBC;②患者外周血网织红细胞升高、外周血可见破碎RBC,血LDH、D-二聚体及FDP增高,提示微血管病性溶血及血栓形成。肾穿刺活检对于明确LN病理分型、判断病情活动及是否存在其他合并症具有重要价值。
患者于入院第4天行肾穿刺活检。免疫荧光:IgG(++),C3(++),颗粒样毛细血管壁、系膜区沉积。光镜(图1):可见34个肾小球,肾小球系膜细胞和内皮细胞弥漫增生,白细胞浸润,基底膜增厚,部分缺血性皱缩,系膜区、上皮下、内皮下嗜复红蛋白沉积,局灶节段性微血栓及白金耳形成,部分缺血性皱缩;肾小管上皮细胞空泡及颗粒变性,局状及片状萎缩,肾间质灶状及片状淋巴和单核细胞浸润;小动脉管壁增厚,内膜肿胀伴血栓形成。该表现符合毛细血管内增生性狼疮肾炎伴基底膜增厚[Ⅳ-G(A)+V]伴血栓性微血管病(TMA)。
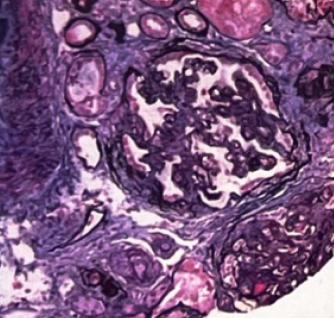
图1.光镜表现
电镜(图2):肾小球系膜细胞和内皮细胞弥漫增生伴中性粒细胞浸润,基底膜内疏松层增厚,上皮下、基底膜内、内皮下及系膜区均可见电子致密物沉积,上皮足突广泛融合,符合光镜诊断。
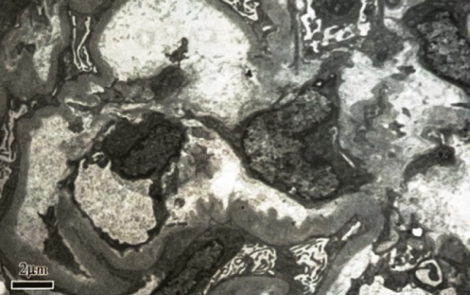
图2. 电镜表现
入院后SCr升至447μmol/L,予透析和甲泼尼龙40mg/d。肾穿刺明确病理诊断后,推测该患者的TMA系AKI的主要原因,但患者因经济原因拒绝血浆置换。鉴于其TMA可能与SLE的自身免疫机制相关,故予甲泼尼龙500mg/d连续3天,SCr和尿量渐正常,1周后加用静脉环磷酰胺0.4g。出院时Hb 89g/L,PLT正常,LDH转为正常。门诊规律激素减量及每月静脉滴注环磷酰胺,尿蛋白及血尿渐转阴,肾功能及血常规维持正常。
最终诊断:系统性红斑狼疮;狼疮性肾炎;毛细血管内增生性狼疮肾炎伴基底膜增厚伴血栓性微血管病;急性肾损伤。
三、讨论
系统性红斑狼疮(SLE)是累及全身多系统的一种自身免疫性疾病,引起一系列全身炎症反应,而系统性红斑狼疮约50%以上患者累及肾脏,形成狼疮性肾炎,狼疮性肾炎为肾小球肾炎中最常见的继发性肾小球肾炎的一种,是SLE 较常见且严重的并发症,狼疮性肾炎既可与SLE的其他临床症状同时出现,也可为首发表现。狼疮性肾炎好发于育龄期妇女,但在儿童及老年性别差别不大[1]。
狼疮性肾炎(LN)是临床上常见的继发性肾小球肾炎类型,不仅可累及肾脏肾小球毛细血管内皮细胞,还可累及肾脏其他微血管如小叶间动脉、小动脉,造成内皮细胞损伤,从而引起一系列补体激活等炎症反应,导致血管内病理改变。LN患者中肾血管病变也得到了越来越多的研究,研究表明肾血管病变可对LN患者远期的肾脏预后产生不良影响,并在治疗方案选择上起着重要的作用。2003年国际肾病学会/肾脏病理学会(ISN/RPS)明确了LN 患者病理中血管损伤的重要性,对肾小管萎缩、间质炎症及纤维化、动脉硬化或其他的血管病变进行了定义及描述。LN患者中肾微血管病变的发病机制仍有待进一步研究,LN的动物模型结果表明,其损伤机制为免疫系统功能障碍,可能是免疫复合物沉积诱导肾脏微血管内皮细胞的激活与功能结构的紊乱。虽然不同类型的血管病变有一些共同的发病机制,但每一种类型的病变都各自有其自身的特点。LN血管病变中,病理分类可大致分为常见的五种:免疫复合物沉积型微血管病(ICD)、动脉硬化 (AS)、血栓性微血管病(TMA)、非炎性坏死性血管病变(NNV)和真性血管炎(TRV)。LN患者不同肾血管病变类型的患者肾脏存活率是不同的,一项研究对比了伴有肾血管损伤与不伴有肾血管病变的LN患者平均随访5年的肾脏存活率,结果显示,伴有肾血管病变的LN患者的表现为更差的肾脏预后,其中五种常见病因中,ICD为第二差的分组,而伴有TMA病变的LN患者的肾脏预后最差[2-4]。
TMA是一组急性临床病理综合征。TMA包括溶血尿毒综合征和血栓性血小板减少性紫癜,其他还有恶性高血压、硬皮病肾危象、SLE、妊娠相关肾病等。TMA的临床特征为微血管病性溶血性贫血、血小板减少以及脏器损害。微血管病性溶血性贫血主要表现为溶血性贫血特征如血红蛋白水平下降、血清间接胆红素升高等;血浆或尿中出现游离血红蛋白;外周血涂片可见破碎红细胞。部分LN 患者虽然肾脏病理改变具有TMA特征,但无微血管病性溶血性贫血等临床表现,被认为是局限于肾脏的TMA。LN合并TMA的临床特征较为突出,高血压发生率明显高于其他类型血管病变,血液系统受累如贫血和血小板减少更严重,且具有更高的血肌酐值、尿蛋白量以及更严重的病理改变包括肾小球炎症细胞浸润、肾间质纤维化、肾小管萎缩等。TMA病理学表现包括急性病变和慢性病变,急性病变主要包括微血管内皮损伤造成的小动脉和(或)肾小球毛细血管内血栓形成,血管腔内可见红细胞碎片;慢性病变主要表现为肾小球基底膜增厚呈“双轨征”、间质小动脉内皮增生呈“葱皮样”改变。不同病因引起的TMA发病机制不同,继发于SLE的TMA发病机制可能与相关的自身抗体(如抗ADAmT-13抗体)及补体过度激活有关[5,6]。
本病例是一例LN合并TMA肾损害的典型范例。LN中TMA发生率较低,目前尚无确切数字。LN中出现TMA,大多数学者认为TMA是继发于SLE,因为大多数相关病例报道均提示SLE诊断在前而TMA发生在后。活动性LN与TMA在临床上不易鉴别,但单纯活动性LN很少出现非免疫性溶血。另外,即使病理明确诊断为LN+TMA,也要考虑是否伴发以下情况:抗磷脂抗体综合征、硬皮病或恶性高血压等。
LN合并TMA的治疗首选血浆置换,同时强调激素及免疫抑制剂的规律治疗。虽然本例患者由于经济原因未行血浆置换,而使用了激素冲击并予正规活动性LN的诱导缓解治疗方案,取得了较好的结果,但长期疗效尚需关注。
参考文献:
[1] Yu C, Li P, Dang X, Zhang X, Mao Y, Chen X. Lupus nephritis: new progress in diagnosis and treatment. J Autoimmun. 2022 Oct;132:102871.
[2] Park MH, Caselman N, Ulmer S, Weitz IC. Complement-mediated thrombotic microangiopathy associated with lupus nephritis. Blood Adv. 2018 Aug 28;2(16):2090-2094.
[3] Munroe ME, James JA. Genetics of Lupus Nephritis: Clinical Implications. Semin Nephrol. 2015 Sep;35(5):396-409.
[4] Iwamoto T, Niewold TB. Genetics of human lupus nephritis. Clin Immunol. 2017 Dec;185:32-39.
[5] Thompson GL, Kavanagh D. Diagnosis and treatment of thrombotic microangiopathy. Int J Lab Hematol. 2022 Sep;44 Suppl 1(Suppl 1):101-113.
[6] Chen WC, Ko PS, Wang HY, Liu YC, Hsiao LT, Gau JP, Liu JH. Difference in thrombotic microangiopathy between concurrently and previously diagnosed systemic lupus erythematosus. J Chin Med Assoc. 2020 Aug;83(8):743-750.
- 推荐文章
