- 首页 > 正文
NEJM重磅: VALIANT研究证实Pegcetacoplan有效降低C3肾小球病与免疫复合物型MPGN患者蛋白尿达68%
发表时间:2026-03-15 10:09:20
C3肾小球病与原发性免疫复合物型膜增生性肾小球肾炎(MPGN)是一类以补体C3调节异常为核心病理特征的罕见肾小球疾病,其共同病理表现为肾小球内异常C3沉积,最终常导致不可逆性肾损伤,甚至肾衰竭。
补体系统激活异常是C3肾小球病和免疫复合物型MPGN的核心发病机制,尽管两者在组织学特征上存在差异,但补体调节紊乱均是驱动疾病进展的关键因素。因此,靶向补体激活通路的抑制剂成为这类疾病治疗的研究方向。Pegcetacoplan作为一种新型C3/C3b双靶点抑制剂,能够同时阻断补体经典途径、凝集素途径和旁路途径的激活,直接抑制C3和C5转化酶活性,为阻断肾小球补体沉积和肾损伤提供了新的治疗策略。近期,《新英格兰医学杂志》(NEJM)发表的VALIANT Ⅲ期临床试验结果为该类疾病提供了治疗新选择。
一、研究背景
C3肾小球病与原发性免疫复合物型MPGN是两种罕见的肾小球病变,其特征为C3调节异常,通常导致肾小球C3异常沉积并引发不可逆的肾脏损伤。数据显示,诊断后10年内,高达50%的患者会进展为晚期肾衰竭,最终需接受透析或肾移植治疗。复发性C3肾小球病可导致高达60%的移植肾功能失败。尽管原发性免疫复合物型MPGN具有独特的组织学特征——除C3肾小球病中观察到的肾小球C3沉积外,还伴有免疫球蛋白沉积,但补体调节异常仍是这两种疾病发病机制的核心。
Pegcetacoplan通过结合C3及其活化片段C3b,从而调控C3的裂解及下游补体效应分子的生成。该药物通过靶向C3和C3b,经由经典补体途径、凝集素途径及替代补体途径抑制补体激活。此外,Pegcetacoplan通过抑制C3b在复合物中的作用,直接抑制C3和C5转化酶的活性,为阻断肾小球补体沉积和肾损伤提供了新的治疗策略。
既往Ⅱ期研究显示,Pegcetacoplan可以有效且安全治疗C3肾小球病与原发性免疫复合物型MPGN患者,此次VALIANT研究旨在评估Pegcetacoplan治疗青少年和成年C3G和免疫复合物型MPGN患者(包括原发性肾脏疾病及肾移植后复发的患者)的疗效与安全性。二、研究设计
VALIANT试验是一项多中心、Ⅲ期、双盲、安慰剂对照临床试验。该试验在19个国家的122个研究中心开展,试验设计包含四个阶段:10周筛选期、26周随机对照治疗期、26周开放标签治疗期,以及未进入长期延伸试验患者的8周随访期。
试验采用1:1随机分组方式,将261例符合条件的患者分为Pegcetacoplan治疗组(n=63)和安慰剂对照组(n=61)。主要终点为第26周时尿蛋白/肌酐比值(UPCR)相对基线的对数转换比值。关键次要终点为肾脏复合终点(eGFR稳定[eGFR降低≤15%]和UPCR降低≥50%)、UPCR降低≥50%的患者比例、C3肾小球病组织学指数活动评分变化、C3免疫荧光染色强度降低≥2级以及eGFR变化等。
三、研究结果
1、主要终点
治疗26周后,Pegcetacoplan组蛋白尿的降幅显著高于安慰剂组:UPCR几何平均变化为-67.2%(95%CI:-74.9~-57.2),而安慰剂组为2.9%(95%CI:-8.6~15.9),相对差异为68.1%(95%CI:57.3~76.2;P<0.001,图1A)。此外,pegcetacoplan组在治疗启动后第4周(首次采样时)即观察到蛋白尿减少,并持续至第26周;而安慰剂组的蛋白尿水平基本未见变化。亚分析显示,蛋白尿减少程度在各患者亚组间总体一致,包括无论是否使用免疫抑制剂(图1B)。
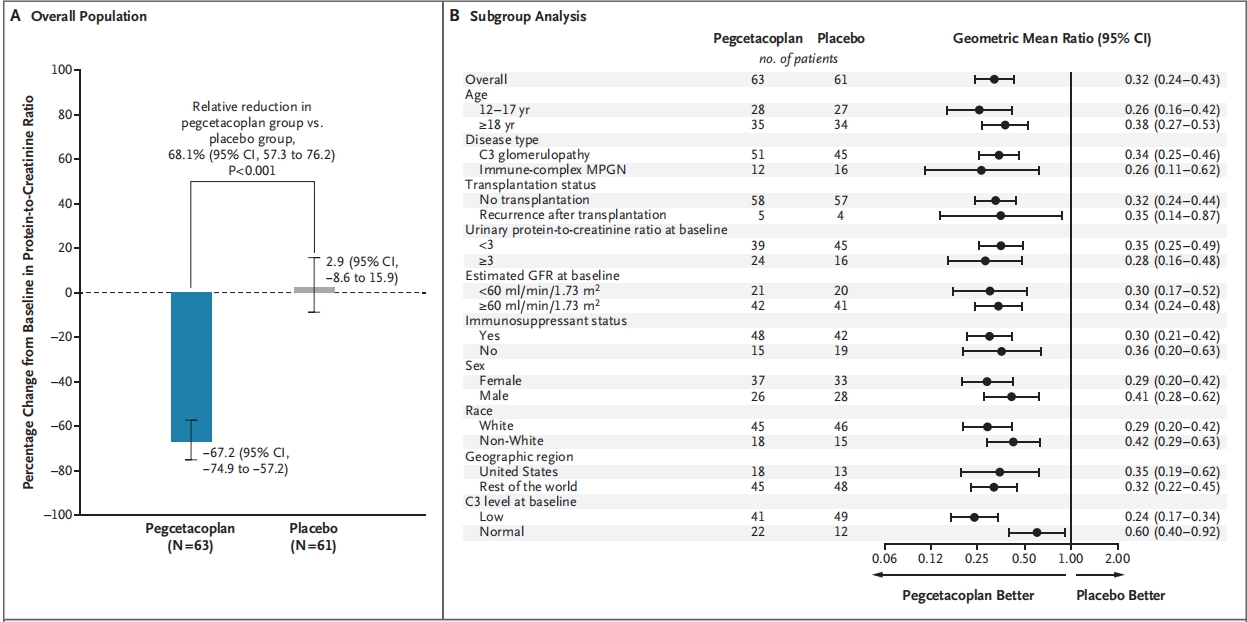
图1. 第26周时UPCR的变化
2、次要终点
在对5项次要终点分层检验中(表1),与安慰剂组相比,Pegcetacoplan组达到肾脏复合终点(估算肾小球滤过率[eGFR]稳定且UPCR降低≥50%)的患者比例显著更高(49% vs. 3%)(RR 14.4,95%CI:3.7~56.9;P<0.001),这一差异主要由蛋白尿下降驱动——Pegcetacoplan组UPCR降低≥50%的患者达60%,而安慰剂组为5%(RR 12,95%CI:4.0~36.1;P<0.001)。
在事后分析中,pegcetacoplan组第26周时UPCR<1 g/g的患者比例较基线明显增加(基线时8% vs. 第26周时51%),肾病范围内UPCR≥3 g/g的患者比例明显下降(38% vs. 14%),以及eGFR稳定或改善(eGFR下降≤15%)的患者比例高于安慰剂组(68% vs. 61%)。
在69例可评估肾活检样本的患者中,Pegcetacoplan组74%(26/35例)的患者C3免疫荧光染色强度降低≥2级,安慰剂组仅为12%(4/34例),相对风险为6.2(95% CI:2.4~15.9),这一结果直接证实了Pegcetacoplan能够有效减少肾小球内C3沉积,从病理层面改善疾病状态。尽管pegcetacoplan组C3肾小球病组织学指数活动评分的变化数值上高于安慰剂组,但未达到显著差异,这可能与样本量、评分系统的敏感性等因素相关。
在eGFR变化方面,从基线至 26 周,Pegcetacoplan 组的 eGFR 最小二乘均值变化为 - 1.5ml/min/1.73m²(95% CI:-5.9~2.9),而安慰剂组为 - 7.8ml/min/1.73m²(95% CI:-11.6~- 4.0),两组差异为 6.3ml/min/1.73m²(95% CI:0.5~12.1),提示 Pegcetacoplan 能够有效稳定患者的肾功能,延缓 eGFR 下降。
表1. 关键次要终点
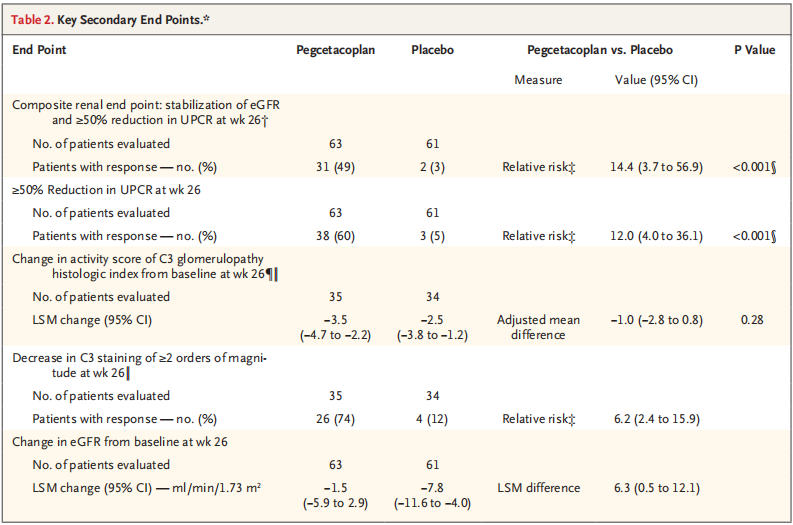
治疗期间,Pegcetacoplan组不良反应发生率与安慰剂组相当,分别为84%、93%,未发生由荚膜细菌引起的严重感染。1例死于新冠肺炎。未发生移植物排斥或丢失。
四、总结
VALIANT临床试验结果证实,Pegcetacoplan作为一种新型C3/C3b双靶点抑制剂,在治疗C3肾小球病和原发性免疫复合物型MPGN方面具有显著的疗效和良好的安全性。治疗26周后,Pegcetacoplan组患者的蛋白尿相对减少68.1%,显著高于安慰剂组,且在复合肾脏终点、肾功能稳定和肾小球C3沉积改善等方面均表现出卓越疗效。该药物的疗效适用于广泛人群,包括青少年、成人、肾移植后复发患者以及正在接受免疫抑制剂治疗的患者。在安全性方面,Pegcetacoplan的不良事件发生率与安慰剂相当,无严重荚膜细菌感染和移植物排斥事件发生,耐受性良好。随着长期研究数据的不断积累,Pegcetacoplan有望成为C3肾小球病和免疫复合物型MPGN治疗的新选择。
参考文献
F. Fakhouri, et al. N Engl J Med. 2025; 393: 2210-20.- 推荐文章
