- 首页 > 正文
肾域华章 | 北大医院周绪杰/张宏团队研究:全维度解析IgA肾病血浆蛋白、免疫细胞及免疫细胞性状的因果因素
发表时间:2026-04-25 13:41:49
编者按:
IgA肾病是全球最常见的原发性肾小球疾病,发病机制尚未完全阐明,部分患者可进展至终末期肾病。近期,北京大学第一医院肾内科周绪杰教授、张宏教授团队在Clinical Journal of the American Society of Nephrology上发表了一篇研究论文(第一作者:Rui-lian You)[1],该研究依托孟德尔随机化全表型关联研究(MR-pheWAS),整合欧洲与亚洲人群血浆蛋白谱、循环免疫细胞及免疫细胞性状数据,结合单细胞转录组、临床样本与动物实验,系统筛选并全面分析了IgA肾病的关键因果分子与免疫特征,为疾病机制阐释、生物标志物开发及靶向治疗提供高等级遗传学证据与转化方向。
IgA肾病以肾小球系膜区IgA免疫复合物沉积为核心病理特征,确诊后20年内约20%~40%患者进展至终末期肾病。当前经典的“四重打击”假说难以完全解释疾病异质性、严重程度差异及完整分子机制。
既往研究提示补体蛋白、免疫细胞亚群紊乱参与IgA肾病发生,但血浆蛋白、免疫细胞类型及细胞性状与疾病间的因果关系仍缺乏严谨遗传学验证。孟德尔随机化全表型关联研究可高效、无偏筛选疾病因果因素,本研究以此为核心方法,开展了跨人群、多维度的因果推断与机制验证。
二、研究结果
(一)血浆蛋白、免疫细胞类型及免疫细胞性状的MR分析
1.血浆蛋白与IgA肾病的因果关联
在欧洲人群中,共纳入代表791种血浆蛋白的797个蛋白定量性状位点(pQTLs);在亚洲人群中,则纳入代表1042种血浆蛋白的1081个pQTLs。
在欧洲人群的MR分析中,补体因子H(CFH)是IgA肾病的重要保护因素(OR=0.54,95%CI:0.45~0.65,P=1.47×10-10)。补体因子H相关蛋白1(CFHR1)(OR=1.21,95%CI:1.12~1.31,P=8.49×10-7)和内质网氨肽酶2(ERAP2)(OR=1.14,95%CI:1.07~1.21,P=7.33×10-6)被确定为IgA肾病的危险因素。MR分析发现52种血浆蛋白与IgA肾病存在提示性因果关联,其中包括32种风险蛋白与20种保护蛋白(如 FCGR2A、FCGR2B及IL7R)(图1);其中45个SNPs通过了Steiger过滤检验。
在亚洲人群中,血浆含吡啶结构域蛋白1(PYDC1)(OR=1.82,95%CI:1.44~2.3,P=6.3×10-7)和防御素α1/1B(DEFA1/DEFA1B)(OR=1.53,95%CI:1.26~1.85,P=1.93×10-5)水平升高与IgA肾病风险显著增加相关;肽酰精氨酸脱亚胺酶4(PADI4)(OR=0.7,95%CI:0.61~0.81,P=1.31×10-6)和核糖核酸酶T2(RNASET2)(OR=0.7,95%CI:0.61~0.81,P=1.31×10-6)则被视为IgA肾病的保护蛋白。共鉴定出56种潜在因果蛋白,其中5种蛋白表现出较强的共定位证据。
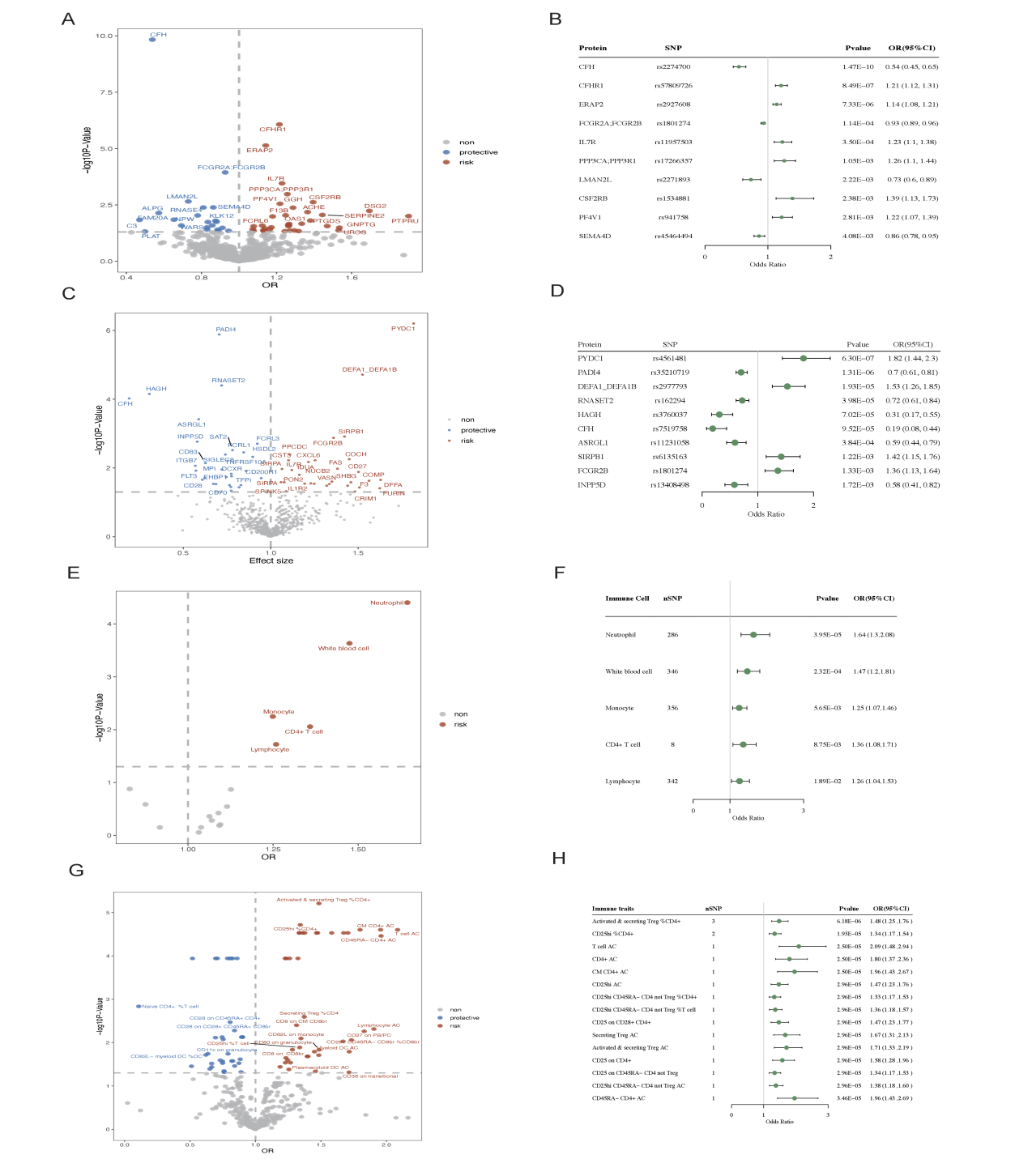
图1. 基于Kiryluk实验室GWAS数据的全表型孟德尔随机化研究(MR-pheWAS)结果
2.免疫细胞及免疫细胞性状的因果关联
在循环免疫细胞类型的MR分析中,共纳入1940个SNPs。中性粒细胞计数、白细胞计数升高与IgA肾病风险升高存在因果关联(图1)。
在免疫细胞性状分析中,筛选出1446个SNPs用于MR评估,共鉴定出15种与IgA肾病存在因果关联的免疫细胞性状。其中最显著的5种风险性状为活化分泌型调节性T细胞占比(%CD4+)、CD25高表达CD4+细胞占比、总T细胞绝对计数、CD4+绝对计数及中央记忆型CD4+绝对计数。此外,共有67种免疫细胞性状被推测与IgA肾病风险相关(图1)。
(二)FinnGen数据库中的MR重复验证分析
5种蛋白(CFH、LMAN2L、GGH、FAM20A和IDUA)被一致证实与IgA肾病存在因果关联(图2)。反向MR分析显示,IgA肾病与血浆蛋白之间不存在显著的反向因果关系。
在FinnGen数据库中,未发现循环免疫细胞类型与IgA肾病存在可重复的因果关联。将本研究结果与Tang等人(2024)[2]的报道进行交集分析,共鉴定出4种共同候选因果分子:CFH、CD200R1、PON2和IL1R2(图2)。
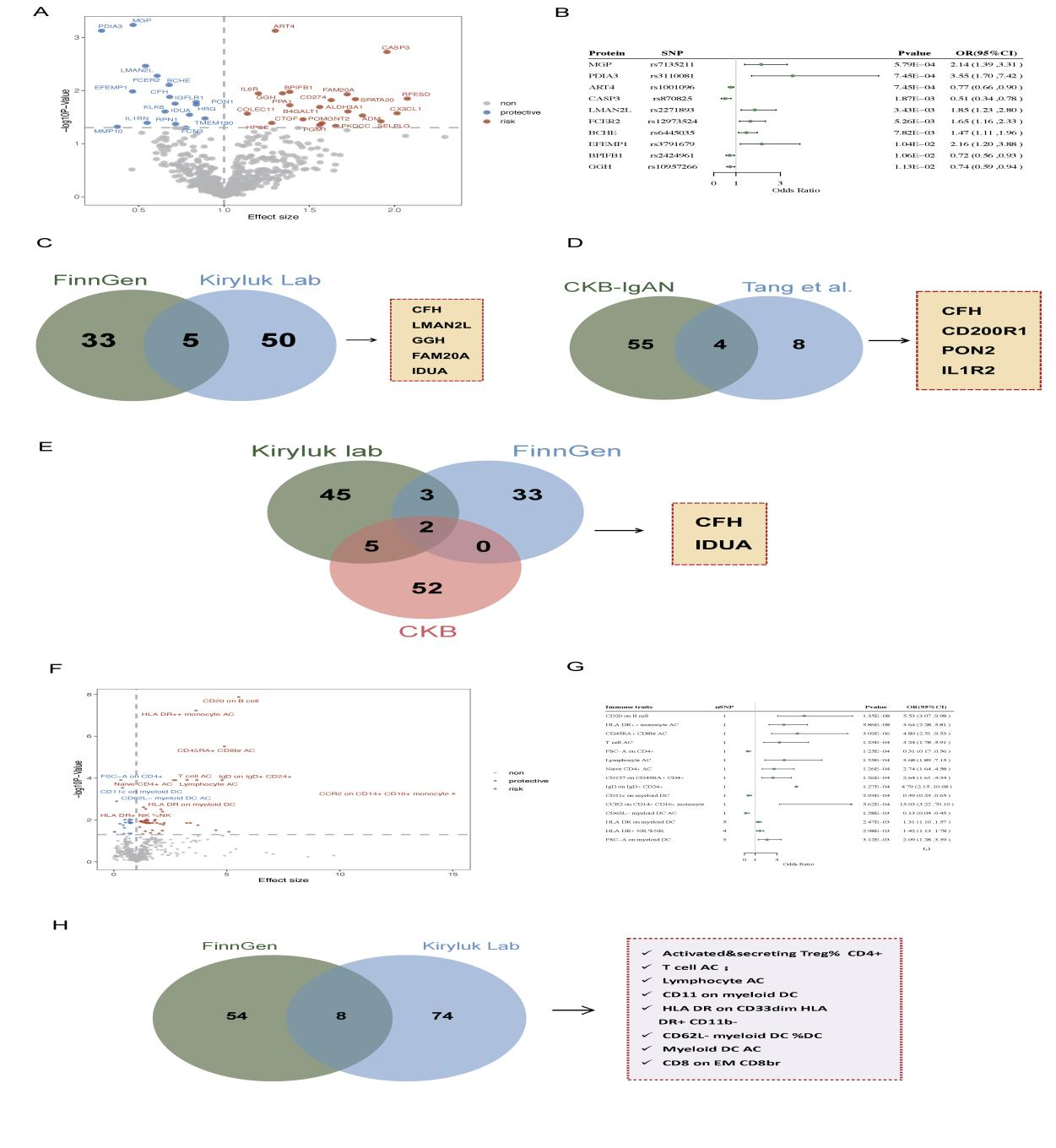
图2. 基于FinnGen数据库进行孟德尔随机化(MR)分析的复制结果
(三)MR后分析
贝叶斯共定位分析强烈提示,6种蛋白(CFH、ERAP2、FAM20A、GGH、IDUA和LMAN2L)与IgA肾病共享相同的因果遗传变异。对合并因果蛋白的通路富集分析显示,这些蛋白主要参与关键生物学过程,包括炎症反应、免疫效应过程,以及补体与凝血级联通路。
(四)蛋白互作网络(PPI)与通路富集分析
这些蛋白构建的PPI网络包含69个节点和159条边。通过CytoHubba分析识别网络中的枢纽蛋白,排名前10的枢纽蛋白为:FCGR2A、FCGR2B、CASP3、GZMB、IL1RN、CCL7、CD274、CD8A、IL7R和IL6R。
欧洲人群的潜在因果蛋白显著富集于炎症反应和补体级联反应通路;
东亚人群的潜在因果蛋白则富集于细胞因子-细胞因子受体互作和淋巴细胞活化调控通路。
(五)药物-基因互作分析
研究发现以下重要关联:
ERAP2:与PI3K/Akt通路抑制剂esculentin在内的5种药物相关;
CFH:与补体C5抑制剂依库珠单抗(eculizumab)及B群脑膜炎球菌疫苗相关;
FCGR2A:与包括重组可溶性人FcγRIIB valziflicept在内的6种药物存在互作。
(六)scRNA-seq分析
对数据集GSE127136的聚类分析,在肾活检组织中鉴定出9种不同细胞群:近端小管细胞、巨噬细胞、亨利袢细胞、T细胞、足细胞、主细胞、内皮细胞、系膜细胞和闰细胞。
LMAN2L在闰细胞中表达水平最高;IL7R主要表达于T细胞;
与对照样本相比,ERAP2在主细胞(P=1.11E-06)和闰细胞(P=3.32E-02)中表达升高;
CFHR1在内皮细胞(P=7.58E-03)和近端小管细胞(P=4.70E-02)中表达更高;
PDIA3在内皮细胞(P=1.90E-04)和亨利袢细胞(P=4.70E-03)中显著上调;
LMAN2L、IDUA、FAM20A和GGH在系膜细胞中显著上调(P值分别为7.00E-03、1.56E-02、4.58E-02、1.53E-02);
LMAN2L、GGH和IDUA在T细胞中表达也显著升高(P值分别为4.01E-02、3.25E-03、3.72E-02)。
针对数据集GSE171314,共对20 570个细胞进行了进一步分析。经聚类及前20个谱系特异性标记基因表达分析,鉴定出14种不同细胞群。
CFH、CFHR1和MGP在系膜细胞中表达显著升高;CFH在内皮细胞(P=0.03)和远端小管细胞中表达也更高;
FAM20A在内皮细胞、单核细胞、损伤近端小管细胞及髓袢升支粗段中表达上调。
(七)在人血浆样本中的验证及动物实验验证
研究纳入40例IgA肾病患者和36例健康对照者。在MR优先筛选的蛋白中,仅IDUA和PYDC1可被可靠定量。ELISA检测显示,IgA肾病患者血浆IDUA、PYDC1水平显著高于健康对照。
生物信息学分析显示:IgA肾病患者组织中PYDC1、NLRP3、IL-1β及caspase1的表达水平显著升高。
动物实验中的表达分析表明,IgA肾病小鼠肾组织Pydc1、Nlrp3、Caspase-1、IL-1β的mRNA表达显著上调,提示NLRP3炎症小体通路活化参与致病。
三、讨论
(一)本研究的机制意义
本研究鉴定出CFH、CFHR1、ERAP2、FAM20A、GGH、IDUA、PYDC1及LMAN2L等多种蛋白,并证实这些蛋白是与IgA肾病发病机制相关的因果蛋白。它们的细胞特异性表达模式为其在疾病机制中的作用提供了额外依据。
补体系统:CFH补证实为保护因素,可能通过调控补体旁路来缓解疾病进展;CFHR1为危险因素,可能通过与CFH竞争补体片段结合位点,降低CFH活性,从而升高疾病风险,这为干预提供了极具前景的靶点。
炎症小体调控:PYDC1是先天免疫的关键负调控因子,可抑制巨噬细胞和粒细胞中细胞因子的释放及炎症小体介导的细胞死亡。本研究结果表明,PYDC1可能通过调控NLRP3通路参与疾病发病机制。
免疫失衡:中性粒细胞和白细胞与更高的疾病风险相关,强调了其在介导炎症中的核心地位。CD4+调节性T细胞亚群异常提示先天与适应性免疫共同参与Ig肾病发病机制。
结合人体样本中的一致结果,可合理推断先天免疫在IgA肾病中发挥重要作用。
(二)种族差异提示
欧洲IgA肾病患者中以补体通路为主导,亚洲人群更富集细胞因子-受体互作与淋巴细胞活化通路,即免疫相关通路在亚洲人群中占主导地位。这为种族分层诊疗提供了理论依据。
(三)治疗的启示
CFH的保护作用支持了补体抑制策略的合理性。FCGR2A作为枢纽基因,其与抗CD20抗体的互作,为将该单克隆抗体疗法重新用于IgA肾病提供了机遇。
(四)与既往研究的对比及本研究优势
与Tang等人的既往研究相比,本研究做出了多项重要新贡献:
1.研究框架拓展
从单一血浆蛋白分析,拓展为联合评估血浆蛋白、免疫细胞类型及免疫细胞性状的整合框架,将蛋白质组信号与特定免疫细胞背景建立关联;
2.种族队列纳入
纳入独立东亚人群队列及种族特异性工具变量,可评估疾病的种族依赖性与共享机制;
3.新因果蛋白鉴定
鉴定出多个在Tang等人研究或其他多组学研究中未被报道为因果蛋白的候选分子(如PYDC1、PADI4、DEFA1/DEFA1B、RNASET2、LMAN2L、GGH、FAM20A、IDUA),并在FinnGen队列中对其中部分进行了重复验证;
4.多层级验证
通过单细胞RNA测序数据集将关键蛋白定位至特定肾脏/免疫细胞亚群,并对IDUA和PYDC1开展人体样本及小鼠模型的实验验证,初步探讨其机制合理性。
Tang等人完成了首个大规模蛋白质组孟德尔随机化筛选,而本研究则整合了跨种族的蛋白质组、免疫学、单细胞及实验数据,进一步细化因果候选分子并提出潜在机制通路
(五)研究局限性
包括:部分工具变量数量有限,残留多效性无法完全排除;免疫细胞指标未在独立队列重复;单细胞样本量较小,需更大队列验证。
四、研究结论
本研究通过跨人群、多维度因果推断与实验验证,证实补体成分、PYDC1及特定CD4+ T细胞亚群是IgA肾病的关键因果因素。上述分子与免疫特征可作为疾病诊断、预后评估的生物标志物,同时为补体抑制、炎症小体调控、免疫细胞靶向等新型治疗策略提供优先研发靶点。
参考文献
[1]You, Rui-lian; et al. Comprehensive Analysis of IgA Nephropathy Causal Factors in Plasma Proteins, Immune Cell Types and Immune Cell Traits. Clinical Journal of the American Society of Nephrology ():10.2215/CJN.0000001022, March 11, 2026. | DOI: 10.2215/CJN.0000001022
[2]Tang C, Chen P, Xu LL, et al. Circulating Proteins and IgA Nephropathy: A Multiancestry Proteome-Wide Mendelian Randomization Study. J Am Soc Nephrol. Aug 1, 2024;35(8):1045-1057. doi:10.1681/ASN.0000000000000379
IgA肾病是全球最常见的原发性肾小球疾病,发病机制尚未完全阐明,部分患者可进展至终末期肾病。近期,北京大学第一医院肾内科周绪杰教授、张宏教授团队在Clinical Journal of the American Society of Nephrology上发表了一篇研究论文(第一作者:Rui-lian You)[1],该研究依托孟德尔随机化全表型关联研究(MR-pheWAS),整合欧洲与亚洲人群血浆蛋白谱、循环免疫细胞及免疫细胞性状数据,结合单细胞转录组、临床样本与动物实验,系统筛选并全面分析了IgA肾病的关键因果分子与免疫特征,为疾病机制阐释、生物标志物开发及靶向治疗提供高等级遗传学证据与转化方向。

IgA肾病以肾小球系膜区IgA免疫复合物沉积为核心病理特征,确诊后20年内约20%~40%患者进展至终末期肾病。当前经典的“四重打击”假说难以完全解释疾病异质性、严重程度差异及完整分子机制。
既往研究提示补体蛋白、免疫细胞亚群紊乱参与IgA肾病发生,但血浆蛋白、免疫细胞类型及细胞性状与疾病间的因果关系仍缺乏严谨遗传学验证。孟德尔随机化全表型关联研究可高效、无偏筛选疾病因果因素,本研究以此为核心方法,开展了跨人群、多维度的因果推断与机制验证。
二、研究结果
(一)血浆蛋白、免疫细胞类型及免疫细胞性状的MR分析
1.血浆蛋白与IgA肾病的因果关联
在欧洲人群中,共纳入代表791种血浆蛋白的797个蛋白定量性状位点(pQTLs);在亚洲人群中,则纳入代表1042种血浆蛋白的1081个pQTLs。
在欧洲人群的MR分析中,补体因子H(CFH)是IgA肾病的重要保护因素(OR=0.54,95%CI:0.45~0.65,P=1.47×10-10)。补体因子H相关蛋白1(CFHR1)(OR=1.21,95%CI:1.12~1.31,P=8.49×10-7)和内质网氨肽酶2(ERAP2)(OR=1.14,95%CI:1.07~1.21,P=7.33×10-6)被确定为IgA肾病的危险因素。MR分析发现52种血浆蛋白与IgA肾病存在提示性因果关联,其中包括32种风险蛋白与20种保护蛋白(如 FCGR2A、FCGR2B及IL7R)(图1);其中45个SNPs通过了Steiger过滤检验。
在亚洲人群中,血浆含吡啶结构域蛋白1(PYDC1)(OR=1.82,95%CI:1.44~2.3,P=6.3×10-7)和防御素α1/1B(DEFA1/DEFA1B)(OR=1.53,95%CI:1.26~1.85,P=1.93×10-5)水平升高与IgA肾病风险显著增加相关;肽酰精氨酸脱亚胺酶4(PADI4)(OR=0.7,95%CI:0.61~0.81,P=1.31×10-6)和核糖核酸酶T2(RNASET2)(OR=0.7,95%CI:0.61~0.81,P=1.31×10-6)则被视为IgA肾病的保护蛋白。共鉴定出56种潜在因果蛋白,其中5种蛋白表现出较强的共定位证据。

图1. 基于Kiryluk实验室GWAS数据的全表型孟德尔随机化研究(MR-pheWAS)结果
2.免疫细胞及免疫细胞性状的因果关联
在循环免疫细胞类型的MR分析中,共纳入1940个SNPs。中性粒细胞计数、白细胞计数升高与IgA肾病风险升高存在因果关联(图1)。
在免疫细胞性状分析中,筛选出1446个SNPs用于MR评估,共鉴定出15种与IgA肾病存在因果关联的免疫细胞性状。其中最显著的5种风险性状为活化分泌型调节性T细胞占比(%CD4+)、CD25高表达CD4+细胞占比、总T细胞绝对计数、CD4+绝对计数及中央记忆型CD4+绝对计数。此外,共有67种免疫细胞性状被推测与IgA肾病风险相关(图1)。
(二)FinnGen数据库中的MR重复验证分析
5种蛋白(CFH、LMAN2L、GGH、FAM20A和IDUA)被一致证实与IgA肾病存在因果关联(图2)。反向MR分析显示,IgA肾病与血浆蛋白之间不存在显著的反向因果关系。
在FinnGen数据库中,未发现循环免疫细胞类型与IgA肾病存在可重复的因果关联。将本研究结果与Tang等人(2024)[2]的报道进行交集分析,共鉴定出4种共同候选因果分子:CFH、CD200R1、PON2和IL1R2(图2)。

图2. 基于FinnGen数据库进行孟德尔随机化(MR)分析的复制结果
(三)MR后分析
贝叶斯共定位分析强烈提示,6种蛋白(CFH、ERAP2、FAM20A、GGH、IDUA和LMAN2L)与IgA肾病共享相同的因果遗传变异。对合并因果蛋白的通路富集分析显示,这些蛋白主要参与关键生物学过程,包括炎症反应、免疫效应过程,以及补体与凝血级联通路。
(四)蛋白互作网络(PPI)与通路富集分析
这些蛋白构建的PPI网络包含69个节点和159条边。通过CytoHubba分析识别网络中的枢纽蛋白,排名前10的枢纽蛋白为:FCGR2A、FCGR2B、CASP3、GZMB、IL1RN、CCL7、CD274、CD8A、IL7R和IL6R。
欧洲人群的潜在因果蛋白显著富集于炎症反应和补体级联反应通路;
东亚人群的潜在因果蛋白则富集于细胞因子-细胞因子受体互作和淋巴细胞活化调控通路。
(五)药物-基因互作分析
研究发现以下重要关联:
ERAP2:与PI3K/Akt通路抑制剂esculentin在内的5种药物相关;
CFH:与补体C5抑制剂依库珠单抗(eculizumab)及B群脑膜炎球菌疫苗相关;
FCGR2A:与包括重组可溶性人FcγRIIB valziflicept在内的6种药物存在互作。
(六)scRNA-seq分析
对数据集GSE127136的聚类分析,在肾活检组织中鉴定出9种不同细胞群:近端小管细胞、巨噬细胞、亨利袢细胞、T细胞、足细胞、主细胞、内皮细胞、系膜细胞和闰细胞。
LMAN2L在闰细胞中表达水平最高;IL7R主要表达于T细胞;
与对照样本相比,ERAP2在主细胞(P=1.11E-06)和闰细胞(P=3.32E-02)中表达升高;
CFHR1在内皮细胞(P=7.58E-03)和近端小管细胞(P=4.70E-02)中表达更高;
PDIA3在内皮细胞(P=1.90E-04)和亨利袢细胞(P=4.70E-03)中显著上调;
LMAN2L、IDUA、FAM20A和GGH在系膜细胞中显著上调(P值分别为7.00E-03、1.56E-02、4.58E-02、1.53E-02);
LMAN2L、GGH和IDUA在T细胞中表达也显著升高(P值分别为4.01E-02、3.25E-03、3.72E-02)。
针对数据集GSE171314,共对20 570个细胞进行了进一步分析。经聚类及前20个谱系特异性标记基因表达分析,鉴定出14种不同细胞群。
CFH、CFHR1和MGP在系膜细胞中表达显著升高;CFH在内皮细胞(P=0.03)和远端小管细胞中表达也更高;
FAM20A在内皮细胞、单核细胞、损伤近端小管细胞及髓袢升支粗段中表达上调。
(七)在人血浆样本中的验证及动物实验验证
研究纳入40例IgA肾病患者和36例健康对照者。在MR优先筛选的蛋白中,仅IDUA和PYDC1可被可靠定量。ELISA检测显示,IgA肾病患者血浆IDUA、PYDC1水平显著高于健康对照。
生物信息学分析显示:IgA肾病患者组织中PYDC1、NLRP3、IL-1β及caspase1的表达水平显著升高。
动物实验中的表达分析表明,IgA肾病小鼠肾组织Pydc1、Nlrp3、Caspase-1、IL-1β的mRNA表达显著上调,提示NLRP3炎症小体通路活化参与致病。
三、讨论
(一)本研究的机制意义
本研究鉴定出CFH、CFHR1、ERAP2、FAM20A、GGH、IDUA、PYDC1及LMAN2L等多种蛋白,并证实这些蛋白是与IgA肾病发病机制相关的因果蛋白。它们的细胞特异性表达模式为其在疾病机制中的作用提供了额外依据。
补体系统:CFH补证实为保护因素,可能通过调控补体旁路来缓解疾病进展;CFHR1为危险因素,可能通过与CFH竞争补体片段结合位点,降低CFH活性,从而升高疾病风险,这为干预提供了极具前景的靶点。
炎症小体调控:PYDC1是先天免疫的关键负调控因子,可抑制巨噬细胞和粒细胞中细胞因子的释放及炎症小体介导的细胞死亡。本研究结果表明,PYDC1可能通过调控NLRP3通路参与疾病发病机制。
免疫失衡:中性粒细胞和白细胞与更高的疾病风险相关,强调了其在介导炎症中的核心地位。CD4+调节性T细胞亚群异常提示先天与适应性免疫共同参与Ig肾病发病机制。
结合人体样本中的一致结果,可合理推断先天免疫在IgA肾病中发挥重要作用。
(二)种族差异提示
欧洲IgA肾病患者中以补体通路为主导,亚洲人群更富集细胞因子-受体互作与淋巴细胞活化通路,即免疫相关通路在亚洲人群中占主导地位。这为种族分层诊疗提供了理论依据。
(三)治疗的启示
CFH的保护作用支持了补体抑制策略的合理性。FCGR2A作为枢纽基因,其与抗CD20抗体的互作,为将该单克隆抗体疗法重新用于IgA肾病提供了机遇。
(四)与既往研究的对比及本研究优势
与Tang等人的既往研究相比,本研究做出了多项重要新贡献:
1.研究框架拓展
从单一血浆蛋白分析,拓展为联合评估血浆蛋白、免疫细胞类型及免疫细胞性状的整合框架,将蛋白质组信号与特定免疫细胞背景建立关联;
2.种族队列纳入
纳入独立东亚人群队列及种族特异性工具变量,可评估疾病的种族依赖性与共享机制;
3.新因果蛋白鉴定
鉴定出多个在Tang等人研究或其他多组学研究中未被报道为因果蛋白的候选分子(如PYDC1、PADI4、DEFA1/DEFA1B、RNASET2、LMAN2L、GGH、FAM20A、IDUA),并在FinnGen队列中对其中部分进行了重复验证;
4.多层级验证
通过单细胞RNA测序数据集将关键蛋白定位至特定肾脏/免疫细胞亚群,并对IDUA和PYDC1开展人体样本及小鼠模型的实验验证,初步探讨其机制合理性。
Tang等人完成了首个大规模蛋白质组孟德尔随机化筛选,而本研究则整合了跨种族的蛋白质组、免疫学、单细胞及实验数据,进一步细化因果候选分子并提出潜在机制通路
(五)研究局限性
包括:部分工具变量数量有限,残留多效性无法完全排除;免疫细胞指标未在独立队列重复;单细胞样本量较小,需更大队列验证。
四、研究结论
本研究通过跨人群、多维度因果推断与实验验证,证实补体成分、PYDC1及特定CD4+ T细胞亚群是IgA肾病的关键因果因素。上述分子与免疫特征可作为疾病诊断、预后评估的生物标志物,同时为补体抑制、炎症小体调控、免疫细胞靶向等新型治疗策略提供优先研发靶点。
参考文献
[1]You, Rui-lian; et al. Comprehensive Analysis of IgA Nephropathy Causal Factors in Plasma Proteins, Immune Cell Types and Immune Cell Traits. Clinical Journal of the American Society of Nephrology ():10.2215/CJN.0000001022, March 11, 2026. | DOI: 10.2215/CJN.0000001022
[2]Tang C, Chen P, Xu LL, et al. Circulating Proteins and IgA Nephropathy: A Multiancestry Proteome-Wide Mendelian Randomization Study. J Am Soc Nephrol. Aug 1, 2024;35(8):1045-1057. doi:10.1681/ASN.0000000000000379
- 推荐文章
ERA专家访谈丨顾乐怡教授:补体相关肾病治疗格局的范式跃迁,口服盐酸兰诺可泮治疗lgA肾病12周尿蛋白达标率高达40%
ERA中国之声 | 东南大学肾内科团队多项研究揭秘急性肾损伤全新作用机制
ERA中国之声丨UMOD H36Y突变如何通过代谢重编程加速肾小管衰老?
ERA专家访谈丨马坤岭教授:补体靶向治疗的“靶点前移”与“近端阻断”,口服盐酸兰诺可泮治疗IgA肾病12周尿蛋白达标率高达40%
ERA中国之声 | 重磅临床发现:抑酸药使用量与腹膜透析患者骨折风险呈梯度相关
ERA中国之声丨Dotinurad通过Nrf2介导的线粒体质量控制发挥直接肾小管保护作用,且该效应不依赖URAT1抑制
2026 ERA研究揭示从认知革新到实践破局的全球图景
江苏省中医院双项成果亮相ERA大会:靶向CTRP1-SGLT2与O-GlcNAc-FAO代谢记忆轴,破解糖尿病肾病发病新机制
ERA专家访谈丨路万虹教授:补体抑制剂助力IgA肾病早期、精准缓解,口服盐酸兰诺可泮治疗12周尿蛋白达标率高达40%
ERA中外专家研讨|聚焦IgA肾病前沿进展,解析临床对因治疗新看点
ERA 2026 | Crovalimab治疗成人及儿童aHUS:COMMUTE-a与COMMUTE-p Ⅲ期研究均达主要终点
ERA 2026 | 12周尿蛋白达标率高达40%,UPCR降幅51.8%!口服补体抑制剂盐酸兰诺可泮IgAN Ⅱ期高影响力研究数据全球首发
AI时代下聚焦批判性思维、技术创新与人文关怀!第63届ERA圆满闭幕,下一站鹿特丹
会议报道:从临床痛点出发,探寻IgA肾病长期管理最优解丨“肾英无界・中外IgA肾病学术前沿对话”成都站圆满收官
ERA 中国之声 | 华西医院30余项研究入选大会交流,4项研究上榜“青年作者优秀摘要”
全球首个APRIL靶向生物制剂斯贝利单抗在华获批,用于治疗IgA肾病
ERA 2026十佳摘要丨已用SGLT2i的2型糖尿病患者,联用GLP-1RA可再降27%肾病进展风险,全肾功能区间获益一致
ERA 2026前沿:三大新机制破局,CKD诊疗格局迎关键转折
ERA 2026重磅研究 | ALIGN试验2.5年eGFR结果:阿曲生坦治疗IgA肾病可显著、持续延缓肾功能下降
ERA 2026|9个月应答不佳仍具长期肾保护,NefIgArd亚组分析为IgA肾病对因治疗决策提供重磅证据【锁定今晚直播,洞悉2026 KDIGO更新要点】
ERA2026重磅研究丨FLOW试验最新数据:司美格鲁肽改善慢性肾脏病合并2型糖尿病患者生活质量
ERA 2026前沿 | 突破诊疗壁垒,迈向全程管理:构建以SGLT2i为核心的CKD早筛早诊早治新格局
ERA 2026十佳摘要丨中国台湾长庚医院单细胞图谱揭秘多囊肾发病源头,锁定全新靶向治疗靶点
ERA 2026丨突破9个月疗程,布地奈德肠溶胶囊长程治疗,为IgA肾病患者带来持久肾功能保护
ERA 2026 | 香港大学研究揭示:脂联素经线粒体重塑途径改善糖胖病相关肾损伤
杨淑敏教授:被忽视的20%——内分泌性高血压筛查专家共识解读
ERA 2026格拉斯哥正式启幕!以开放思维锚定肾病未来,《柳叶刀》重磅数据敲响CKD全球防控警钟
ERA 2026重磅丨IgA肾病尽早对因治疗:锚定蛋白尿≥0.5 g/d肾病进展风险人群,早用早达标、护肾更及时
ERA 2026前沿 | 突破“5.0时代”,迈向长期管理:真实世界研究驱动高钾血症诊疗变革
血液透析患者高血压管理的十个核心建议:基于ERA共识的临床实践指导
陈莉明教授:糖尿病慢性肾脏病的修正策略——从流行病学到多靶点治疗 | PUDF 2026
会议报道:聚焦临床痛点 共谋全程管理丨“肾英无界”中外IgA肾病学术前沿对话北京站成功举办
从AI到异种移植:ERA 2026最值得关注的五大未来技术
CIC 2026 | 任景怡教授:醛固酮介导心衰进展,nsMRA带来全新突破——从机制到临床的精准制导
ERA 2026三大临床试验专场:IgA肾病、CKD与罕见肾病治疗格局或将迎来新变化
何娅妮教授:糖尿病肾病治疗策略新进展——GDMT四大支柱筑牢心肾防线
Vadadustat(每周三次)对比不同基线剂量的甲氧基聚乙二醇促红素β治疗透析依赖型慢性肾病贫血患者的疗效与安全性分析
CCBPC 2026|涂晓文教授:血浆净化技术及其临床应用新进展
ERA 2026开幕在即!“Open your mind”背后,肾脏病学正在发生哪些改变?
ERA 2026|布地奈德肠溶胶囊23项全新研究闪耀登场,多维夯实对因、尽早、长期治疗临床证据体系
“生命之河”堵塞,肾脏告急!警惕“堵”出来的肾病——梗阻性肾病
中美双队列研究:不合并ASCVD的CKD患者,他汀治疗降低死亡风险26%~39%
会议报道:开放视野 探索前沿丨“肾英无界”中外IgA肾病学术前沿对话上海站圆满落幕
学术纵横丨常染色体显性多囊肾病(ADPKD)最新学术进展:风险评估、人群特征与创新药物探索
病例分享 | 血糖不高却频发酮症!这例糖尿病背后藏着双重隐秘病因,解密糖尿病胃轻瘫与肾糖阈减低的恶性循环
张宏教授:立足机制,解析B细胞靶向治疗IgA肾病的最新进展
肾移植术后膜性肾病研究:首个覆盖复发、未复发与新发类型的系统回顾与Meta分析核心结论与临床启示
压力与心血管疾病:成人期的隐形杀手
周晓霜教授:临床常规代谢指标与IgA肾病肾功能及病理损伤程度显著相关
非典型溶血尿毒综合征(aHUS)多学科诊疗专家共识要点,补体抑制剂为一线首选治疗
崔兆强教授:从“单纯降压”到“综合获益”——深度解析高血压治疗新趋势
以问破局 以共识远——《IgA肾病临床实践60问(2026版)》重磅发布,直击临床痛点,全面解锁IgA肾病对因治疗
开放思维,共探肾学前沿——第63届ERA大会即将启幕!26项中国研究入选最佳/优秀摘要
孙宁玲教授:破局“高容量”——从评估到干预,高血压管理如何走出困境?
CCBPC 2026|马坤岭教授:肠道菌群介导DKD肾损伤机制及转化应用新进展
