- 首页 > 正文
每月1针,UPCR降幅可达62%!WCN 2026公布IgA肾病中国队列数据
发表时间:2026-04-25 18:08:42
2026年WCN大会上,斯贝利单抗中国队列数据正式发布:尿蛋白降幅约62%,与全球主队列高度一致,为中国IgA肾病患者带来新希望。
IgA肾病是我国最常见的原发性肾小球疾病,约占全部肾活检病例的54.3%,是我国慢性肾脏病(CKD)和终末期肾病(ESKD)的主要原因之一,高达40%的IgA肾病患者在诊断后20年内发展为ESKD[1]。该病的病理特征为含半乳糖缺陷型免疫球蛋白 A1 (Gd-IgA1) 的免疫复合物在肾小球系膜区沉积[2]。 其中,增殖诱导配体 (APRIL) 可在这一过程中发挥关键作用,可促进Gd-IgA1生成,进而可能引发免疫复合物形成与肾脏损伤[3],严重影响患者的生活质量,提示该病具有较高的进展风险,以及临床对新型靶向治疗的迫切需求。
2026年世界肾脏病学大会(WCN 2026)上,全球首个选择性APRIL抑制剂斯贝利单抗(Sibeprenlimab)公布了中国队列的中期分析结果,数据显示其在降低尿蛋白、诱导血尿缓解等方面表现优异,与全球主队列结果高度一致,为中国IgA肾病患者提供了新的治疗希望。
全球III期VISIONARY研究:NEJM发表的51.2%尿蛋白降幅奠定疗效基础
2025年11月发表于NEJM的III期VISIONARY试验全球主队列中期分析首次证实了斯贝利单抗在IgA肾病治疗中的疗效与安全性[4]。该研究是一项随机、双盲、安慰剂对照试验,旨在评估斯贝利单抗治疗IgA肾病成人患者24个月的有效性与安全性[4]。
全球主队列预设中期分析显示,治疗9个月时,斯贝利单抗组经安慰剂校正的24小时尿蛋白肌酐比值(uPCR-24h)降幅达51.2%(96.5% CI, 42.9-58.2; P<0.001),达到主要终点[4]。同时,斯贝利单抗强效抑制APRIL水平(抑制率95.8%),并显著降低Gd-IgA1水平(降幅67.1%)[4]。安全性方面,斯贝利单抗治疗组不良事件发生率与安慰剂组相当,未发现新的安全性信号[5]。
中国队列数据发布:疗效显著,与全球结果高度一致
在本次WCN 2026上,北京大学第一医院张宏教授牵头报告的III期VISIONARY试验[4]中国队列中期分析结果引发广泛关注。研究纳入42例中国IgA肾病患者,其中25例接受斯贝利单抗治疗,17例接受安慰剂。截至中期分析数据截止日,所有患者均完成了9个月的uPCR-24h评估。结果显示:
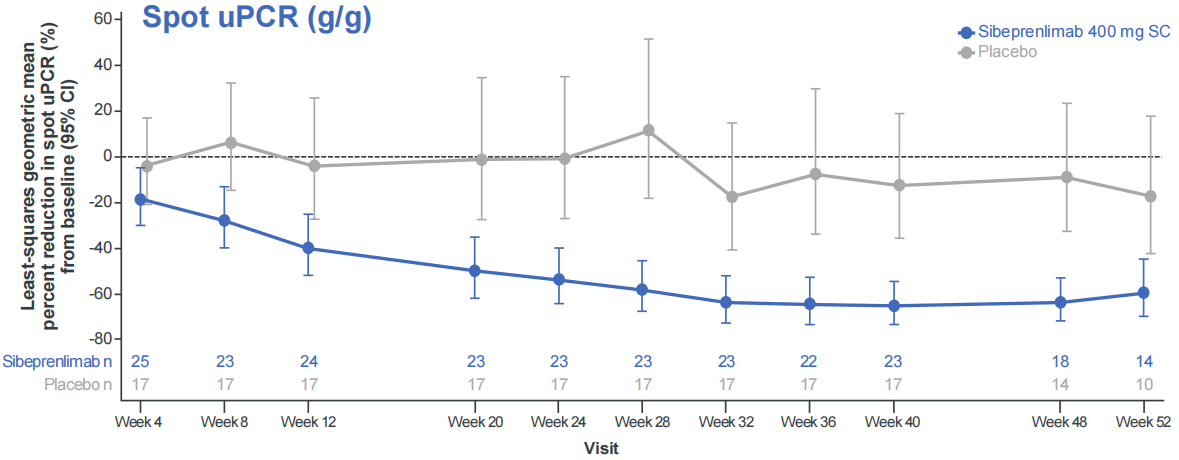
尿蛋白显著下降:治疗9个月时,经安慰剂校正的uPCR-24h降幅约为62%(图1),具有明确的临床意义,是目前中国IgA肾病患者中,III期临床研究uPCR-24h降幅效果最好的一项数据。

图1 第9个月时uPCR-24h较基线的变化:中国大陆队列与全球队列
A) 中国大陆队列中,斯贝利单抗组(n=25)uPCR-24h下降63.1%,安慰剂组(n=17)下降3.1%,安慰剂校正后的治疗效果为61.9%(95% CI: 43.2%-74.5%)。B) 全球队列中,斯贝利单抗组(n=152)下降50.2%,安慰剂组(n=168)升高2.1%,安慰剂校正后的治疗效果为51.2%(96.5% CI: 42.9%-58.2%,P<0.0001)
强效抑制APRIL:斯贝利单抗治疗组APRIL水平抑制率约为96%,同时显著降低Gd-IgA1等致病性生物标志物水平(图2)。
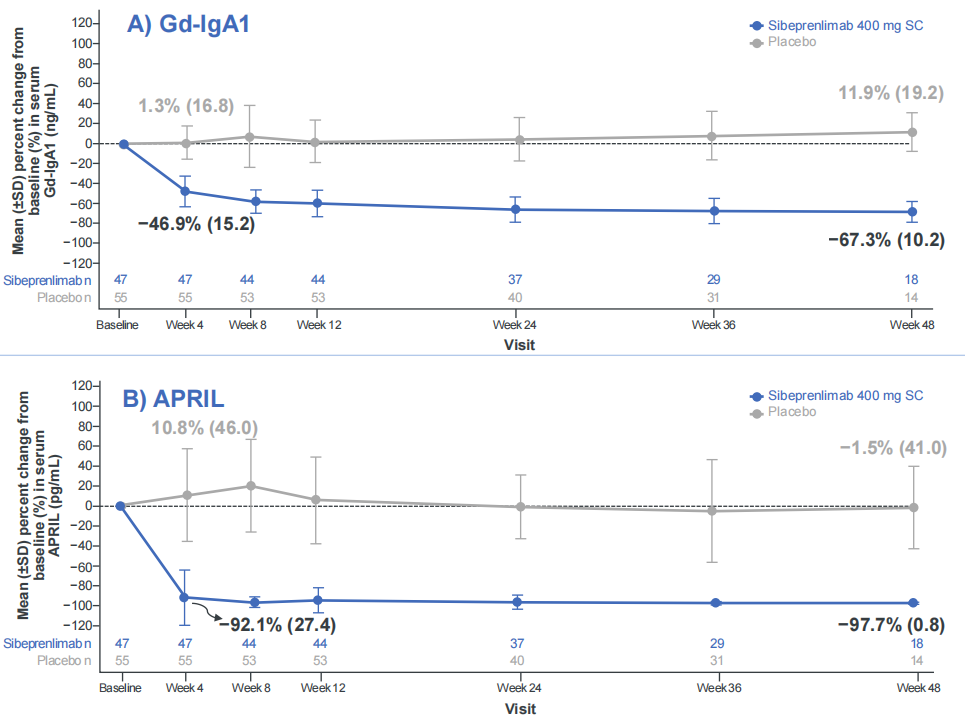
图2 Gd-IgA1与APRIL水平较基线的平均百分比变化(中国大陆队列)
血尿缓解率更高:斯贝利单抗治疗组患者镜下血尿转阴率更高,缓解速度更快。
安全性良好:未报告治疗相关严重不良事件,安全性特征与安慰剂相当。
上述结果与全球主队列公布的数据高度一致[4],证实斯贝利单抗的疗效与安全性在中国人群中同样适用。值得注意的是,中国队列的尿蛋白降幅数值上略高于全球主队列,这可能与基线特征、人群差异或样本量有关,但总体疗效趋势高度吻合(图3)。
镜下血尿缓解新证据:82.5%患者48周转阴,中位缓解时间仅9周
本次大会还公布了VISIONARY试验[4]关于镜下血尿影响的补充分析。镜下血尿是IgA肾病患者肾小球活动性损伤的标志性特征,与疾病进展风险密切相关。随着时间的推移,持续性镜下血尿逐渐被认定为疾病活动的标志物及疾病进展的风险因素,而血尿缓解则预示着肾脏结局的改善[5]。
分析基于III期VISIONARY试验48周的数据,评估斯贝利单抗对镜下血尿的影响。在基线伴镜下血尿的全球患者中,治疗至48周时:
斯贝利单抗治疗组82.5%的患者(33/40)镜下血尿转阴[红细胞≤5个/高倍视野(HPF)],而安慰剂组仅为52.6%(51/97);
采用Kaplan-Meier法估算,48周内斯贝利单抗治疗组血尿缓解概率为90.9%,显著高于安慰剂组的68.1%;
中位缓解时间:斯贝利单抗组为9周,安慰剂组为24周。
这些数据进一步支持APRIL抑制在控制免疫介导肾损伤中的关键作用,也为临床提供了除尿蛋白外的另一疗效评估维度。同时,斯贝利单抗治疗组患者的蛋白尿缓解率更高,与血尿缓解结果互为补充。
VISOR试验进行中:重复肾活检将直接评估肾组织学改变
为进一步明确斯贝利单抗对肾脏组织学的影响,研究者已启动VISOR试验[6]。这是一项IIb期、多中心、开放标签、重复肾活检、单臂临床试验,旨在直接评估APRIL抑制对IgA肾病成人患者肾脏组织病理学的影响。开展VISOR试验的目的是为了进一步明确全球VISIONARY研究项目中观察到的临床改善是否能转化为肾脏内可量化的组织学改变,从而帮助阐明APRIL抑制的作用机制与改善疾病进程的潜力。
研究计划纳入约50例患者,接受最长2年的斯贝利单抗治疗,方案规定的肾活检分别在基线、52周时进行,持续接受治疗的患者将在104周时再次接受肾活检。探索性分析将额外评估疾病活动度相关的组织学与细胞标志物,包括肾小球IgA沉积变化;MEST-C评分动态演变;免疫细胞浸润、补体沉积;空间转录组学特征。
该研究是首个评估斯贝利单抗治疗后肾组织学变化的临床试验,有望为APRIL抑制的机制与疗效提供组织层面的直接证据,超越临床生物标志物,提供组织层面的疾病活动度评估指标。
专家述评
作为III期VISIONARY试验学术指导委员会成员和中国队列的主要研究者,张宏教授表示:“IgA肾病在中国造成了沉重的疾病负担,大量患者仍面临进展为肾衰竭的风险。尿蛋白水平升高与患者更快进展为ESKD密切相关。在该研究的中国队列中,斯贝利单抗可显著降低患者尿蛋白水平,降幅具有明确临床意义,与全球主队列的观察结果高度一致。”
张宏教授进一步讲道:“本次WCN上公布的补充分析结果,包括血尿相关研究发现以及正在开展的VISOR试验,进一步深化了我们对IgA肾病领域中APRIL抑制的认知。血尿作为疾病活动度的标志,其缓解速度与程度为我们提供了新的疗效评估维度,也为 IgA肾病的精准治疗提供了更全面的循证依据。同时,我们也期待这一靶向治疗未来能够惠及更多的中国患者。”
结语
斯贝利单抗作为全球首个选择性抑制APRIL的IgA肾病治疗药物,在III期VISIONARY试验中展现出优异的疗效与安全性。全球主队列数据的发表,为其临床应用奠定了坚实的循证基础。中国队列数据与全球结果高度一致,为其在中国人群中的应用提供了直接证据。随着血尿缓解、生物标志物变化及肾脏组织学数据的不断积累,APRIL抑制有望成为IgA肾病治疗的新基石,为众多面临疾病进展风险的IgA肾病患者带来新的希望。
专家简介

张宏教授
北京大学第一医院肾内科主任,北京大学肾脏疾病研究所副所长
主任医师、教授、博士/博士后导师
日本冈山大学医学部医学博士;美国耶鲁大学医学院遗传系客座研究员
国家自然科学基金委杰出青年/教育部新世纪优秀人才/中华医学专项人才
国际肾脏病学会教育大使;国之名医-优秀风范奖获得者
国际肾脏病学会(ISN)东北亚委员会委员;ISN继续教育顾问委员会委员
ISN临床试验促进委员会委员;ISN临床研究委员会委员
国际IgA肾病合作组(IIgANN)专家委员会委员
中国IgA肾病合作组(IIgANN-China) 主席
中国医师协会循证医学专委会常委;北京医学会肾脏病学分会副主委
SCI论文260余篇,代表性论文在JAMA、KI、JASN、Nat Genet等发表
参考文献:
[1]中国医药卫生文化协会肾病与血液净化专业委员会.原发性IgA肾病管理和治疗中国专家共识[J].中华肾病研究电子杂志,2024, 13 (1): 1-28.
[2]Wang Gangan , Zheng Ke , Li Xuemei. Researches progress on pathogenesis of IgA nephropathy[J]. Chinese Journal of Nephrology, 2024, 40(3): 225-230.
[3]Suzuki H, et al. Increased APRIL Expression Induces IgA1 Aberrant Glycosylation in IgA Nephropathy [J]. Medicine, 2016, 95 (11): e3099.
[4] Perkovic V, Trimarchi H, Tesar V, et al. Sibeprenlimab in IgA nephropathy — interim analysis of a phase 3 trial[J]. N Engl J Med, 2025, 393(12): 1123-1134.
[5]Floege J, Fervenza FC, Coppo R. Microscopic hematuria in IgA nephropathy: a biomarker of disease activity[J]. Clinical Kidney Journal, 2026, 19(2): sfag003.
[6] VISOR Study Group. VISOR: A phase 2b, open-label, repeat kidney biopsy trial to evaluate the effects of sibeprenlimab on renal histology in patients with IgA nephropathy [J]. Nephrol Dial Transplant, 2026, 41(Suppl 1): i123-i124.
IgA肾病是我国最常见的原发性肾小球疾病,约占全部肾活检病例的54.3%,是我国慢性肾脏病(CKD)和终末期肾病(ESKD)的主要原因之一,高达40%的IgA肾病患者在诊断后20年内发展为ESKD[1]。该病的病理特征为含半乳糖缺陷型免疫球蛋白 A1 (Gd-IgA1) 的免疫复合物在肾小球系膜区沉积[2]。 其中,增殖诱导配体 (APRIL) 可在这一过程中发挥关键作用,可促进Gd-IgA1生成,进而可能引发免疫复合物形成与肾脏损伤[3],严重影响患者的生活质量,提示该病具有较高的进展风险,以及临床对新型靶向治疗的迫切需求。
2026年世界肾脏病学大会(WCN 2026)上,全球首个选择性APRIL抑制剂斯贝利单抗(Sibeprenlimab)公布了中国队列的中期分析结果,数据显示其在降低尿蛋白、诱导血尿缓解等方面表现优异,与全球主队列结果高度一致,为中国IgA肾病患者提供了新的治疗希望。
全球III期VISIONARY研究:NEJM发表的51.2%尿蛋白降幅奠定疗效基础
2025年11月发表于NEJM的III期VISIONARY试验全球主队列中期分析首次证实了斯贝利单抗在IgA肾病治疗中的疗效与安全性[4]。该研究是一项随机、双盲、安慰剂对照试验,旨在评估斯贝利单抗治疗IgA肾病成人患者24个月的有效性与安全性[4]。
全球主队列预设中期分析显示,治疗9个月时,斯贝利单抗组经安慰剂校正的24小时尿蛋白肌酐比值(uPCR-24h)降幅达51.2%(96.5% CI, 42.9-58.2; P<0.001),达到主要终点[4]。同时,斯贝利单抗强效抑制APRIL水平(抑制率95.8%),并显著降低Gd-IgA1水平(降幅67.1%)[4]。安全性方面,斯贝利单抗治疗组不良事件发生率与安慰剂组相当,未发现新的安全性信号[5]。
中国队列数据发布:疗效显著,与全球结果高度一致
在本次WCN 2026上,北京大学第一医院张宏教授牵头报告的III期VISIONARY试验[4]中国队列中期分析结果引发广泛关注。研究纳入42例中国IgA肾病患者,其中25例接受斯贝利单抗治疗,17例接受安慰剂。截至中期分析数据截止日,所有患者均完成了9个月的uPCR-24h评估。结果显示:
尿蛋白显著下降:治疗9个月时,经安慰剂校正的uPCR-24h降幅约为62%(图1),具有明确的临床意义,是目前中国IgA肾病患者中,III期临床研究uPCR-24h降幅效果最好的一项数据。

图1 第9个月时uPCR-24h较基线的变化:中国大陆队列与全球队列
A) 中国大陆队列中,斯贝利单抗组(n=25)uPCR-24h下降63.1%,安慰剂组(n=17)下降3.1%,安慰剂校正后的治疗效果为61.9%(95% CI: 43.2%-74.5%)。B) 全球队列中,斯贝利单抗组(n=152)下降50.2%,安慰剂组(n=168)升高2.1%,安慰剂校正后的治疗效果为51.2%(96.5% CI: 42.9%-58.2%,P<0.0001)
强效抑制APRIL:斯贝利单抗治疗组APRIL水平抑制率约为96%,同时显著降低Gd-IgA1等致病性生物标志物水平(图2)。

图2 Gd-IgA1与APRIL水平较基线的平均百分比变化(中国大陆队列)
血尿缓解率更高:斯贝利单抗治疗组患者镜下血尿转阴率更高,缓解速度更快。
安全性良好:未报告治疗相关严重不良事件,安全性特征与安慰剂相当。
上述结果与全球主队列公布的数据高度一致[4],证实斯贝利单抗的疗效与安全性在中国人群中同样适用。值得注意的是,中国队列的尿蛋白降幅数值上略高于全球主队列,这可能与基线特征、人群差异或样本量有关,但总体疗效趋势高度吻合(图3)。
镜下血尿缓解新证据:82.5%患者48周转阴,中位缓解时间仅9周
本次大会还公布了VISIONARY试验[4]关于镜下血尿影响的补充分析。镜下血尿是IgA肾病患者肾小球活动性损伤的标志性特征,与疾病进展风险密切相关。随着时间的推移,持续性镜下血尿逐渐被认定为疾病活动的标志物及疾病进展的风险因素,而血尿缓解则预示着肾脏结局的改善[5]。
分析基于III期VISIONARY试验48周的数据,评估斯贝利单抗对镜下血尿的影响。在基线伴镜下血尿的全球患者中,治疗至48周时:
斯贝利单抗治疗组82.5%的患者(33/40)镜下血尿转阴[红细胞≤5个/高倍视野(HPF)],而安慰剂组仅为52.6%(51/97);
采用Kaplan-Meier法估算,48周内斯贝利单抗治疗组血尿缓解概率为90.9%,显著高于安慰剂组的68.1%;
中位缓解时间:斯贝利单抗组为9周,安慰剂组为24周。
这些数据进一步支持APRIL抑制在控制免疫介导肾损伤中的关键作用,也为临床提供了除尿蛋白外的另一疗效评估维度。同时,斯贝利单抗治疗组患者的蛋白尿缓解率更高,与血尿缓解结果互为补充。
VISOR试验进行中:重复肾活检将直接评估肾组织学改变
为进一步明确斯贝利单抗对肾脏组织学的影响,研究者已启动VISOR试验[6]。这是一项IIb期、多中心、开放标签、重复肾活检、单臂临床试验,旨在直接评估APRIL抑制对IgA肾病成人患者肾脏组织病理学的影响。开展VISOR试验的目的是为了进一步明确全球VISIONARY研究项目中观察到的临床改善是否能转化为肾脏内可量化的组织学改变,从而帮助阐明APRIL抑制的作用机制与改善疾病进程的潜力。
研究计划纳入约50例患者,接受最长2年的斯贝利单抗治疗,方案规定的肾活检分别在基线、52周时进行,持续接受治疗的患者将在104周时再次接受肾活检。探索性分析将额外评估疾病活动度相关的组织学与细胞标志物,包括肾小球IgA沉积变化;MEST-C评分动态演变;免疫细胞浸润、补体沉积;空间转录组学特征。
该研究是首个评估斯贝利单抗治疗后肾组织学变化的临床试验,有望为APRIL抑制的机制与疗效提供组织层面的直接证据,超越临床生物标志物,提供组织层面的疾病活动度评估指标。
专家述评
作为III期VISIONARY试验学术指导委员会成员和中国队列的主要研究者,张宏教授表示:“IgA肾病在中国造成了沉重的疾病负担,大量患者仍面临进展为肾衰竭的风险。尿蛋白水平升高与患者更快进展为ESKD密切相关。在该研究的中国队列中,斯贝利单抗可显著降低患者尿蛋白水平,降幅具有明确临床意义,与全球主队列的观察结果高度一致。”
张宏教授进一步讲道:“本次WCN上公布的补充分析结果,包括血尿相关研究发现以及正在开展的VISOR试验,进一步深化了我们对IgA肾病领域中APRIL抑制的认知。血尿作为疾病活动度的标志,其缓解速度与程度为我们提供了新的疗效评估维度,也为 IgA肾病的精准治疗提供了更全面的循证依据。同时,我们也期待这一靶向治疗未来能够惠及更多的中国患者。”
结语
斯贝利单抗作为全球首个选择性抑制APRIL的IgA肾病治疗药物,在III期VISIONARY试验中展现出优异的疗效与安全性。全球主队列数据的发表,为其临床应用奠定了坚实的循证基础。中国队列数据与全球结果高度一致,为其在中国人群中的应用提供了直接证据。随着血尿缓解、生物标志物变化及肾脏组织学数据的不断积累,APRIL抑制有望成为IgA肾病治疗的新基石,为众多面临疾病进展风险的IgA肾病患者带来新的希望。
专家简介

张宏教授
北京大学第一医院肾内科主任,北京大学肾脏疾病研究所副所长
主任医师、教授、博士/博士后导师
日本冈山大学医学部医学博士;美国耶鲁大学医学院遗传系客座研究员
国家自然科学基金委杰出青年/教育部新世纪优秀人才/中华医学专项人才
国际肾脏病学会教育大使;国之名医-优秀风范奖获得者
国际肾脏病学会(ISN)东北亚委员会委员;ISN继续教育顾问委员会委员
ISN临床试验促进委员会委员;ISN临床研究委员会委员
国际IgA肾病合作组(IIgANN)专家委员会委员
中国IgA肾病合作组(IIgANN-China) 主席
中国医师协会循证医学专委会常委;北京医学会肾脏病学分会副主委
SCI论文260余篇,代表性论文在JAMA、KI、JASN、Nat Genet等发表
参考文献:
[1]中国医药卫生文化协会肾病与血液净化专业委员会.原发性IgA肾病管理和治疗中国专家共识[J].中华肾病研究电子杂志,2024, 13 (1): 1-28.
[2]Wang Gangan , Zheng Ke , Li Xuemei. Researches progress on pathogenesis of IgA nephropathy[J]. Chinese Journal of Nephrology, 2024, 40(3): 225-230.
[3]Suzuki H, et al. Increased APRIL Expression Induces IgA1 Aberrant Glycosylation in IgA Nephropathy [J]. Medicine, 2016, 95 (11): e3099.
[4] Perkovic V, Trimarchi H, Tesar V, et al. Sibeprenlimab in IgA nephropathy — interim analysis of a phase 3 trial[J]. N Engl J Med, 2025, 393(12): 1123-1134.
[5]Floege J, Fervenza FC, Coppo R. Microscopic hematuria in IgA nephropathy: a biomarker of disease activity[J]. Clinical Kidney Journal, 2026, 19(2): sfag003.
[6] VISOR Study Group. VISOR: A phase 2b, open-label, repeat kidney biopsy trial to evaluate the effects of sibeprenlimab on renal histology in patients with IgA nephropathy [J]. Nephrol Dial Transplant, 2026, 41(Suppl 1): i123-i124.
- 推荐文章
WCN中国之声丨吕继成教授:HSK39297强效抑制AP活性近80%,显著降低IgA肾病蛋白尿约50%
WCN 2026丨临床突破接连落地,B细胞靶向治疗成肾小球疾病治疗核心赛道
每月1针,UPCR降幅可达62%!WCN 2026公布IgA肾病中国队列数据
WCN中国之声丨中山大学附属第三医院彭晖教授团队:AKI-CKD转归与EPS发病机制新突破
心血管代谢联盟——心-肾-代谢综合征(CKM)学术研讨会在武汉圆满落幕
WCN 2026丨Vlado Perkovic教授重磅公布APPLAUSE-IgAN研究最终分析结果,为补体抑制提供了首个长期肾功能保护证据
WCN中国之声丨陈会想教授:痛风患者血尿酸水平与CKD发病风险呈线性剂量反应关系
共晶技术赋能,降压护靶协同——中国原研ARNI开创高血压治疗新未来
WCN 2026重磅|iCaReMe高钾结果揭晓与Balcinrenone联合达格列净为CKD高钾血症带来新选择
WCN 2026丨郝传明教授主持国际研讨会,解读2026版KDIGO CKD贫血管理指南与诊疗前沿
ACC.26 | 面对降压的“天花板效应”,源头截流是否更有效?——KARDINAL Ⅱ期研究结果发布
WCN 2026巅峰对话丨有进展风险的IgA肾病患者首选治疗:布地奈德肠溶胶囊还是补体抑制剂?——不是“非此即彼”,而是“协同共进”
WCN中国之声丨孙良忠教授团队聚焦肾消耗病(肾单位肾痨)发病机制的研究取得新进展
WCN 2026丨全体大会:Bywaters奖揭晓+足细胞病新分类体系重磅发布
WCN 2026丨Zigakibart治疗IgA肾病再添力证:eGFR稳定获益不依赖基线肾功能、蛋白尿水平,SHIFT研究首次探究其对肾组织IgA沉积的影响
WCN中国之声丨北大张路霞教授做精彩报告,分享全球CKD诊断、检测最新进展
WCN中国之声丨李贵森教授团队:CKD血管钙化新机制与干预靶点最新发现
WCN 2026热点争鸣丨朋友还是敌人:SUMO化修饰在肾脏损伤与修复中的双向调控机制
WCN 2026丨Difelikefalin在难治性CKD-aP治疗、AKI的肾保护与抗炎中均展现出重要临床价值
WCN中国之声丨余学清教授在HIT专场报告ASPIRED研究进展,探索低剂量阿司匹林对透析患者心血管保护价值
WCN中国之声丨姜雪教授团队IgAN重磅成果:黄芪甲苷IV创新机制与临床真实世界证据
最新证据:肥胖人士每日摄入杏仁,对改善炎症有帮助!
WCN 2026|靶向肠道,直击源头——多项研究筑牢布地奈德肠溶胶囊对因治疗IgA肾病的基石地位
WCN 2026丨OLYMPUS试验设计公布,双靶点药物Povetacicept有望改写原发性膜性肾病治疗格局
走进河北省人民医院:探讨内分泌科在“CKM早期行动”中的“前哨”作用
指南共识丨本土循证+精准实操!2026版中国ADPKD临床实践指南发布,25条核心推荐规范全病程管理
WCN 2026丨锁定IgA肾病蛋白尿“早治窗口”,布地奈德肠溶胶囊直击肠源,实现长久护肾
WCN 2026盛大开幕:聚全球智慧 探肾病前沿 共赴健康之约
指南共识丨本土循证+WCN 2026|醛固酮合成酶抑制剂Baxdrostat BaxHTN全球研究结果重磅亮相、BaxAsia亚洲人群基线特征首次公布精准实操!2026版中国ADPKD临床实践指南发布,25条核心推荐规范全病程管理
肾例明鉴 | 夜尿2年竟藏致命血管炎!29岁男子的肾脏“嗜酸危机”,这个“沉默”的肾脏肉芽肿差点漏诊
治疗原发性膜性肾病:利妥昔单抗与环磷酰胺联合激素的疗效与安全性相当
2型糖尿病合并慢性肾脏病患者长期强化降尿酸治疗
肾域华章 | 北大医院周绪杰/张宏团队研究:全维度解析IgA肾病血浆蛋白、免疫细胞及免疫细胞性状的因果因素
超50万例患者的研究揭秘:SGLT2i与GLP-1RA单药还是联合,更能预防2型糖尿病肾衰竭?
打破“身”“心”壁垒:万人研究证实抑郁越重,CKM综合征进展风险越高,TyG指数是关键中介
征文投稿倒计时10天 | 中华医学会肾脏病学分会第二十届重症肾脏病与血液净化大会
ACC 2026前沿速递:心肾代谢综合征与肥胖专题精彩预告
WCN 2026前瞻|巅峰聚焦IgA肾病从“尽早干预”到“源头阻断”,中国证据再添力证
国际专家组发表血液吸附联合血液透析(HAHD)共识声明,蔡广研/丁小强/林洪丽作为专家组成员参与制定
ASN发布《肾衰竭患者保守治疗肾脏健康指南》及《执行摘要》
一文读懂CKM:从病理机制到治疗进展
IgA肾病15种疗法大比拼:李贵森团队对37项RCT、4889例患者的网络荟萃分析,谁是疗效与安全的最优解?
慢性肾脏病患者的多重用药:临床医师必须监测的10类药物
最新研究预警!30~40岁血压偏高,40岁后心肾疾病风险大幅上升
中国力量闪耀WCN 2026!200余项原创研究入选,其中3项重磅研究将在高影响力临床试验专场亮相
降压目标之争:120 mmHg还是130 mmHg?最新荟萃分析给出答案
肾例明鉴|67岁老人肾衰、咯血、反复感染,元凶竟是两种自身抗体联手!这例罕见肾炎,藏着太多教训
《新英格兰医学杂志》重磅发布奥妥珠单抗ALLEGORY Ⅲ期研究成果,进一步完善其在自身免疫性疾病中的证据链
最新Meta分析:死亡风险随CKM分期进展呈“阶梯式”攀升
WCN2026即将启幕,中国青年学者斩获国际大奖+四大核心主题锚定肾脏医学发展方向
首个突破!FINE-ONE Ⅲ期研究证实非奈利酮为1型糖尿病肾病治疗破局
临床价值深度解析:司美格鲁肽片何以在口服GLP-1RA中脱颖而出?
非奈利酮FIND-CKD研究Ⅲ期结果重磅公布,非糖尿病慢性肾病治疗迎来新方法
临床常见但容易令医师头疼的慢性肾病——微小病变肾病的治疗方案总结归纳,值得收藏!
JAMA子刊重磅:CKM综合征分期越晚,强化降压获益越小?3.3万中国数据给出答案
