- 首页 > 正文
WCN 2026丨郝传明教授主持国际研讨会,解读2026版KDIGO CKD贫血管理指南与诊疗前沿
发表时间:2026-04-25 17:14:30
导读
慢性肾脏病(CKD)贫血是CKD患者最常见的并发症之一,显著增加患者心血管事件、肾衰竭及全因死亡风险,是CKD全程管理的核心环节。3月30日,2026年世界肾脏病大会(WCN)特设 “CKD 贫血管理:最新证据与未来方向” 专题研讨会,由复旦大学附属华山医院郝传明教授担任会议主持。美国斯坦福大学Wolfgang Winkelmayer教授、马来西亚双威大学Sunita Bavanandan教授、德国埃尔朗根纽伦堡大学KaiUwe Eckardt教授三位国际顶尖学者,分别从2026 KDIGO指南更新、全球诊疗地区差异、前沿治疗进展三个维度,系统梳理了CKD贫血诊疗的现状与未来,为全球肾脏病医师带来了权威解读。
一、2026 KDIGO CKD贫血指南解读:核心更新与临床实践
1.优化铁剂管理,维持铁稳态
作为本次研讨会的首个环节,美国斯坦福大学Wolfgang Winkelmayer教授,系统解读了2026 KDIGO CKD贫血指南的关键更新,为临床诊疗提供了权威框架。指南明确了不同CKD分期患者的铁剂管理阈值:非透析CKD患者,当转铁蛋白饱和度(TSAT)<20%、铁蛋白<100 ng/mL时启动补铁;血液透析患者,TSAT<20%、铁蛋白<200 ng/mL时启动补铁,且优先选择静脉铁剂(如蔗糖铁、羧基麦芽糖铁)。基于PIVOTAL等大型研究证据,指南推荐主动补铁以维持铁稳态,避免铁缺乏影响促红细胞生成素(ESA)疗效,同时减少ESA的使用剂量,从而降低相关风险[1]。
2.明确ESA与氧诱导因子-脯氨酰羟化酶抑制剂(HIF-PHI)一线/二线定位,严格适用人群
本次指南的核心调整之一,是明确ESA为CKD贫血治疗的一线首选药物,而HIF-PHI因长期心血管安全性数据不足、潜在血栓风险,被列为二线治疗,仅用于ESA不耐受或疗效不佳的患者。同时,严格限制HIF-PHI的适用人群,禁用于有血栓病史、恶性肿瘤、妊娠的CKD患者,强调需充分评估获益风险后使用。
1.全球CKD贫血地区分布差异显著
马来西亚双威大学Sunita Bavanandan教授聚焦全球CKD贫血诊疗的不均衡性,系统分析了不同地区的管理差异,为中低收入国家的诊疗改进提供了方向。全球CKD患者贫血患病率随肾功能下降显著升高:CKD 3~5期非透析患者患病率约30%~60%,血液透析患者高达90%以上。中亚、撒哈拉以南非洲地区患病率最高(>70%),西欧、北美最低(<40%)(图1);女性、老年患者患病率显著高于男性、年轻患者,中低收入地区患者贫血严重程度更高[2]。ISN i-NET-CKD全球队列研究也证实,不同地区CKD患者的血红蛋白水平存在显著的分布差异,进一步验证了CKD贫血管理的地区不均衡性[3]。
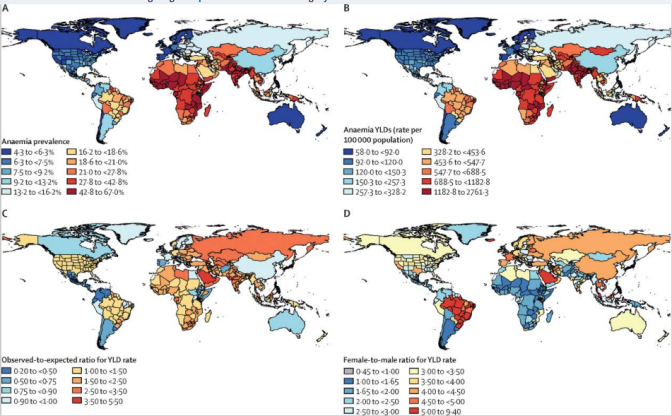
图1. 2021年全球慢性肾脏病相关贫血流行病学分布[2]
Bavanandan教授指出,全球CKD贫血管理的差异源于多维度因素。
(1)人群因素:中低收入地区慢性感染(如疟疾、结核)、营养缺乏(铁、维生素B12、叶酸)、遗传因素(如镰状细胞贫血),导致贫血患病率更高、更严重[4-5];
(2)医疗资源:中低收入地区贫血筛查覆盖率不足30%,铁剂、ESA、HIF-PHI等药物可及性差,血透中心数量不足,导致干预滞后[6-7];
(3)政策与指南:不同地区指南标准不一,KDIGO、欧洲肾脏病学会欧洲透析移植学会(ERBP)、日本肾脏病学会(JSDT)的诊断阈值、治疗目标存在差异,影响临床实践的同质化[8];
(4)临床实践:治疗惰性、医师对贫血危害认知不足,导致近40%的贫血患者未得到及时干预[9-10]。不同国家腹膜透析患者的贫血管理实践也存在显著差异,ESA、静脉铁剂的使用率差异显著[11],CKD opps系列研究更显示,仅当患者血红蛋白呈持续下降趋势时,临床医师才会启动贫血治疗,进一步加剧了治疗滞后的问题[12]。
2.全球同质化管理的改进方向
针对上述差异,Bavanandan教授提出了四大改进策略:(1)建立全球CKD贫血监测网络,推动标准化诊疗流程;(2)优化医疗政策,提高药物可及性,降低患者经济负担;(3)加强基层医师培训,提升贫血管理能力;(4)开展本土循证研究,制定适配地区人群的诊疗方案[13]。
三、CKD贫血治疗新进展:超越ESA与铁剂,迈向多靶点精准干预
1.钠葡萄糖协同转运蛋白2(SGLT2)抑制剂:CKD贫血的基础干预新选择
德国埃尔朗根纽伦堡大学KaiUwe Eckardt教授系统梳理了CKD贫血治疗的前沿进展,提出了超越传统“ESA+铁剂”的多靶点干预策略,为未来诊疗指明了方向。多项大型RCT研究(如DAPACKD、EMPAKIDNEY)证实,SGLT2抑制剂可通过升高内源性EPO、降低铁调素、减轻慢性炎症,显著改善CKD患者贫血,升高Hb水平,同时降低心血管事件、肾衰竭风险[14]。虽轻度增加红细胞增多症风险,但不升高血栓事件风险[15],可作为CKD贫血的基础干预药物,尤其适用于合并糖尿病、心力衰竭的患者[16]。
2.新型EPO受体激动剂与抗炎治疗
中国原研聚乙二醇化EPO模拟剂(Pegmolesatide)的Ⅲ期临床数据显示,其半衰期长达140小时,可每4周给药一次,疗效与传统ESA相当,安全性良好,显著提升了患者的治疗依从性,为CKD贫血的长期管理提供了便利[17]。此前国际同类产品培莫沙肽的系列研究,也为EPO受体激动剂的研发与临床应用奠定了基础,同时也明确了该类药物的适用人群与安全风险[18-20]。此外,补充与替代医学在肾性贫血中的应用也逐步受到关注,相关综述总结了16项可提升血红蛋白水平的补充替代治疗研究,为临床提供了更多潜在选择[21]。
白细胞介素-6(IL-6)抑制剂(如clazakizumab、ziltivekimab)可通过抑制炎症因子,降低铁调素水平,改善炎症性贫血,为难治性CKD贫血(尤其是合并慢性炎症的患者)提供了新的治疗选择。多项Ⅱ/Ⅲ期研究证实,IL-6抑制剂可显著升高Hb,减少ESA使用,安全性良好,有望成为CKD贫血治疗的新靶点[22-25]。
3.心肾贫血综合征(CRAS)整合管理,协同改善预后
Eckardt教授提出了CRAS的整合管理框架,强调贫血、心功能不全、肾功能不全三者相互影响,需联合铁剂、HIF-PHI、SGLT2i、抗炎药物,多靶点干预,同时改善心肾预后[26]。贫血管理是CKD全程管理的重要组成部分,需与心血管保护、肾功能保护协同进行,实现一体化管理。
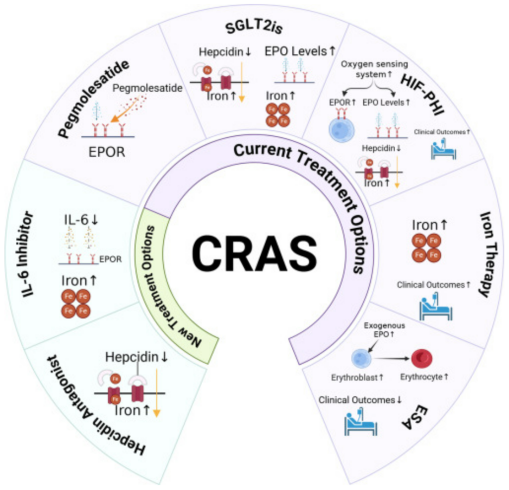
图2. 心肾贫血综合征(CRAS)的现有与新型治疗策略概览[26]
总结
本次WCN 2026 CKD贫血专题研讨会,明确了ESA的一线地位与铁剂管理的优化策略。全球地区差异的分析,为中低收入国家的诊疗改进提供了方向。前沿进展则为超越传统治疗、实现多靶点精准干预奠定了基础。对于肾病医师而言,需在遵循国际指南的基础上,结合本土人群的流行病学特征、药物可及性,制定本土化的诊疗方案。
专家简介

肾内科教授,主任医师,上海特聘专家
复旦大学肾脏病研究所常务副所长
中国生理学会肾脏生理分会前任主任委员
上海医师协会肾科医师分会会长
亚太肾病学会CME委员会委员
Am J Physiol – renal编委、 Kidney Disease副主编
主要从事高血压和糖尿病肾病的基础和临床研究,先后主持国家自然基金重点项目,国际合作重点项目, 面上项目、卫生部行业基金子课题、973子课题、美国国立卫生院基金等;近年来发表论SCI收录论文180余篇,包括JCI, JASN, KI, Hypertension, Nat Med,NEJM等
参考文献
[1] KDIGO 2026 Clinical Practice Guideline for Anemia in Chronic Kidney Disease. Kidney Int.
[2] Liu Y, et al. Clinical Kidney Journal. 2025;18(2):287-298.
[3] Canney M, et al. Kidney International Reports. 2023;8(11):2677-2687.
[4] Kassebaum NJ, et al. Blood. 2014;123(5):615-624.
[5] Levin A, et al. Lancet. 2017;389(10075):1248-1260.
[6] Wong G, et al. Clinical Kidney Journal. 2020;13(3):412-421.
[7] Bello AK, Okpechi IG, Levin A, et al. Lancet Global Health. 2024;12(3):e382-e395.
[8] Hasegawa T, et al. Kidney International. 2011;79(11):1234-1241.
[9] Wong G, et al. Clinical Kidney Journal. 2019;12(6):897-905.
[10] Minutolo R, et al. Nephrology Dialysis Transplantation. 2013;28(6):1524-1532.
[11] Perlman RL, et al. Peritoneal Dialysis International. 2019;39(5):484-493.
[12] Lopes AA, et al. Scientific Reports. 2021;11(1):12345.
[13] Luyckx VA, et al. American Journal of Nephrology. 2023;54(10):789-801.
[14] Koshino K, et al. NEJM Evidence. 2023;2(11):eoaid2300168.
[15] Lewis E, et al. JAMA Network Open. 2025;8(3):e254872.
[16] Packer M, Cleland JGF. Journal of Cardiac Failure. 2023;29(12):1027-1030.
[17] Xie J, et al. Kidney International Reports. 2025;10(12):2897-2906.
[18] Macdougall IC, et al. New England Journal of Medicine. 2009;361(17):1640-1653.
[19] Fishbane S, et al. New England Journal of Medicine. 2013;369(19):1792-1802.
[20] Macdougall IC, et al. New England Journal of Medicine. 2013;369(19):1803-1813.
[21] Lu CM, Hsu YH, Lin H, et al. Frontiers in Endocrinology (Lausanne). 2025;16:1428737.
[22] Chertow GM, et al. Nature Medicine. 2024;30(6):1524-1534.
[23] Neuen BL, et al. Journal of the American Society of Nephrology. 2025;36(4):789-802.
[24] Pergola PE, et al. Journal of the American Society of Nephrology. 2024;35(10):1897-1908.
[25] Ridker PM, et al. Lancet. 2021;398(10309):1483-1494.
[26] Heng L, et al. European Journal of Internal Medicine. 2026;S0953-6205(26)00087-2.
慢性肾脏病(CKD)贫血是CKD患者最常见的并发症之一,显著增加患者心血管事件、肾衰竭及全因死亡风险,是CKD全程管理的核心环节。3月30日,2026年世界肾脏病大会(WCN)特设 “CKD 贫血管理:最新证据与未来方向” 专题研讨会,由复旦大学附属华山医院郝传明教授担任会议主持。美国斯坦福大学Wolfgang Winkelmayer教授、马来西亚双威大学Sunita Bavanandan教授、德国埃尔朗根纽伦堡大学KaiUwe Eckardt教授三位国际顶尖学者,分别从2026 KDIGO指南更新、全球诊疗地区差异、前沿治疗进展三个维度,系统梳理了CKD贫血诊疗的现状与未来,为全球肾脏病医师带来了权威解读。

一、2026 KDIGO CKD贫血指南解读:核心更新与临床实践
1.优化铁剂管理,维持铁稳态
作为本次研讨会的首个环节,美国斯坦福大学Wolfgang Winkelmayer教授,系统解读了2026 KDIGO CKD贫血指南的关键更新,为临床诊疗提供了权威框架。指南明确了不同CKD分期患者的铁剂管理阈值:非透析CKD患者,当转铁蛋白饱和度(TSAT)<20%、铁蛋白<100 ng/mL时启动补铁;血液透析患者,TSAT<20%、铁蛋白<200 ng/mL时启动补铁,且优先选择静脉铁剂(如蔗糖铁、羧基麦芽糖铁)。基于PIVOTAL等大型研究证据,指南推荐主动补铁以维持铁稳态,避免铁缺乏影响促红细胞生成素(ESA)疗效,同时减少ESA的使用剂量,从而降低相关风险[1]。
2.明确ESA与氧诱导因子-脯氨酰羟化酶抑制剂(HIF-PHI)一线/二线定位,严格适用人群
本次指南的核心调整之一,是明确ESA为CKD贫血治疗的一线首选药物,而HIF-PHI因长期心血管安全性数据不足、潜在血栓风险,被列为二线治疗,仅用于ESA不耐受或疗效不佳的患者。同时,严格限制HIF-PHI的适用人群,禁用于有血栓病史、恶性肿瘤、妊娠的CKD患者,强调需充分评估获益风险后使用。
指南强调,需基于患者的CKD分期、合并症、贫血严重程度,制定个体化的血红蛋白(Hb)目标值,推荐一般患者Hb维持在11~12 g/dL,避免超过13 g/dL,以平衡贫血改善的获益与心血管事件、血栓的风险[1]。
1.全球CKD贫血地区分布差异显著
马来西亚双威大学Sunita Bavanandan教授聚焦全球CKD贫血诊疗的不均衡性,系统分析了不同地区的管理差异,为中低收入国家的诊疗改进提供了方向。全球CKD患者贫血患病率随肾功能下降显著升高:CKD 3~5期非透析患者患病率约30%~60%,血液透析患者高达90%以上。中亚、撒哈拉以南非洲地区患病率最高(>70%),西欧、北美最低(<40%)(图1);女性、老年患者患病率显著高于男性、年轻患者,中低收入地区患者贫血严重程度更高[2]。ISN i-NET-CKD全球队列研究也证实,不同地区CKD患者的血红蛋白水平存在显著的分布差异,进一步验证了CKD贫血管理的地区不均衡性[3]。

图1. 2021年全球慢性肾脏病相关贫血流行病学分布[2]
Bavanandan教授指出,全球CKD贫血管理的差异源于多维度因素。
(1)人群因素:中低收入地区慢性感染(如疟疾、结核)、营养缺乏(铁、维生素B12、叶酸)、遗传因素(如镰状细胞贫血),导致贫血患病率更高、更严重[4-5];
(2)医疗资源:中低收入地区贫血筛查覆盖率不足30%,铁剂、ESA、HIF-PHI等药物可及性差,血透中心数量不足,导致干预滞后[6-7];
(3)政策与指南:不同地区指南标准不一,KDIGO、欧洲肾脏病学会欧洲透析移植学会(ERBP)、日本肾脏病学会(JSDT)的诊断阈值、治疗目标存在差异,影响临床实践的同质化[8];
(4)临床实践:治疗惰性、医师对贫血危害认知不足,导致近40%的贫血患者未得到及时干预[9-10]。不同国家腹膜透析患者的贫血管理实践也存在显著差异,ESA、静脉铁剂的使用率差异显著[11],CKD opps系列研究更显示,仅当患者血红蛋白呈持续下降趋势时,临床医师才会启动贫血治疗,进一步加剧了治疗滞后的问题[12]。
2.全球同质化管理的改进方向
针对上述差异,Bavanandan教授提出了四大改进策略:(1)建立全球CKD贫血监测网络,推动标准化诊疗流程;(2)优化医疗政策,提高药物可及性,降低患者经济负担;(3)加强基层医师培训,提升贫血管理能力;(4)开展本土循证研究,制定适配地区人群的诊疗方案[13]。
三、CKD贫血治疗新进展:超越ESA与铁剂,迈向多靶点精准干预
1.钠葡萄糖协同转运蛋白2(SGLT2)抑制剂:CKD贫血的基础干预新选择
德国埃尔朗根纽伦堡大学KaiUwe Eckardt教授系统梳理了CKD贫血治疗的前沿进展,提出了超越传统“ESA+铁剂”的多靶点干预策略,为未来诊疗指明了方向。多项大型RCT研究(如DAPACKD、EMPAKIDNEY)证实,SGLT2抑制剂可通过升高内源性EPO、降低铁调素、减轻慢性炎症,显著改善CKD患者贫血,升高Hb水平,同时降低心血管事件、肾衰竭风险[14]。虽轻度增加红细胞增多症风险,但不升高血栓事件风险[15],可作为CKD贫血的基础干预药物,尤其适用于合并糖尿病、心力衰竭的患者[16]。
2.新型EPO受体激动剂与抗炎治疗
中国原研聚乙二醇化EPO模拟剂(Pegmolesatide)的Ⅲ期临床数据显示,其半衰期长达140小时,可每4周给药一次,疗效与传统ESA相当,安全性良好,显著提升了患者的治疗依从性,为CKD贫血的长期管理提供了便利[17]。此前国际同类产品培莫沙肽的系列研究,也为EPO受体激动剂的研发与临床应用奠定了基础,同时也明确了该类药物的适用人群与安全风险[18-20]。此外,补充与替代医学在肾性贫血中的应用也逐步受到关注,相关综述总结了16项可提升血红蛋白水平的补充替代治疗研究,为临床提供了更多潜在选择[21]。
白细胞介素-6(IL-6)抑制剂(如clazakizumab、ziltivekimab)可通过抑制炎症因子,降低铁调素水平,改善炎症性贫血,为难治性CKD贫血(尤其是合并慢性炎症的患者)提供了新的治疗选择。多项Ⅱ/Ⅲ期研究证实,IL-6抑制剂可显著升高Hb,减少ESA使用,安全性良好,有望成为CKD贫血治疗的新靶点[22-25]。
3.心肾贫血综合征(CRAS)整合管理,协同改善预后
Eckardt教授提出了CRAS的整合管理框架,强调贫血、心功能不全、肾功能不全三者相互影响,需联合铁剂、HIF-PHI、SGLT2i、抗炎药物,多靶点干预,同时改善心肾预后[26]。贫血管理是CKD全程管理的重要组成部分,需与心血管保护、肾功能保护协同进行,实现一体化管理。

图2. 心肾贫血综合征(CRAS)的现有与新型治疗策略概览[26]
总结
本次WCN 2026 CKD贫血专题研讨会,明确了ESA的一线地位与铁剂管理的优化策略。全球地区差异的分析,为中低收入国家的诊疗改进提供了方向。前沿进展则为超越传统治疗、实现多靶点精准干预奠定了基础。对于肾病医师而言,需在遵循国际指南的基础上,结合本土人群的流行病学特征、药物可及性,制定本土化的诊疗方案。
专家简介

肾内科教授,主任医师,上海特聘专家
复旦大学肾脏病研究所常务副所长
中国生理学会肾脏生理分会前任主任委员
上海医师协会肾科医师分会会长
亚太肾病学会CME委员会委员
Am J Physiol – renal编委、 Kidney Disease副主编
主要从事高血压和糖尿病肾病的基础和临床研究,先后主持国家自然基金重点项目,国际合作重点项目, 面上项目、卫生部行业基金子课题、973子课题、美国国立卫生院基金等;近年来发表论SCI收录论文180余篇,包括JCI, JASN, KI, Hypertension, Nat Med,NEJM等


参考文献
[1] KDIGO 2026 Clinical Practice Guideline for Anemia in Chronic Kidney Disease. Kidney Int.
[2] Liu Y, et al. Clinical Kidney Journal. 2025;18(2):287-298.
[3] Canney M, et al. Kidney International Reports. 2023;8(11):2677-2687.
[4] Kassebaum NJ, et al. Blood. 2014;123(5):615-624.
[5] Levin A, et al. Lancet. 2017;389(10075):1248-1260.
[6] Wong G, et al. Clinical Kidney Journal. 2020;13(3):412-421.
[7] Bello AK, Okpechi IG, Levin A, et al. Lancet Global Health. 2024;12(3):e382-e395.
[8] Hasegawa T, et al. Kidney International. 2011;79(11):1234-1241.
[9] Wong G, et al. Clinical Kidney Journal. 2019;12(6):897-905.
[10] Minutolo R, et al. Nephrology Dialysis Transplantation. 2013;28(6):1524-1532.
[11] Perlman RL, et al. Peritoneal Dialysis International. 2019;39(5):484-493.
[12] Lopes AA, et al. Scientific Reports. 2021;11(1):12345.
[13] Luyckx VA, et al. American Journal of Nephrology. 2023;54(10):789-801.
[14] Koshino K, et al. NEJM Evidence. 2023;2(11):eoaid2300168.
[15] Lewis E, et al. JAMA Network Open. 2025;8(3):e254872.
[16] Packer M, Cleland JGF. Journal of Cardiac Failure. 2023;29(12):1027-1030.
[17] Xie J, et al. Kidney International Reports. 2025;10(12):2897-2906.
[18] Macdougall IC, et al. New England Journal of Medicine. 2009;361(17):1640-1653.
[19] Fishbane S, et al. New England Journal of Medicine. 2013;369(19):1792-1802.
[20] Macdougall IC, et al. New England Journal of Medicine. 2013;369(19):1803-1813.
[21] Lu CM, Hsu YH, Lin H, et al. Frontiers in Endocrinology (Lausanne). 2025;16:1428737.
[22] Chertow GM, et al. Nature Medicine. 2024;30(6):1524-1534.
[23] Neuen BL, et al. Journal of the American Society of Nephrology. 2025;36(4):789-802.
[24] Pergola PE, et al. Journal of the American Society of Nephrology. 2024;35(10):1897-1908.
[25] Ridker PM, et al. Lancet. 2021;398(10309):1483-1494.
[26] Heng L, et al. European Journal of Internal Medicine. 2026;S0953-6205(26)00087-2.
- 推荐文章
WCN中国之声丨吕继成教授:HSK39297强效抑制AP活性近80%,显著降低IgA肾病蛋白尿约50%
WCN 2026丨临床突破接连落地,B细胞靶向治疗成肾小球疾病治疗核心赛道
每月1针,UPCR降幅可达62%!WCN 2026公布IgA肾病中国队列数据
WCN中国之声丨中山大学附属第三医院彭晖教授团队:AKI-CKD转归与EPS发病机制新突破
心血管代谢联盟——心-肾-代谢综合征(CKM)学术研讨会在武汉圆满落幕
WCN 2026丨Vlado Perkovic教授重磅公布APPLAUSE-IgAN研究最终分析结果,为补体抑制提供了首个长期肾功能保护证据
WCN中国之声丨陈会想教授:痛风患者血尿酸水平与CKD发病风险呈线性剂量反应关系
共晶技术赋能,降压护靶协同——中国原研ARNI开创高血压治疗新未来
WCN 2026重磅|iCaReMe高钾结果揭晓与Balcinrenone联合达格列净为CKD高钾血症带来新选择
WCN 2026丨郝传明教授主持国际研讨会,解读2026版KDIGO CKD贫血管理指南与诊疗前沿
ACC.26 | 面对降压的“天花板效应”,源头截流是否更有效?——KARDINAL Ⅱ期研究结果发布
WCN 2026巅峰对话丨有进展风险的IgA肾病患者首选治疗:布地奈德肠溶胶囊还是补体抑制剂?——不是“非此即彼”,而是“协同共进”
WCN中国之声丨孙良忠教授团队聚焦肾消耗病(肾单位肾痨)发病机制的研究取得新进展
WCN 2026丨全体大会:Bywaters奖揭晓+足细胞病新分类体系重磅发布
WCN 2026丨Zigakibart治疗IgA肾病再添力证:eGFR稳定获益不依赖基线肾功能、蛋白尿水平,SHIFT研究首次探究其对肾组织IgA沉积的影响
WCN中国之声丨北大张路霞教授做精彩报告,分享全球CKD诊断、检测最新进展
WCN中国之声丨李贵森教授团队:CKD血管钙化新机制与干预靶点最新发现
WCN 2026热点争鸣丨朋友还是敌人:SUMO化修饰在肾脏损伤与修复中的双向调控机制
WCN 2026丨Difelikefalin在难治性CKD-aP治疗、AKI的肾保护与抗炎中均展现出重要临床价值
WCN中国之声丨余学清教授在HIT专场报告ASPIRED研究进展,探索低剂量阿司匹林对透析患者心血管保护价值
WCN中国之声丨姜雪教授团队IgAN重磅成果:黄芪甲苷IV创新机制与临床真实世界证据
最新证据:肥胖人士每日摄入杏仁,对改善炎症有帮助!
WCN 2026|靶向肠道,直击源头——多项研究筑牢布地奈德肠溶胶囊对因治疗IgA肾病的基石地位
WCN 2026丨OLYMPUS试验设计公布,双靶点药物Povetacicept有望改写原发性膜性肾病治疗格局
走进河北省人民医院:探讨内分泌科在“CKM早期行动”中的“前哨”作用
指南共识丨本土循证+精准实操!2026版中国ADPKD临床实践指南发布,25条核心推荐规范全病程管理
WCN 2026丨锁定IgA肾病蛋白尿“早治窗口”,布地奈德肠溶胶囊直击肠源,实现长久护肾
WCN 2026盛大开幕:聚全球智慧 探肾病前沿 共赴健康之约
指南共识丨本土循证+WCN 2026|醛固酮合成酶抑制剂Baxdrostat BaxHTN全球研究结果重磅亮相、BaxAsia亚洲人群基线特征首次公布精准实操!2026版中国ADPKD临床实践指南发布,25条核心推荐规范全病程管理
肾例明鉴 | 夜尿2年竟藏致命血管炎!29岁男子的肾脏“嗜酸危机”,这个“沉默”的肾脏肉芽肿差点漏诊
治疗原发性膜性肾病:利妥昔单抗与环磷酰胺联合激素的疗效与安全性相当
2型糖尿病合并慢性肾脏病患者长期强化降尿酸治疗
肾域华章 | 北大医院周绪杰/张宏团队研究:全维度解析IgA肾病血浆蛋白、免疫细胞及免疫细胞性状的因果因素
超50万例患者的研究揭秘:SGLT2i与GLP-1RA单药还是联合,更能预防2型糖尿病肾衰竭?
打破“身”“心”壁垒:万人研究证实抑郁越重,CKM综合征进展风险越高,TyG指数是关键中介
征文投稿倒计时10天 | 中华医学会肾脏病学分会第二十届重症肾脏病与血液净化大会
ACC 2026前沿速递:心肾代谢综合征与肥胖专题精彩预告
WCN 2026前瞻|巅峰聚焦IgA肾病从“尽早干预”到“源头阻断”,中国证据再添力证
国际专家组发表血液吸附联合血液透析(HAHD)共识声明,蔡广研/丁小强/林洪丽作为专家组成员参与制定
ASN发布《肾衰竭患者保守治疗肾脏健康指南》及《执行摘要》
一文读懂CKM:从病理机制到治疗进展
IgA肾病15种疗法大比拼:李贵森团队对37项RCT、4889例患者的网络荟萃分析,谁是疗效与安全的最优解?
慢性肾脏病患者的多重用药:临床医师必须监测的10类药物
最新研究预警!30~40岁血压偏高,40岁后心肾疾病风险大幅上升
中国力量闪耀WCN 2026!200余项原创研究入选,其中3项重磅研究将在高影响力临床试验专场亮相
降压目标之争:120 mmHg还是130 mmHg?最新荟萃分析给出答案
肾例明鉴|67岁老人肾衰、咯血、反复感染,元凶竟是两种自身抗体联手!这例罕见肾炎,藏着太多教训
《新英格兰医学杂志》重磅发布奥妥珠单抗ALLEGORY Ⅲ期研究成果,进一步完善其在自身免疫性疾病中的证据链
最新Meta分析:死亡风险随CKM分期进展呈“阶梯式”攀升
WCN2026即将启幕,中国青年学者斩获国际大奖+四大核心主题锚定肾脏医学发展方向
首个突破!FINE-ONE Ⅲ期研究证实非奈利酮为1型糖尿病肾病治疗破局
临床价值深度解析:司美格鲁肽片何以在口服GLP-1RA中脱颖而出?
非奈利酮FIND-CKD研究Ⅲ期结果重磅公布,非糖尿病慢性肾病治疗迎来新方法
临床常见但容易令医师头疼的慢性肾病——微小病变肾病的治疗方案总结归纳,值得收藏!
JAMA子刊重磅:CKM综合征分期越晚,强化降压获益越小?3.3万中国数据给出答案
