- 首页 > 正文
从机制到临床:一文读懂非奈利酮在CKM综合征中的最新证据
发表时间:2026-02-04 10:24:47
心血管-肾脏-代谢(CKM)综合征是心血管疾病(CVD)、慢性肾脏病(CKD)与糖尿病、肥胖等代谢风险因素相互作用形成的复杂病理网络,已成为全球致残和致死的重要原因。近年来,非甾体类盐皮质激素受体拮抗剂(ns-MRA)的出现,为这一综合征的管理带来了新的曙光。Future Cardiology杂志近期发表的一篇综述,系统梳理了ns-MRA在CKM综合征中的当代循证证据。综述重点探讨了其在心力衰竭、CKD及相关并发症中的应用价值,深入至其在心脏、肾脏及血管层面的作用机制,并指出当前证据的局限与未来研究方向,旨在为临床医生提供全面、严谨的学术参考。
CKM综合征是一种系统性病理状态,其特征是CVD、CKD与糖尿病、肥胖等代谢风险因素之间存在复杂的交互作用,这种复杂的病理网络导致了显著的全球疾病负担。传统治疗手段虽有成效,但在改善CKM综合征整体预后方面仍存在局限。近年来,ns-MRA作为一类新兴疗法,展现出显著改善CKM综合征患者心血管和肾脏结局的潜力。
非奈利酮:机制与优势
盐皮质激素受体(MR)的过度激活与氧化应激、炎症和纤维化密切相关,是推动CVD和CKD进展的关键机制。传统的甾体类MRA(如螺内酯、依普利酮)虽有效,但因拮抗效力不足或存在脱靶效应,常导致高钾血症、男性乳房发育等不良反应,限制了其临床应用。
非奈利酮是ns-MRA的代表,其分子结构与甾体类药物截然不同,具有更高的MR选择性和拮抗效力。其非甾体结构使其亲脂性较低,不易穿透血脑屏障,且在心脏和肾脏组织中的分布更为均衡。更重要的是,非奈利酮是一种“被动”MRA,能更有效地阻止MR与醛固酮的结合,并抑制转录辅因子的募集,甚至在无醛固酮存在时也表现出“反向激动剂”特性,从而更彻底地阻断MR的病理信号通路(图1)。
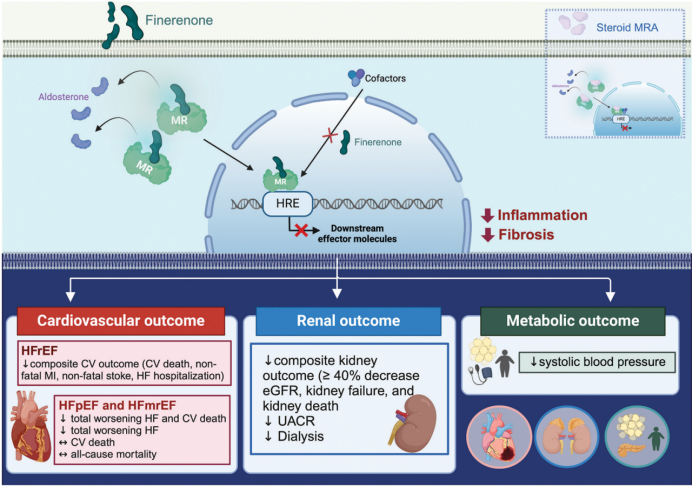
图1. 非奈利酮在CKM综合征中的细胞分子机制和临床结果非奈利酮在
心力衰竭中的证据
目前指南推荐MRA用于射血分数降低的心力衰竭(HFrEF)患者,但对射血分数轻度降低的心力衰竭(HFmrEF)和射血分数保留的心力衰竭(HFpEF)患者,证据尚不充分。里程碑式的TOPCAT研究虽未在整体人群中证实螺内酯对HFpEF的主要复合终点有益,但事后分析提示其可能对特定亚组有益。
FINEARTS-HF研究为非奈利酮在HFmrEF和HFpEF患者中的应用提供了关键证据。该研究纳入6001例左心室射血分数(LVEF)≥40%、纽约心脏协会(NYHA)心功能Ⅱ~Ⅳ级、N末端B型利钠肽前体(NT-proBNP)≥300 pg/ml且年龄≥40岁的患者,患者随机接受非奈利酮(20 mg或40 mg)或安慰剂治疗。结果显示,在中位32个月的随访后,与安慰剂相比,非奈利酮使总体(首次或复发)心力衰竭加重事件和心血管死亡的复合终点风险显著降低16%(HR=0.84),其获益主要源于心力衰竭加重事件的减少。此外,非奈利酮还显著改善了患者的堪萨斯城心肌病问卷(KCCQ)评分。值得注意的是,无论患者LVEF水平、性别或是否联用钠-葡萄糖共转运蛋白2(SGLT-2)抑制剂,非奈利酮的获益均保持一致,提示其可能与现有疗法产生协同效应。
尽管如此,目前关于ns-MRA在HFrEF人群中的大型随机研究仍属空白,其与传统MRA的头对头比较及安全性优势仍需进一步验证。
非奈利酮在糖尿病合并CKD中的证据
传统MRA在2型糖尿病(T2DM)合并CKD中的应用证据有限。FIDELIO-DKD和FIGARO-DKD两项关键研究填补了这一领域的空白。
FIDELIO-DKD研究显示,在伴有白蛋白尿的T2DM合并CKD患者中,中位随访2.6年后,非奈利酮使主要肾脏复合终点(eGFR持续下降≥40%、终末期肾病或肾病相关死亡)风险显著降低18%,次要心血管复合终点(心血管死亡、非致死性心肌梗死、非致死性卒中或心力衰竭住院)也显著降低,白蛋白尿/肌酐比值(UACR)改善。
FIGARO-DKD研究显示,在CKD程度相对较轻的2型糖尿病患者中,中位随访3.4后,非奈利酮使主要心血管复合终点(心血管死亡、非致死性心肌梗死、非致死性卒中或心力衰竭住院)风险显著降低13%,其获益主要由心力衰竭住院风险显著降低29%所驱动。
FIDELITY(FIDELIO-DKD与FIGARO-DKD的汇总分析)进一步证实,非奈利酮可显著降低心血管复合终点和肾脏复合终点风险。而FINE-HEART研究(FIDELIO-DKD、FIGARO-DKD和FINEARTS-HF的汇总分析)则首次在广泛的CKM综合征患者中证实,非奈利酮可显著降低心力衰竭住院、心血管复合终点和肾脏复合终点风险,并降低全因死亡风险。
值得注意的是,这些研究均在患者已接受最大耐受剂量的血管紧张素转换酶抑制剂(ACEI)/血管紧张素Ⅱ受体拮抗剂(ARB)治疗的基础上进行,非奈利酮的额外获益凸显了即使在标准治疗下,肾素-血管紧张素-醛固酮系统(RAAS)仍存在未被充分抑制的空间。
非奈利酮在心房颤动管理中的潜力
心房颤动是CKM综合征4期的常见并发症,与CKD、糖尿病和肥胖等因素密切相关。FINEARTS-HF试验的预设分析显示,非奈利酮在伴或不伴心房颤动的心力衰竭患者中均能有效降低心力衰竭加重事件和心血管死亡的复合终点风险。此外,一项meta分析表明,MRA与安慰剂相比可显著降低心房颤动事件的发生风险。这些数据支持非奈利酮在CKM综合征相关心房颤动管理中的潜在应用。
非奈利酮的细胞与分子作用机制
基础研究揭示了非奈利酮多靶点、多器官的保护作用。在体外和体内模型中,非奈利酮通过多种机制减轻心肾损伤(图2和图3):
1. 抗纤维化与抗炎:有效抑制转化⽣⻓因⼦-β(TGF-β)、如结缔组织⽣⻓因⼦(CTGF)等促纤维化通路,减少胶原沉积和巨噬细胞浸润。
2. 改善细胞功能:在CKD模型中,非奈利酮可恢复心肌细胞钙离子处理蛋白(如PLN、CaMKII)的磷酸化,改善心脏功能;在糖尿病模型中,可减轻心肌和肾小管细胞的凋亡。
3. 改善线粒体功能与自噬:在糖尿病肾病模型中,非奈利酮可恢复线粒体融合/分裂蛋白(Mfn1/2,OPA1,Drp1)的平衡,改善线粒体动力学,并恢复自噬相关蛋白(LC3-II,p62,Beclin-1)的表达。
4. 改善内皮功能:通过减少氧化应激、增强一氧化氮(NO)生物利用度,改善血管内皮功能和血管僵硬度。
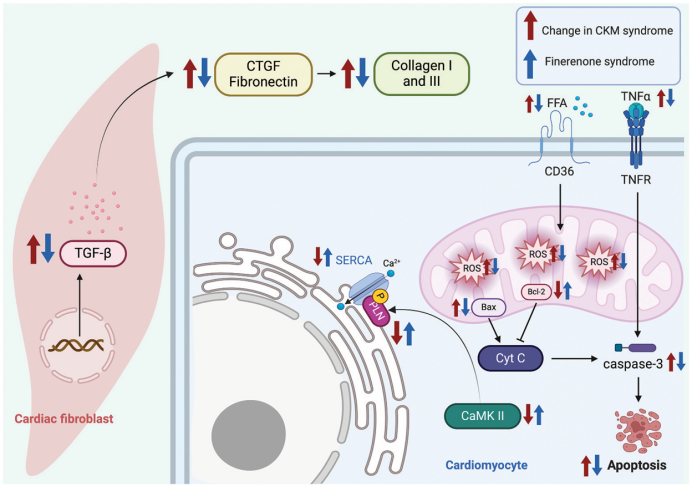
图2. 奈利酮对CKM综合征模型中肌细胞和肌成纤维细胞的潜在影响
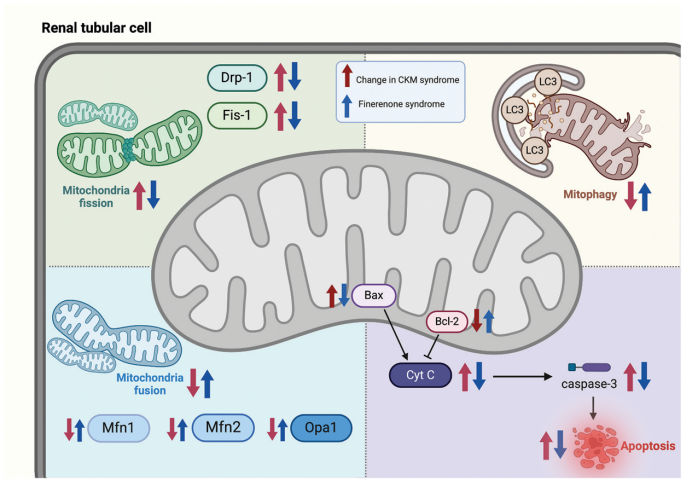
图3. 奈利酮对CKM综合征模型中肾小管细胞的潜在影响
证据缺口与未来展望
尽管来自体外和体内的证据令人鼓舞,但ns-MRA在CKM综合中的作用仍存在显著的知识缺口。例如,目前还缺乏大型RCT评估非奈利酮在HFrEF患者中的疗效和安全性,其在非糖尿病CKD患者中的有效性和安全性也尚不明确,以及在心肌梗死后患者中对心室重构和远期预后的影响尚有待探索。
此外,高钾血症仍是MRA使用的主要顾虑。虽然关键研究中非奈利酮相关的高钾血症发生率可控,但其在真实世界更广泛人群中的安全性仍需真实世界研究来验证。
结语
当前的大型随机对照试验证据充分支持非奈利酮在CKM综合征中的重要地位,它不仅能显著改善HFmrEF/HFpEF患者的心血管结局,还能在T2DM合并CKD患者中同时带来心肾双重获益。其独特的作用机制为CKM综合征的综合管理提供了强有力的工具。未来的研究应聚焦于填补现有证据空白,以期将非奈利酮的治疗获益扩展至更广泛的CKM患者群体。
文献索引:Attachaipanich T, Kaewboot K, Attachaipanich S. Contemporary evidence of non-steroidal mineralocorticoid receptor antagonists in cardio-kidney-metabolic syndrome. Future Cardiol. 2025 Jul 8:1-15.
- 推荐文章
