- 首页 > 正文
肾域华章丨李贵森教授团队:泰它西普在肾移植后复发IgA肾病中的治疗价值探索
发表时间:2026-02-03 14:22:36
引言
IgA肾病(IgAN)是全球最常见的原发性肾小球疾病之一,尽管肾移植是终末期肾病(ESKD)患者的有效治疗手段,但IgAN的复发率极高,严重影响移植肾长期存活。传统免疫抑制方案在此类患者中的疗效有限,迫切需要新的治疗手段。泰它西普作为一种同时阻断B淋巴细胞活化因子(BAFF)和增殖诱导配体(APRIL)的双重抑制剂,近年来在原发性IgAN及系统性红斑狼疮(SLE)中展现出良好的疗效与安全性。四川省人民医院李贵森教授团队7月在Clin Kidney J发表的研究[1],对泰它西普治疗肾移植后复发IgAN的疗效与安全性进行了系统回顾分析,为该领域提供了新的探索证据。此外,近期在布拉格举行的第18届国际IgAN肾病研讨会(IIgANN 2025)上,李贵森教授以壁报的形式分享了该研究结果(摘要号:P-65)[2]。
IgAN患者即使在接受肾移植后,仍有相当比例出现疾病复发。复发的IgAN常表现为持续性蛋白尿、血尿以及移植肾功能减退,最终可能导致移植肾失功。现有治疗策略主要包括糖皮质激素、钙调神经磷酸酶抑制剂(如他克莫司)以及霉酚酸类药物,但对复发IgAN的疗效有限。
近年来,新型药物如耐赋康(布地奈德靶向释放制剂)、司帕生坦(内皮素A型受体与血管紧张素1型受体双阻滞剂)、斯贝利单抗(人源化IgG2单克隆抗体)及盐酸伊普可泮(补体因子B抑制剂)在原发性IgAN中取得积极进展,但其在移植后复发IgAN中的应用证据仍不足。
泰它西普是一种重组融合蛋白,能够同时抑制BAFF和APRIL,阻断B细胞分化及浆细胞生成,减少致病性糖基缺陷IgA1(Gd-IgA1)及相关免疫复合物的形成,从而减轻肾小球系膜沉积及炎症反应。既往Ⅱ期临床试验提示其在原发性IgAN中显著降低蛋白尿,且安全性可接受。基于此,本研究聚焦于其在移植后复发IgAN中的应用。
研究方法
研究设计与对象
该回顾性队列研究在四川省人民医院开展,时间跨度为2023年8月至2025年4月。纳入标准为经肾穿刺活检明确诊断为复发IgAN的肾移植受者,所有患者在接受标准免疫抑制治疗(糖皮质激素、钙调神经磷酸酶抑制剂及霉酚酸类药物)的基础上,额外加用泰它西普。入组患者年龄18~70岁,血压控制在140/90 mmHg以下,且有规律随访记录。排除继发性IgAN、多器官移植、严重肝功能衰竭或心衰等情况。
给药方案
泰它西普初始剂量为每周皮下注射160 mg,部分患者根据耐受性及疾病控制情况调整至240 mg/周。常规治疗还包括RAS系统抑制剂及部分患者联合SGLT2抑制剂。
观察指标
主要终点为治疗6个月时蛋白尿水平的变化,并延伸至12个月随访。完全缓解(CR)定义为24小时蛋白尿<0.3 g/d,且血清肌酐(Scr)升高<15%;部分缓解(PR)定义为尿蛋白较基线下降≥50%且≤3.5 g/d,Scr升高<15%。次要终点包括Scr与估算肾小球滤过率(eGFR)的变化,以及尿红细胞计数、血清白蛋白等指标。安全性评估包括不良事件(AEs)及严重不良事件(SAEs)。
研究结果
基线特征(表1)
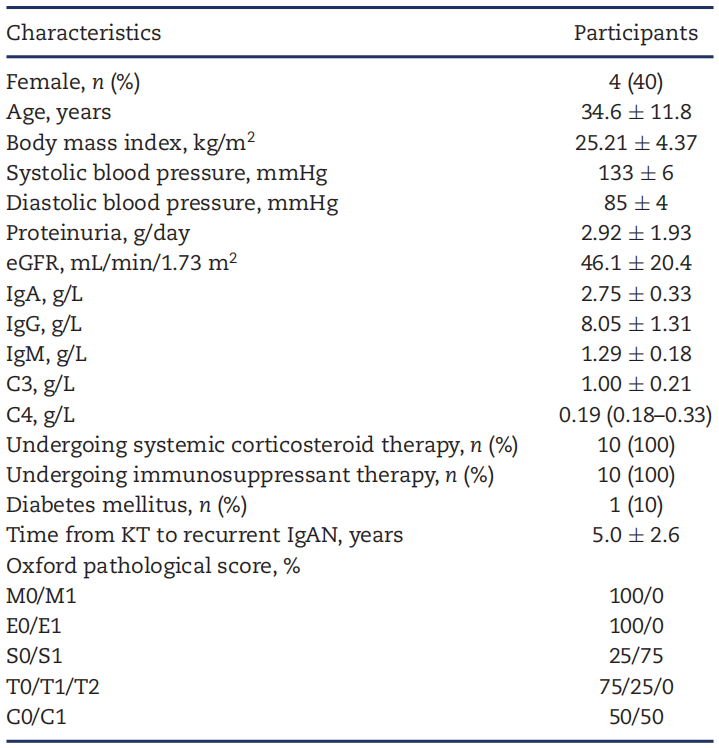
共10例患者纳入,平均年龄34.6±11.8岁,女性占40%。平均体重指数为25.21±4.37 kg/m²,平均从肾移植到IgAN复发的时间为5.0±2.6年。基线蛋白尿水平为2.92±1.93 g/d,平均eGFR为46.1±20.4 mL/min/1.73m²。
根据Oxford MEST-C分型,75%的患者存在节段性硬化(S1),25%伴有小管萎缩/间质纤维化(T1),50%伴有新月体形成(C1)。
表1. 受试者人口统计学和基线特征(引自发表原文)
蛋白尿变化
在6个月随访时,2例患者达到CR,2例达到PR,另有6例(60%)蛋白尿下降超过30%。
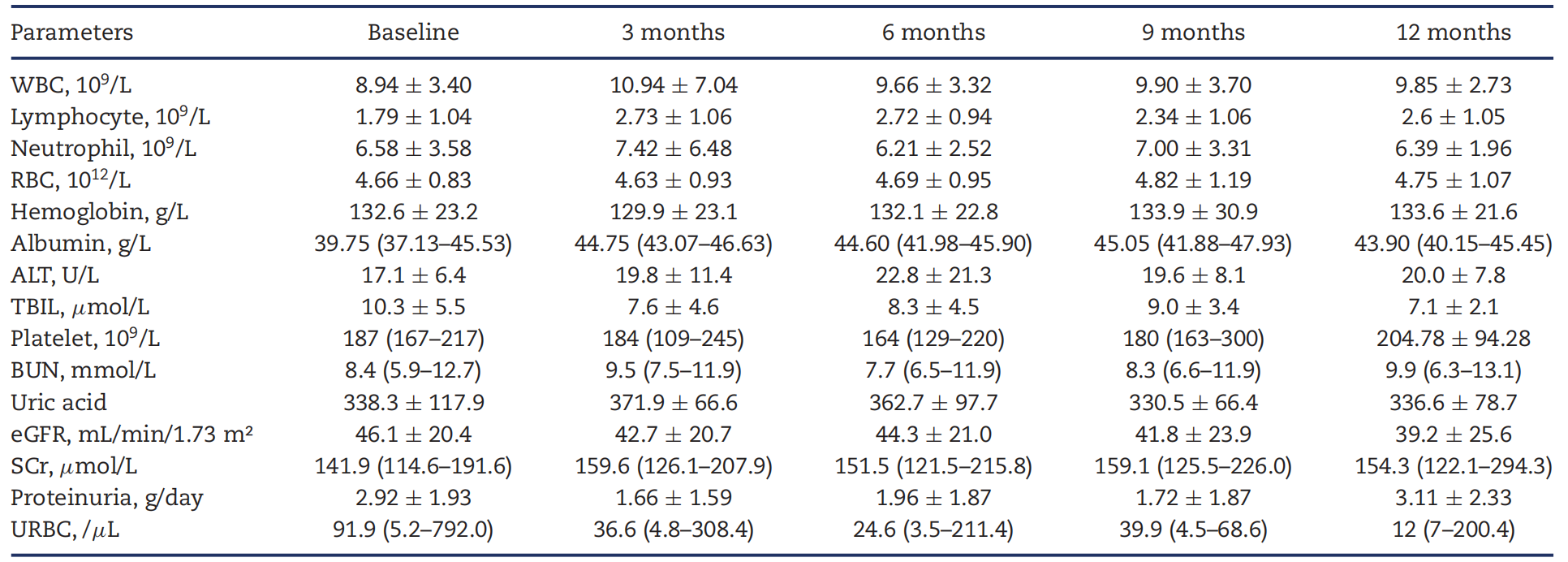
治疗3个月后,平均24小时蛋白尿由基线2.92±1.93 g/d降至1.66±1.59 g/d(下降43.15%),6个月时出现部分反弹(1.96±1.87 g/d,与基线相比下降32.88%),随后在9个月时进一步减少(1.72±1.87 g/d),然而,治疗12个月后再次出现反弹,蛋白尿升高到3.11±2.33 g/d(表2)。值得注意的是,平均血清白蛋白水平随着时间的推移逐渐升高,在12个月的治疗中观察到比基线升高8.86%。
表2. 入组患者实验室参数及变化(引自发表原文)
肾功能与血尿变化
随访期间,Scr和eGFR在9例患者中保持相对稳定(图1b和c)。基线Scr为141.9(114.6–191.6) μmol/L,eGFR为46.1±20.4 ml/(min·1.73m²)。治疗6个月后,eGFR下降至44.3±21.0 ml/min(下降3.84%),Scr上升至151.5(121.5–215.8)μmol/L(下降6.77%)(P>0.05)。治疗监测显示肾功能呈进行性变化,在第9和12个月时,eGFR有可测的下降,同时Scr升高。随访评估显示,治疗后9个月和12个月时eGFR有中度降低,在此期间平均Scr水平保持稳定。
值得注意的是,治疗12个月后,血尿情况明显缓解(图1d)。尿红细胞计数在治疗后明显下降,12个月时较基线下降86.94%。
关于血清尿酸水平,治疗6个月后,10例患者的平均血清尿酸水平呈上升趋势,其中1例患者血清尿酸升高超过30%,3例升高10%~30%,4例呈下降趋势。尽管如此,经12个月治疗后的综合评估显示,患者平均血清尿酸水平仍保持稳定(从338.3±117.9 μmol/L变化至336.6±78.7 μmol/L)。
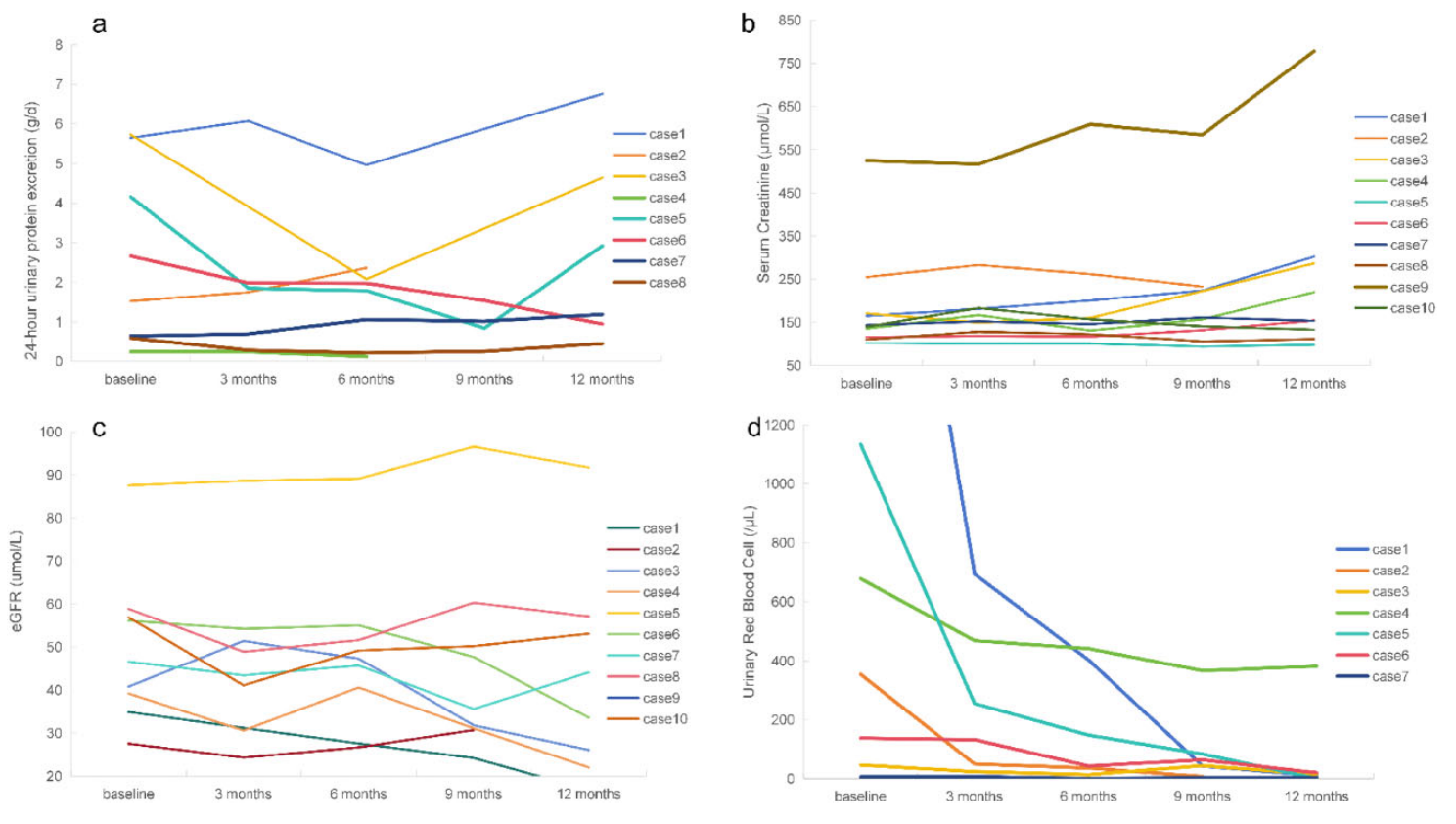
图1. 接受泰它西普治疗的患者从基线至12个月时的蛋白尿、Scr、eGFR和尿RBC计数的变化;(a)24小时蛋白尿,(b) Scr,(c)eGFR,(d)尿RBC计数(引自发表原文)
安全性
治疗过程中未出现死亡或进入ESKD的病例。常见不良事件包括高尿酸血症(40%)、注射部位反应(20%)、头晕(20%)、上呼吸道及泌尿道感染各1例。1例患者在治疗12个月后发生抗体介导性排斥反应,但未导致移植肾失功。整体上,泰它西普耐受性良好,未出现严重不良反应。
讨论
移植后复发IgAN是影响移植肾长期预后的重要挑战,传统免疫抑制方案常难以控制疾病进展。该研究显示,泰它西普能够在部分患者中诱导蛋白尿缓解,并显著改善血尿,且在12个月内维持移植肾功能稳定。这与其抑制B细胞活化、降低Gd-IgA1生成及免疫复合物沉积的机制高度吻合。
与既往研究相比,本研究结果与原发IgAN人群中泰它西普降低蛋白尿的疗效相呼应,进一步提示其可能成为复发IgAN的有效治疗选择。值得注意的是,部分患者在12个月时蛋白尿出现反弹,提示长期疗效仍需进一步随访。
该研究的局限性包括:①回顾性设计,存在选择偏倚及数据缺失和未测量的混杂因素的影响;②缺乏对照组,限制了结果的推广性;③部分患24小时蛋白尿排泄数据不完整,可能影响相关结局的可靠性;④未评估泰它西普治疗后关键生物标志物(包括IgA、IgM、IgG、BAFF/APRIL和Gd-IgA1)的治疗后变化。未来研究应探索不同剂量与疗程的疗效差异,并结合生物标志物(如Gd-IgA1、BAFF/APRIL水平)开展更深入的机制研究。此外,经济因素是真实世界药物可及性的挑战,未来研究应整合社会经济支持策略以提高保留率。
结论
本研究表明,泰它西普在肾移植后复发IgAN患者中显示出良好的安全性和一定的疗效,能够降低蛋白尿水平、改善血尿并维持移植肾功能稳定。其作为B细胞靶向治疗药物,为复发IgAN的管理提供了新的治疗思路。未来需进一步开展大样本、前瞻性随机对照试验,以验证其长期疗效与安全性,并探索其在临床实践中的最优应用模式。
来源:
1.Clin Kidney J. 2025 Jul 16;18(8):sfaf232. doi: 10.1093/ckj/sfaf232. eCollection 2025 Aug.2.Guisen Li. Telitacicept Treatment for Recurrent IgA Nephropathy after Kidney Transplantation. Presented at: IIgANN 2025, Sep. 17-20. P-65.
- 推荐文章
