- 首页 > 正文
精准突破,共起治疗新篇——2025年肾病领域获批及申报中的新药盘点
发表时间:2026-03-13 15:57:52
2025年,肾脏病学领域迎来里程碑式发展。其中,美国食品药品监督管理局(FDA)与中国国家药品监督管理局(NMPA)相继批准10款肾病新药,覆盖慢性肾脏病(CKD)、IgA肾病、狼疮性肾炎(LN)和C3肾小球病(C3G)等多个细分领域。这些新药以精准靶向、机制创新为核心,不仅推动肾病领域治疗从传统对症治疗向精准化、机制导向管理模式转型,更为全球肾病患者实现从“延缓进展”迈向“追求缓解”提供新选择。
2025年10款肾病新药获批上市
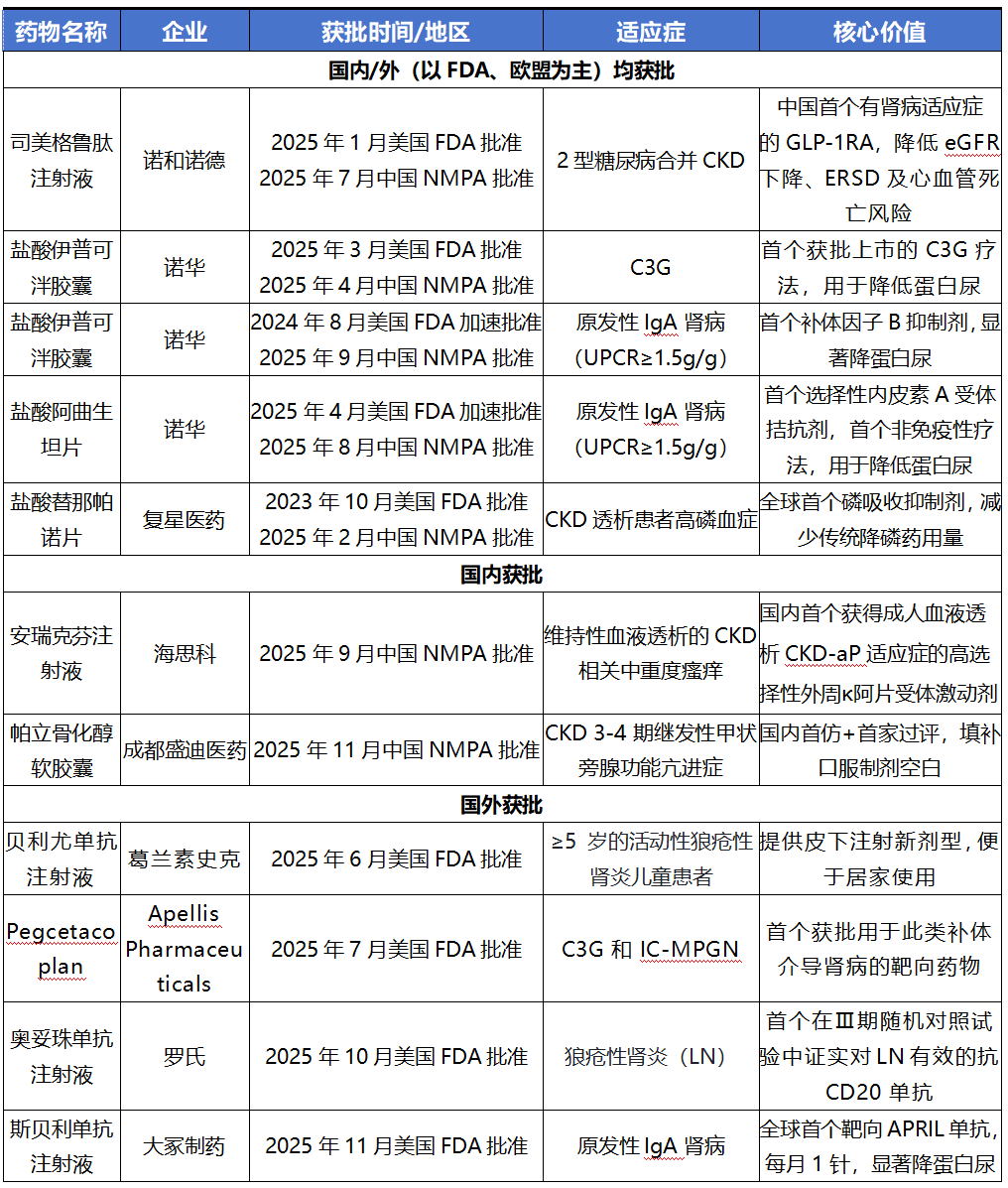
注:UPCR:尿蛋白/肌酐比值;CKD-ap:CKD相关瘙痒症;C3G:C3肾小球病;IC-MPGN:免疫复合物型膜增生性肾炎;GLP-1RA:胰高血糖素样肽-1受体激动剂;eGFR:估算肾小球滤过率;ERSD:终末期肾病;APRIL:增殖诱导配体
(一)国内外均获批
1、司美格鲁肽用于2型糖尿病合并CKD
司美格鲁肽注射液(Semaglutide,诺和泰®)除了获得降糖、心血管获益适应证之外,其肾脏保护作用在今年得到“官方认证”——分别于1月、7月获得美国FDA和中国NMPA批准,用于降低2型糖尿病合并CKD成人患者的eGFR持续下降、ESRD及心血管死亡风险。这一批准基于Ⅲb期FLOW试验数据。该试验显示,在标准治疗基础上联合司美格鲁肽治疗,相比安慰剂可使2型糖尿病合并CKD患者的肾脏复合事件风险降低24%。
司美格鲁肽此次新适应证的获批,不仅使其成为全球首个斩获肾脏保护官方认证的GLP-1RA,更为2型糖尿病合并CKD患者提供降糖、心肾共护的一体化治疗新选择,进一步拓宽了GLP-1RA类药物的临床应用范围。
2、伊普可泮用于C3肾小球病和IgA肾病
今年3月、4月,盐酸伊普可泮胶囊(Iptacopan,飞赫达®)分别获得FDA和中国NMPA批准用于治疗成人C3G,以减少蛋白尿,成为首个获批上市的C3G疗法。这一批准主要是基于关键Ⅲ期APPEAR-C3研究的积极数据。该研究是一项多中心、随机、双盲、安慰剂对照临床试验,结果显示,治疗6个月后,伊普可泮组患者实现了具有临床意义的蛋白尿水平下降,最早在第14天见效,并持续至第12个月。这是伊普可泮在华获批的第一个肾脏病治疗相关适应症。
今年8月、9月,盐酸伊普可泮胶囊(Iptacopan,飞赫达®)分别获得FDA和中国NMPA批准,用于降低有疾病快速进展风险的原发性IgA肾病成人患者的蛋白尿(一般来说,这类患者的UPCR≥1.5 g/g)。该适应症的获批是基于APPLAUSE-IgAN Ⅲ期临床研究的预设中期分析结果。该研究纳入了接受最佳支持治疗(稳定且最大耐受剂量的ACEi或ARB±SGLT2i)≥90天后仍存在蛋白尿(UPCR≥1.0 g/g)的原发性IgA肾病成人患者,结果显示,伊普可泮组与安慰剂组相比,9个月时24h-UPCR显著降低了38.3%(P<0.0001)。伊普可泮此次新适应症的获批,标志着中国IgA肾病治疗正式迈入了靶向补体通路的新阶段。此外,该研究最终分析显示,在两年内,与安慰剂相比,伊普可泮在eGFR斜率方面表现出统计学显著且具有临床意义的改善。据悉,相关数据将于2026年世界肾脏病学大会(WCN)上公布。
3、阿曲生坦获加速批准用于IgA肾病
盐酸阿曲生坦片(Atrasentan,诺锐达®)分别于4月、8月获得美国FDA和中国NMPA批准,成为首个获批用于降低快速进展风险的原发性IgA肾病成人患者蛋白尿水平(一般来说,这类患者的UPCR≥1.5 g/g)的选择性内皮素A受体拮抗剂,并填补了IgA肾病非免疫性治疗的临床空白。Ⅲ期ALIGN研究数据显示,伊普可泮组患者最早在第6周即可观察到UPCR的降低,36周时较安慰剂组24小时UPCR降幅达36.1%。
4、替那帕诺用于降磷
2月26日,全球首个磷吸收抑制剂盐酸替那帕诺片(万缇达®)在中国获批,用于控制对磷结合剂疗效不充分或不耐受的CKD成人透析患者的血清磷水平。其作用机制独树一帜,与传统磷结合剂在肠道内直接结合磷不同,替那帕诺通过抑制肠道上皮细胞的钠氢交换体3(NHE3),减少细胞旁途径的磷吸收,从源头上控制血磷吸收。替那帕诺与现有磷结合剂联合治疗能将血磷达标率提升至63.3%,同时将患者日均服药体积减少超70%。该药已于12月纳入2025年国家医保药品目录,预计2026年1月1日起执行。此外,该药早在2023年10月已获得美国FDA的批准。
(二)国内获批
5、安瑞克芬治疗CKD-aP
9月15日,中国NMPA正式批准国内自主研发的1类创新药安瑞克芬注射液(思舒静®)新增适应证上市,用于治疗接受维持性血液透析的慢性肾脏病相关中重度瘙痒(CKD-aP)的成人患者。作为国内首个获批用于该适应症的高选择性外周κ阿片受体激动剂,安瑞克芬关键Ⅲ期临床试验数据结果显示,治疗12周后,患者每周平均24h最严重瘙痒数字评分量表(WI-NRS)评分至少降低4分的患者比例为37%,而安慰剂组为15%,组间比值比(OR)为3.56(95%CI:2.30~5.50)。
此外,早在5月15日,中国NMPA也批准该药适用于治疗腹部手术后的轻、中度疼痛。
6、帕立骨化醇治疗CKD继发性SHPT
11月24日,中国NMPA正式批准国内3类仿制药帕立骨化醇软胶囊上市并视同过评,填补了该类药物在国内市场的空白。帕立骨化醇作为骨化三醇的活性类似物,是治疗继发性甲状旁腺功能亢进症(SHPT)的核心药物,主要适用于CKD 3-5期患者。而在此之前,该品种原研药尚未在国内获批,此次首仿获批,凭借“视同过评”的质量背书,有望成为该细分领域的标杆产品。
(三)FDA获批
7、贝利尤单抗自动注射器用于儿童LN
6月24日,FDA批准200 mg/mL规格的贝利尤单抗自动注射器用于≥5岁的活动性LN儿童患者,补充了其此前获批的儿童系统性红斑狼疮(SLE)适应症。贝利尤单抗是一种B淋巴细胞刺激因子(BAFF)特异性抑制单克隆抗体。这种皮下注射剂型允许患者居家给药,有助于提高治疗依从性、减少门诊就诊次数,改善儿童患者的真实世界疾病管理效果。
8、Pegcetacoplan用于C3G和IC-MPGN
7月28日,FDA批准Pegcetacoplan用于青少年及成人C3G和IC-MPGN患者,包括移植后复发患者。补体系统激活异常是C3肾小球病和免疫复合物型MPGN的核心发病机制,Pegcetacoplan作为一种新型C3/C3b双靶点抑制剂,能够同时阻断补体经典途径、凝集素途径和旁路途径的激活,直接抑制C3和C5转化酶活性,为阻断肾小球补体沉积和肾损伤提供了新的治疗策略。
此次适应证批准基于26周VALIANT试验的阳性结果,该试验是此类罕见疾病中规模最大的单项临床试验。研究结果显示,治疗26周后,Pegcetacoplan组UPCR较安慰剂组降低68.1%。Pegcetacoplan该适应证的获批,标志着一种长效、精准的治疗策略正式落地,成为首个获批此适应证的靶向药物,有望改变补体介导的肾小球疾病的管理模式,并改善高危患者及移植后患者的预后。
9、奥妥珠单抗治疗LN
10月17日,美国FDA正式批准抗CD20单抗药物——奥妥珠单抗注射液(Obinutuzumab,佳罗华®)用于接受标准治疗的活动性LN成人患者。此次获批是基于Ⅲ期REGENCY研究的显著成果。该研究结果显示,治疗76周后,奥妥珠单抗组完全肾脏缓解率达46.4%,显著高于安慰剂组。
此次适应证获批,使奥妥珠单抗成为全球首个且唯一一个在Ⅲ期随机对照试验中证实对活动性LN有效的抗CD20单抗,为改善患者预后提供新武器。此前,该药物已获批用于慢性淋巴细胞白血病、滤泡性淋巴瘤的治疗。
10、斯贝利单抗治疗IgA肾病
11月25日,美国FDA批准首个APRIL抑制剂斯贝利单抗注射液()用于IgA肾病成人患者。其关键支持性证据来自VISIONARY Ⅲ期研究。该研究为全球最大IgA肾病Ⅲ期试验,中期分析显示,在优化支持治疗(如RASi±SGLT2i)基础上,斯贝利单抗(400 mg每月皮下注射1次)治疗9个月后,患者24h-UPCR较基线降低50.2%,较安慰剂组额外减少51.2%。此次适应证的获批,标志着IgA肾病领域全球首个靶向APRIL抑制剂的创新药正式列入IgA肾病患者的用药清单。
2025年申报上市中的重点药物
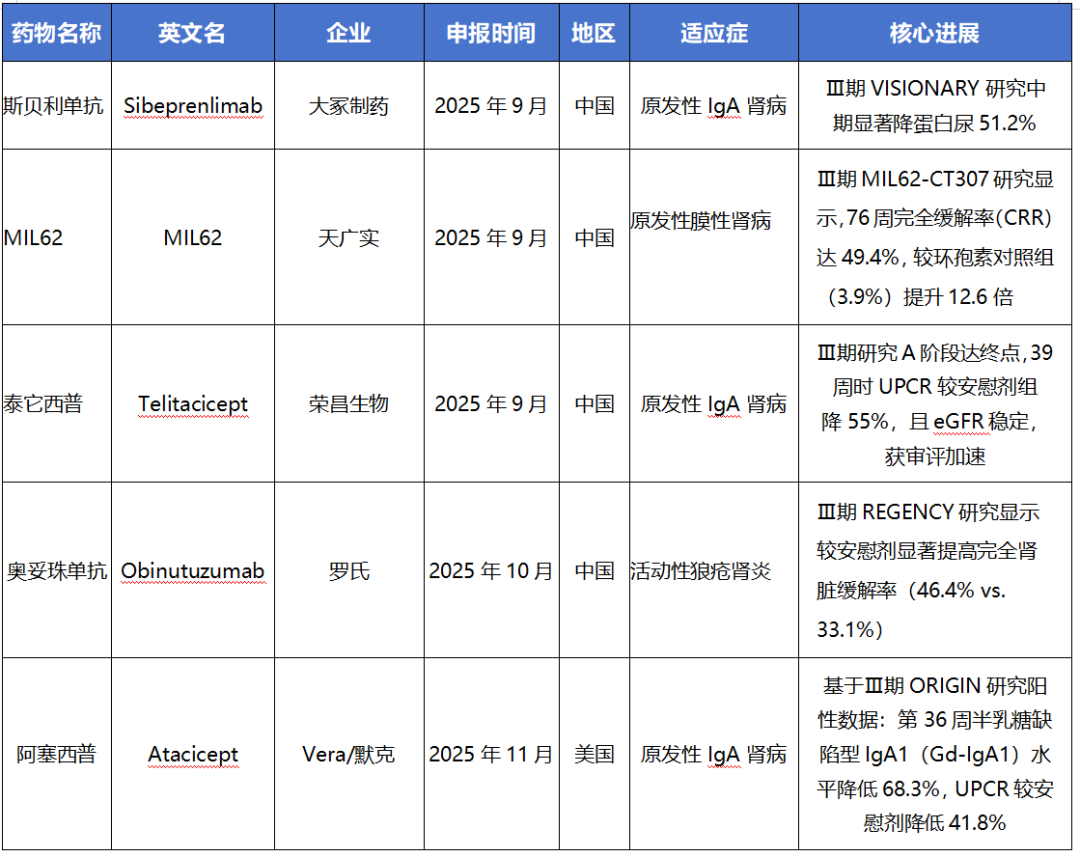
2025年肾病领域的新药突破,不仅丰富了临床治疗武器库,更确立了精准靶向、机制导向的发展方向。随着申报阶段药物的持续推进,以及补体通路、免疫调节、肾脏保护等领域研究的深入,预计未来将有更多创新疗法落地,覆盖更多肾病亚型与特殊人群,进一步提升肾病患者的生存率与生活质量,推动全球肾脏病学治疗进入全新发展阶段。
- 推荐文章
