- 首页 > 正文
年度盘点|SGLT2i治疗常染色体显性多囊肾病(ADPKD)的作用机制与研究进展
发表时间:2026-03-13 16:02:25
SGLT2i的核心作用机制及与ADPKD病理的交集(图1)
(一)血流动力学调节:改善肾小球高滤过与高血压
SGLT2i对肾脏的保护作用首先体现在血流动力学层面。其通过抑制近端肾小管对钠-葡萄糖的重吸收,增加致密斑处氯化钠的递送,激活管-球反馈(TGF),促使腺苷释放并激活入球小动脉A1受体,引发入球小动脉收缩,同时可能通过前列腺素、一氧化氮等途径介导出球小动脉舒张,最终降低肾小球内压力,缓解肾小球高滤过损伤。这种调节可在不影响肾灌注的前提下,减少肾小球滤过率(GFR)的过度消耗,对ADPKD患者尤为关键。
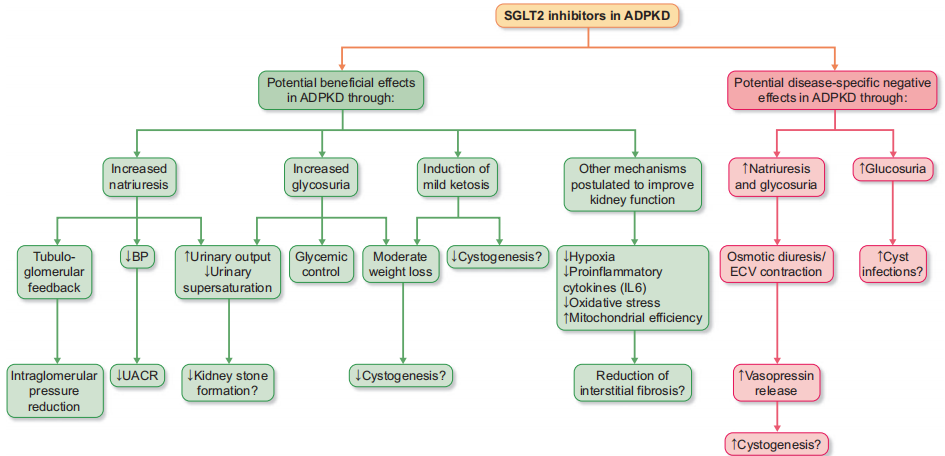
图1. SGLT2i在ADPKD中的作用机制
ADPKD早期即存在肾小球高滤过,伴随肾内血流灌注紊乱:囊肿扩张压迫肾内小动脉,引发肾素-血管紧张素-醛固酮系统(RAAS)过度激活、交感神经张力升高及内皮功能障碍,约70%患者30岁前出现高血压,而高血压又会加速肾囊肿进展与肾功能衰退。SGLT2i可通过温和的利钠利尿作用降低血容量,且不会引发反射性心动过速或醛固酮水平异常;同时其能抑制夜间交感神经活性、改善内皮功能,在糖尿病及非糖尿病人群中可实现收缩压平均降低2.5 mmHg、舒张压降低1.5 mmHg,为ADPKD患者的血压控制提供了新路径。
(二)代谢重编程:逆转Warburg效应与调控酮体生成
ADPKD囊肿上皮细胞存在典型的Warburg样代谢重塑,即有氧条件下优先进行糖酵解以满足快速增殖的生物合成需求,这一过程加剧了细胞内代谢应激。SGLT2i可通过降低胰岛素水平、升高胰高血糖素,诱导肝脏酮体生成,模拟热量限制状态,为肾脏、心脏等器官提供替代能量底物,同时抑制合成代谢信号,重塑细胞能量平衡。
此外,SGLT2i可激活腺苷酸活化蛋白激酶(AMPK),上调过氧化物酶体增殖物激活受体γ共激活因子1α(PGC1α),改善线粒体功能、减少氧化应激,并促进底物从葡萄糖向脂质的转换,增强脂肪酸氧化。这一代谢切换不仅能纠正囊肿上皮细胞的糖酵解依赖,还可通过减少糖酵解中间产物的积累,限制囊肿的增殖与扩张。同时,SGLT2i可抑制肾小管尿酸转运体URAT1,降低血清尿酸水平,缓解ADPKD患者常见的高尿酸血症及其介导的RAAS激活、血管炎症与纤维化。
(三)抑制囊肿增殖与液体分泌
ADPKD的囊肿扩张依赖上皮细胞异常增殖与氯离子驱动的液体分泌。前者与哺乳动物雷帕霉素靶蛋白复合物1(mTORC1)通路过度激活密切相关,而AMPK是mTORC1的负向调控因子。SGLT2i诱导的轻度能量缺乏状态可激活AMPK,进而抑制mTORC1通路,减少囊肿上皮细胞增殖。在液体分泌方面,囊肿纤维化跨膜电导调节因子(CFTR)是核心效应蛋白,AMPK可通过转录和翻译后修饰抑制CFTR功能,减少氯离子及相关液体的分泌,从而延缓囊肿体积增大。
(四)改善肾内缺氧与免疫微环境
囊肿扩张会压迫周围肾单位及肾小管毛细血管,导致局部缺血缺氧,激活缺氧诱导因子-1α(HIF-1α),进而促进血管生成、细胞外基质重塑与上皮增殖,加速肾间质纤维化。SGLT2i可降低近端肾小管转运负荷,减少氧耗,改善肾组织氧合,并通过上调HIF-2α促进促红细胞生成素合成,提升血红细胞比容,增强整体氧输送能力。
在免疫层面,ADPKD肾脏内巨噬细胞呈现“先促炎后促纤维化”的表型转换:早期M1型巨噬细胞释放肿瘤坏死因子α(TNF-α)、白细胞介素6(IL-6)等促炎因子,损伤肾小管;后期M2型巨噬细胞分泌转化生长因子β(TGF-β),驱动间质纤维化。SGLT2i可抑制M1型巨噬细胞活化,并限制M2型巨噬细胞向纤维化亚型转化,同时通过抑制Toll样受体4(TLR4)和核因子κB(NF-κB)通路,减少炎症因子释放,改善肾脏免疫微环境。
SGLT2i治疗ADPKD的临床证据
(一)临床前研究:模型依赖性的疗效差异
动物实验为SGLT2i的应用提供了初步依据,但结果存在模型特异性(表1)。在携带ANKS6突变的Han:SPRD大鼠(近端肾小管囊肿模型)中,达格列净可改善肾功能、降低尿白蛋白,但对囊肿负荷无显著影响;而双靶点SGLT1/2抑制剂根皮苷则能显著降低囊肿体积密度和肾脏重量,其疗效优于选择性SGLT2i,推测与SGLT1对致密斑葡萄糖感知的调节有关。与之相反,在常染色体隐性多囊肾病PCK大鼠(远端肾小管囊肿模型)中,达格列净反而增加了囊肿体积和尿白蛋白,可能是渗透性应激对远端肾小管囊肿的特异性影响。
表1. SGLT2i治疗PKD的动物实验
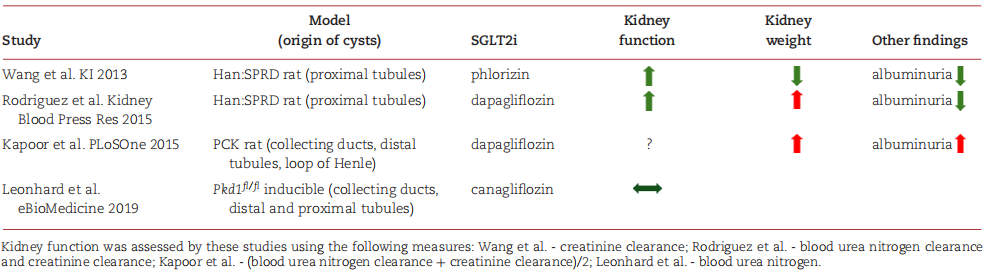
需注意的是,SGLT2i可能激活血管加压素通路:在糖尿病大鼠模型中,伊格列净治疗可使尿血管加压素水平升高,肾内V2受体和磷酸化水通道蛋白2表达上调,而血管加压素的激活可能加速ADPKD囊肿进展,这也是其临床应用的主要顾虑。
(二)临床研究:初步探索与矛盾结果
受限于入组限制,ADPKD患者的SGLT2i临床数据多来自回顾性研究和小样本试验。一项针对20例ADPKD患者的回顾性研究显示,达格列净治疗3.5个月后,患者GFR从47.9 ml/min/1.73m²降至40.8 ml/min/1.73m²,身高校正肾脏总体积(htTKV)从599 ml/m增至617 ml/m,提示存在短期血流动力学影响;但血红蛋白水平从13.1 g/dl升至14.0 g/dl,符合SGLT2i的促红细胞生成效应。
在接受托伐普坦治疗的ADPKD患者中,联合达格列净的小样本随机试验显示出积极信号:6个月后,联合治疗组eGFR下降斜率从-3.66 ml/min/1.73m²/年改善至1.03 ml/min/1.73m2/年,htTKV增长率从5.04%降至-0.44%,尽管患者血浆血管加压素水平有所升高,但未出现明显安全事件。此外,美国退伍军人队列研究发现,SGLT2i初始治疗3个月内eGFR下降速度快于二肽基肽酶4抑制剂(DPP4i),但3-12个月时eGFR斜率更稳定,提示其对肾功能的长期影响或呈“先降后稳”的特征。
(三)正在进行的关键临床试验
目前两项大型Ⅲ期临床试验(DAPA-PKD和STOP-PKD)正在推进,旨在明确SGLT2i的疗效与安全性。DAPA-PKD计划纳入400例18~75岁ADPKD患者,以24个月MRI检测的TKV变化为主要终点,同时评估eGFR斜率和心血管结局;STOP-PKD则纳入420例高进展风险患者(携带PKD1截断突变或eGFR年下降>3 ml/min/1.73m²),以36个月eGFR斜率为核心终点。两项试验均排除托伐普坦使用者,以避免联合治疗的容量紊乱风险,其结果将为SGLT2i的临床定位提供高级别证据。目前已开展的SGLT2i治疗PKD的临床研究见表2。
表2. SGLT2i治疗PKD患者的临床研究概览
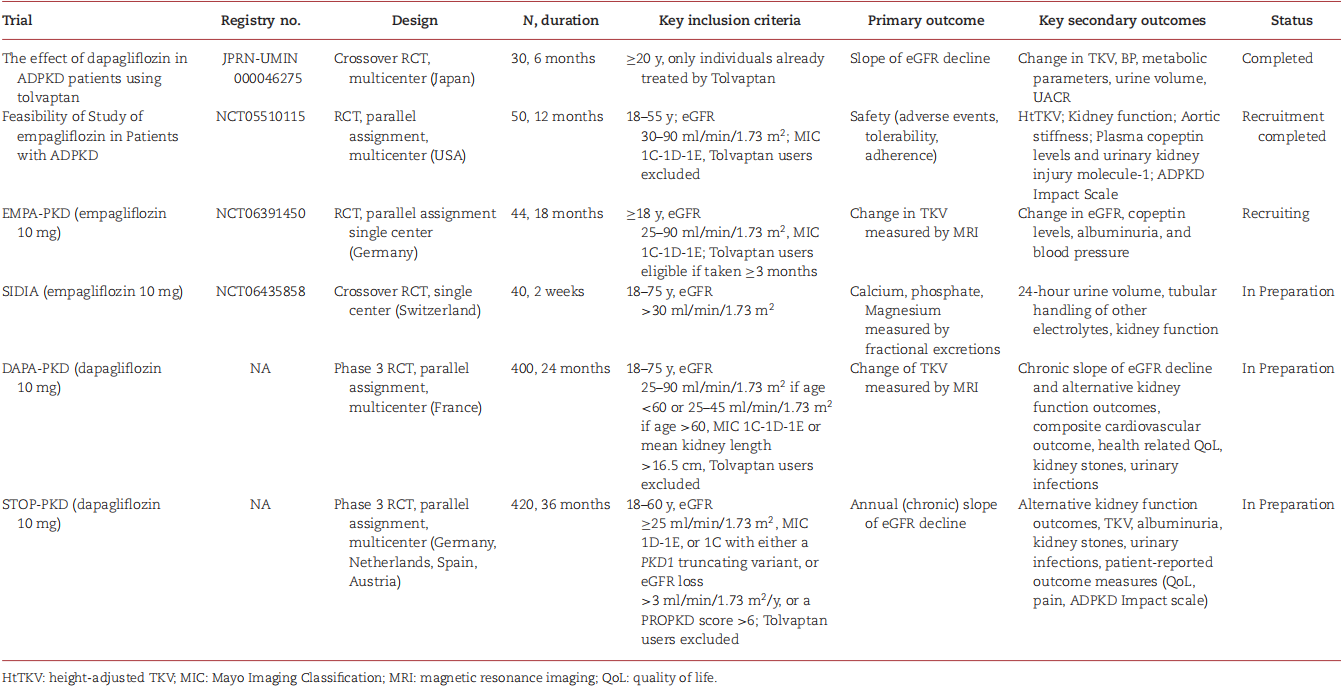
SGLT2i应用于ADPKD的挑战与未来方向
(一)遗传异质性的精准分层
ADPKD存在显著遗传异质性,约78%患者为PKD1突变、15%为PKD2突变,其余7%为DNAJB11、ALG8、ALG9等罕见基因型。现有临床试验多富集于PKD1/2快速进展型患者,而DNAJB11等基因型常伴随更严重的肾间质纤维化,其对SGLT2i的应答可能与经典型不同。例如,SGLT2i的抗纤维化作用可能对间质纤维化为主的亚型更有益,但相关数据尚未见报道。未来需按基因型、疾病进展风险及合并症进行分层,实现SGLT2i的精准应用。
(二)安全性争议的澄清
血管加压素激活和容量紊乱是SGLT2i用于ADPKD的核心安全顾虑。一方面,SGLT2i引发的渗透性利尿可能升高血浆渗透压,刺激血管加压素释放,而血管加压素V2受体是托伐普坦的作用靶点,其激活会通过环磷酸腺苷(cAMP)通路促进囊肿分泌;另一方面,ADPKD患者本身存在肾脏浓缩功能异常,联合SGLT2i可能增加脱水风险。已有病例报告显示,1例ADPKD患者接受达格列净1年,TKV增加40%、eGFR显著下降,但停药后指标部分逆转,提示需警惕个体差异。未来研究需明确SGLT2i对血管加压素通路的影响阈值,以及与托伐普坦联用的安全性。
(三)联合治疗的探索
托伐普坦作为唯一获批药物,与SGLT2i的联合应用是潜在方向。二者机制互补:托伐普坦抑制血管加压素V2受体以减少囊肿液体分泌,SGLT2i则改善血流动力学和代谢紊乱。日本一项小型交叉试验已证实,托伐普坦联合达格列净可改善eGFR斜率并抑制TKV增长,但样本量小、随访短的局限性明显。未来需开展大样本长期研究,明确联合方案的获益-风险比。
结语
ADPKD是累及肾脏和心血管系统的复杂性疾病,托伐普坦的局限性凸显了治疗方案的迫切需求。SGLT2i通过血流动力学调节、代谢重编程、免疫调控等多重机制,与ADPKD病理生理形成精准契合,尽管早期临床证据存在矛盾,但小样本试验已显示出延缓囊肿进展和保护肾功能的潜力。正在开展的Ⅲ期临床试验将为其疗效和安全性提供关键数据,而基于基因型的分层研究、联合治疗探索及长期安全性监测,将是推动SGLT2i成为ADPKD辅助或一线治疗方案的核心方向。2025年KDIGO指南的谨慎态度提示,在获得确证性证据前,SGLT2i的应用需严格遵循临床试验框架,同时关注患者个体差异,平衡获益与风险。
参考文献
1.Bou Antoun MT, et al. J Am Soc Nephrol . 2025 Nov 10. doi: 10.1681/ASN.0000000943. Online ahead of print.2.Mülle BL, et al. Nephrol Dial Transplant. 2025; 40: 2231-2238.
- 推荐文章
