- 首页 > 正文
Baxdrostat在CKD合并难治性高血压患者中的疗效与安全性——一项Ⅱ期FigHTN试验解读
发表时间:2026-02-03 11:11:16

一、研究背景
高血压既是CKD最常见的并发症,也是其进展至终末期肾病和心血管事件的首要危险因素。全球逾8.5亿人罹患CKD,其中90%合并高血压,而血压达标率仍低于20%。醛固酮通过促进远曲小管钠重吸收、钾排泄及肾脏炎症纤维化,直接推动血压升高和肾功能恶化。传统盐皮质激素受体拮抗剂(MRA)如螺内酯、依普利酮虽可阻断醛固酮信号,但存在高钾血症、男性乳腺发育等副作用,且长期应用可因“逃逸现象”致血浆醛固酮反跳。
Baxdrostat(CIN-107)是一种高选择性醛固酮合成酶抑制剂(ASI),对CYP11B2的抑制强度为CYP11B1的100倍,理论上可在不影响皮质醇合成的前提下持续降低醛固酮。前期BrigHTN 2期试验显示,baxdrostat对难治性高血压具显著降压作用,但CKD人群的安全有效性尚待验证。为此,研究者设计了FigHTN试验,旨在评估baxdrostat在合并CKD且血压未控制患者中的疗效、安全性及蛋白尿改善潜力。
二、研究设计
FigHTN是一项美国78家中心参与的随机、双盲、安慰剂对照、平行分组、剂量探索2期临床试验(NCT05432167)。受试者年龄≥18岁,估算肾小球滤过率(eGFR)25~75 ml·min-1·1.73 m-2,尿白蛋白/肌酐比值(UACR)≥100 mg/g,坐位诊室收缩压(SBP)140~180 mmHg(非糖尿病)或130~180 mmHg(合并2型糖尿病),且已稳定使用最大耐受剂量ACEI或ARB≥4周。排除1型糖尿病、糖化血红蛋白>10.5%、合用MRA或保钾利尿剂者。
经过5周筛查(含2周导入期)后,195例受试者按1:1:1随机分入低剂量组(LD,0.5 mg/日,第3周可上调至1 mg)、高剂量组(HD,2 mg/日,可上调至4 mg)或安慰剂组,治疗26周,随访2周。随机分层因素包括基线SGLT2抑制剂使用、SBP≤155或>155 mmHg、eGFR≤45或>45 ml·min-1·1.73 m-2。
主要终点为第26周坐位诊室SBP较基线的变化(baxdrostat合并组 vs. 安慰剂);次要终点为LD、HD组分别与安慰剂的SBP差异;探索终点包括SBP<130 mmHg达标率、舒张压(DBP)、UACR、eGFR变化;安全性终点为治疗期不良事件(TEAE)、高钾血症、低血压、肾功能急性波动等。
三、基线特征
195例受试者平均年龄66±11岁,女性32%,白人58%,80%合并2型糖尿病,平均SBP 151.2±13.1 mmHg,平均eGFR 44±14 ml·min-1·1.73 m-2,中位UACR 714 mg/g,76%呈大量白蛋白尿。三组背景治疗相似:ACEI/ARB使用率100%,SGLT2抑制剂33%,利尿剂44%,平均使用2.8种降压药。
四、研究结果
1、主要终点:第26周baxdrostat合并组SBP下降15.2 mmHg,安慰剂组下降7.2 mmHg,安慰剂校正后LS均差为-8.1 mmHg(95%CI:-13.4~-2.8,P=0.003,图1)。
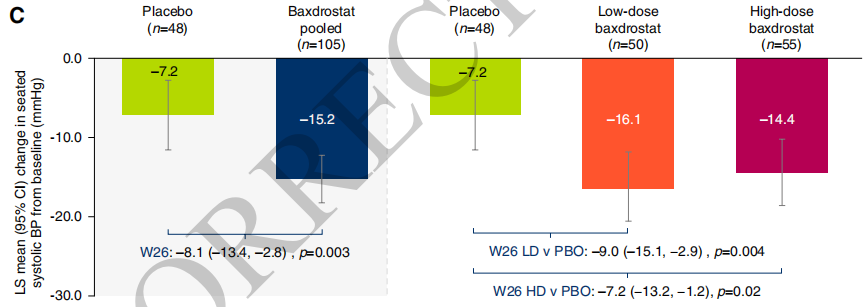
图1. SBP较基线的变化
2、次要终点:LD组与安慰剂组的LS均差为-9.0 mmHg(P=0.004),HD组与安慰剂组的LS均差为-7.2 mmHg(-13.2~-1.2,P=0.02,图1)。
3、血压达标:SBP<130 mmHg的比例在baxdrostat合并组为36%,安慰剂组17%;LD组42%,HD组31%。此外,baxdrostat合并组舒张压较安慰剂多降4.8 mmHg。
4、蛋白尿:第26周,baxdrostat合并组UACR几何均值下降55.2%,安慰剂组下降6.1%,校正后净下降约50%;LD组下降52%,HD组下降58%(图2)。
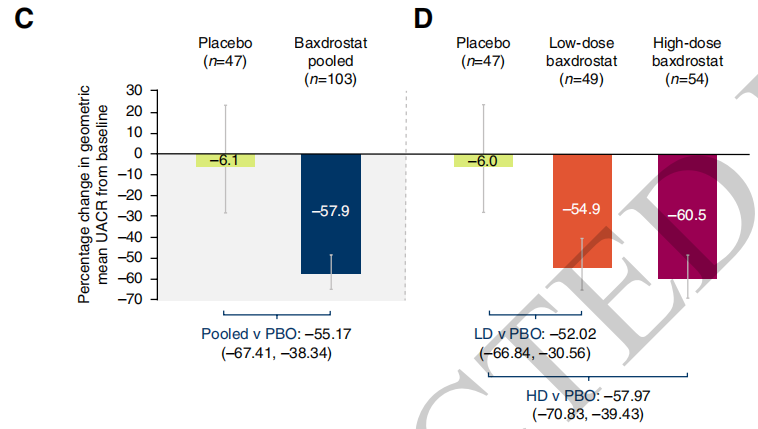
图2. UACR较基线的变化
5、肾功能:第26周,与安慰剂组相比,baxdrostat合并组、LD组、HD组eGFR较基线下降分别为2.3 、1.8、2.8 ml·min-1·1.73 m-2。15%接受Baxdrostat治疗的受试者在两次随访间的估算肾小球滤过率(eGFR)下降幅度超过 30%(低剂量组10人,占比 15%;高剂量组9人,占比14%),而接受安慰剂治疗的受试者中,这一比例为 11 人(占比17%)。在两次随访间eGFR下降幅度超过50%的情况中,随机分配至安慰剂组的受试者有1人,而随机分配至Baxdrostat组的受试者无此情况。
6、药效学:血清醛固酮浓度下降,肾素活性代偿性升高,符合ASI作用机制。
7、安全性
Baxdrostat合并组78%、安慰剂55%出现TEAE;严重TEAE分别为9%与3%。高钾血症是最常见的并发症,baxdrostat合并组为41%(LD 32%,HD 51%)vs. 安慰剂5%;3例(LD 2,HD 1)出现高钾相关严重不良事件,9例(7%)因此停药。第二常见的不良事件是血肌酐升高,baxdrostat合并组20% vs 安慰剂8%,均为非严重。
研究中期收紧了血钾>5.5 mmol/L时的剂量下调规则,高钾事件多发生于修订前入组人群。
四、讨论与意义
FigHTN首次证实,在已接受标准RAS阻断的CKD合并未控制高血压患者中,baxdrostat 0.5~4 mg/日可额外降低SBP约7~9 mmHg,同时使蛋白尿下降50%以上,且降压与降蛋白尿效应在4周内显现并持续26周。该幅度优于既往强化降压(SBP目标<120 mmHg)带来的16% UACR减少,提示baxdrostat可能通过减少醛固酮介导的肾小球高滤过、炎症及纤维化,产生独立于血压的肾脏保护作用。尽管高钾血症发生率升高,但多数为轻中度、可逆,且与剂量相关;无死亡或肾上腺功能不全病例。结合SGLT2抑制剂可降低ASI/MRA相关高钾风险的循证证据,未来联合方案值得进一步探索。
五、展望
基于FigHTN的积极结果,两项全球Ⅲ期研究(NCT06742723;NCT06268873)已启动,将评估baxdrostat联合达格列净对CKD进展及心肾硬终点的影响;另一项Prevent-HF研究(NCT06677060)则聚焦心衰住院与心血管死亡。若Ⅲ期结果重复Ⅱ期疗效并证实长期安全,baxdrostat有望成为继SGLT2抑制剂、非甾体MRA之后,CKD合并高血压及蛋白尿治疗的新支柱,实现“血压-蛋白尿-心肾事件”三重获益。
Dwyer JP, et al. JASN 00: 1–13, 2025. doi: https://doi.org/10.1681/ASN.0000000849
- 推荐文章
