- 首页 > 正文
三例IgA肾病罕见病因与病理类型的临床启示
发表时间:2026-03-15 10:15:09
编者按
IgA肾病作为最常见的原发性肾小球疾病,其临床表现与病理类型多样,病因机制复杂。除经典的免疫介导途径外,临床实践中常遇到由感染、特殊病理形态或先天血管畸形等罕见因素诱发或共存的病例,为诊断与治疗带来挑战。本文汇编三篇摘要,分别揭示了麻风感染、特殊膜增生样病理形态及先天性肝外门体分流(Abernethy畸形)与IgA肾病的内在关联,旨在拓宽临床视野,强调全面评估与个体化治疗的重要性。
一、麻风病合并系膜增生性IgA肾病:感染与免疫的复杂交织
麻风病是一种慢性细菌性疾病,可引发多种形式的肾脏损害,但系膜增生性IgA肾病作为麻风病的并发症并不常见。这种IgA肾病并非由麻风分枝杆菌直接导致,而是在感染活动期及结节性红斑麻风反应时,免疫复合物相互作用的结果。此外,抗麻风药物也可能造成肾脏损伤。
本病例由来自尼泊尔的Susmin Karki等[1]报道。患者为一名18岁男性麻风病患者,因全身水肿、气短、乏力及尿量减少就诊。患者已根据尼泊尔国家麻风病指南完成了18个月的联合化疗(MDT),药物包括氨苯砜、利福平及氯法齐明,同时耳部存在多发结节(图1)。
图1
尿液分析显示肾病范围蛋白尿,血肌酐进行性升高,抗核抗体(ANA)阳性。皮肤slit涂片检查提示多菌型皮损。肾脏病理检查显示系膜增生性IgA肾病。
直接免疫荧光(DIF)结果:系膜区可见IgA(3+)颗粒状沉积,IgG、IgM阴性;补体C3(3+)颗粒状沉积于系膜区,C1q阴性;κ轻链阴性,λ轻链(2+)颗粒状沉积于系膜区。
经胸超声心动图(TTE)提示心力衰竭伴中值射血分数(HFmrEF),射血分数为45%~50%,合并Ⅲ级左心室舒张功能障碍(LVDD)。患者计划行动静脉内瘘(AVF)成形术以建立血液透析通路。
治疗方案包括:碳酸氢钠、雷尼替丁、醋酸钙、维生素D、哌唑嗪、卡维地洛、硝苯地平、地尔硫卓、铁剂、叶酸、甲钴胺,以及氨苯砜、利福平、氯法齐明,同时联用糖皮质激素并维持血液透析。患者皮肤损害经治疗后好转,但仍需持续依赖透析。
临床启示:随着肾活检的广泛应用,麻风病患者中肾小球肾炎的检出率逐渐升高。本病例提示,年轻麻风病患者可出现复杂的临床表现,合并肾脏损害进而发展为肾病。及时诊断并处理感染及肾脏并发症,对改善患者预后至关重要。
二、膜增生样IgA肾病:肝脏疾病关联与病理特殊性
抗肾小球基底膜(抗GBM)病由循环致病性自身抗体引发,这类抗体特异性靶向表达于器官基底膜的自身抗原。当肾脏受累时,可导致新月体形成及肾小球坏死,免疫荧光通常表现为IgG和C3沿肾小球基底膜呈线性沉积。然而,该病也可表现为寡免疫型肾损伤。
新月体性IgA肾病(IgAN)是IgA肾病的一种特殊亚型,以病情进展迅速、预后差为特征。既往尚无新月体性IgA肾病合并抗GBM肾炎,且无肾小球基底膜免疫复合物沉积的病例报道。
西北大学附属医院/西安市第三医院喻倩等[2]报道了一例病例。患者为34岁男性,主因“肉眼血尿伴发热半月,血肌酐(Scr)升高2天”入院。血清抗GBM抗体阳性,肾活检提示新月体性肾小球肾炎,但免疫荧光显示肾小球基底膜无免疫球蛋白沉积,仅系膜区可见IgA和C3呈团块状沉积(图2)。
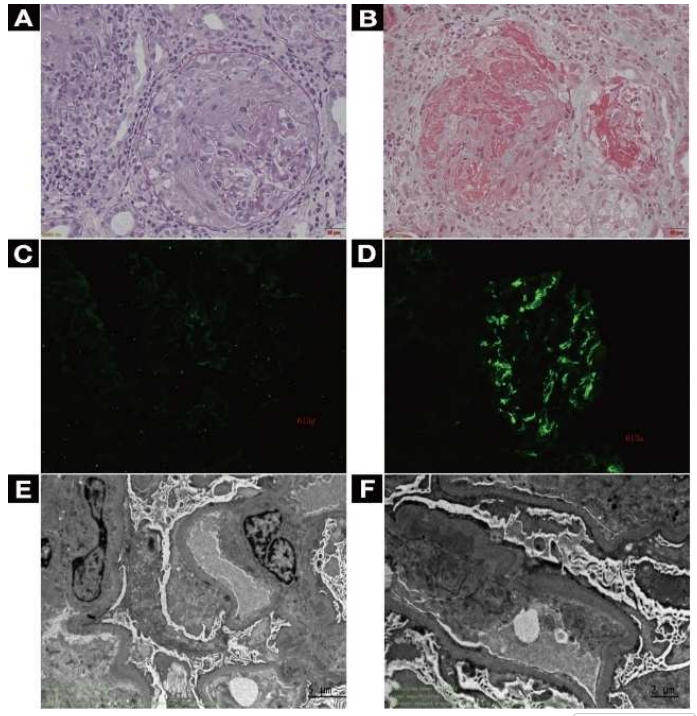
图2
最终诊断为新月体性IgA肾病合并抗GBM肾炎。患者接受了静脉甲泼尼龙冲击联合环磷酰胺治疗,并在住院期间完成22次血浆置换,直至抗GBM抗体转阴。患者血肌酐水平未下降,需持续依赖透析治疗。
讨论及启示:该病例是首例报道的“新月体性IgA肾病合并无典型基底膜沉积的抗GBM肾炎”的特殊组合。治疗对血清肌酐降低无应答且需持续透析,凸显了这种共存疾病的复杂性和严重性。需进一步研究以更好地理解其潜在机制,并为这类罕见且具有挑战性的肾脏疾病开发更有效的治疗策略。
三、阿伯内西畸形合并IgA肾病:门体分流绕过肝脏清除的新机制
阿伯内西畸形(Abernethy,AM)是一种罕见的先天性门体分流畸形,极少合并肾小球肾炎。门体分流在IgA肾病(IgAN)发病机制中的因果关联及临床意义尚不明确,尤其是在肝硬化发生前出现的Ⅱ型阿伯内西畸形。
西北大学附属医院/西安市第三医院Wenya Cao等[3]报道的这例阿伯内西畸形合并IgA肾病患者为30岁男性,因肾病综合征就诊,经活检确诊为系膜增生性IgA肾病(Lee氏分级Ⅲ级,牛津分型M1E0S1T0-C1型)。同期诊断为肝硬化(CT:结节性改变、脾肿大、静脉曲张)及后续复发性肝性脑病。
血管造影检查明确诊断为Ⅱ型阿伯内西畸形(图3):存在一条粗大的门静脉-腔静脉分流道,直接引流入下腔静脉,伴门静脉流速减慢及血管走形异常。这是全球范围内少数几例报道的阿伯内西畸形合并IgA肾病的病例之一。
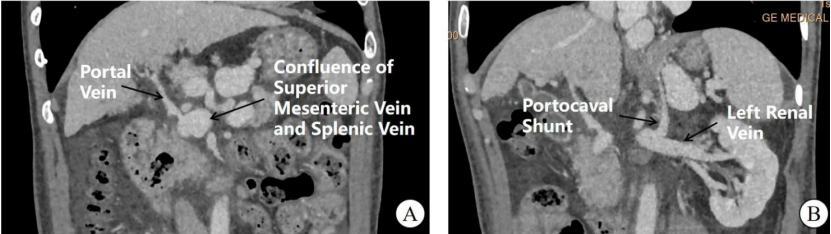
图3
由于试行夹闭分流道存在出血风险,患者于2023年5月接受了腹腔镜下分流道部分封堵术(封堵80%)。术后门静脉流速较基线水平(6~8 cm/s)提升至10~12 cm/s。关键的是,蛋白尿从术前基线水平(0.8~2.1 g/24h)在术后2个月显著降至0.19~0.29 g/24h,且未增加免疫抑制强度。在10个月的随访中,肝性脑病发作次数也明显减少。
讨论
该病例为门体分流直接导致IgA肾病的假说提供了强有力的临床证据,且其机制独立于肝硬化相关因素。分流道部分矫正后,蛋白尿显著且持续下降,分流诱导的肝清除旁路是通过系统性IgA免疫复合物积聚导致肾小球损伤的关键机制。即使存在已形成的肝硬化,这种改善仍发生,表明分流效应可能独立于肝硬化本身或与之叠加。这些结果与既往关于分流矫正后肾脏功能改善的有限观察结果一致。值得注意的是,本病例表明,当因安全性问题无法完全闭合时,部分分流闭塞仍可获得显著的肾脏获益。
这一罕见病例提示,Ⅱ型阿伯内西畸形可能是IgA肾病的潜在病因。靶向分流道干预后蛋白尿的显著减少,为“异常门体分流直接影响IgA肾病活动”提供了确凿的临床证据。尽早干预分流道或可延缓肾小球损伤进展。
这些发现提示:对于原因不明的IgA肾病患者,尤其是合并肝脏异常时,应考虑评估是否存在门体分流;而分流道矫正可能成为一种非免疫抑制的治疗选择。未来需多中心研究进一步证实该方案的长期获益。
小结
以上三个案例从感染、特殊病理、血管畸形不同角度,揭示了IgA肾病病因与表现的多样性。它们共同提示临床医生:对于IgA肾病患者,尤其是临床表现不典型、疗效不佳或合并肝病患者,应拓宽诊断思路,积极寻找潜在感染灶、进行详细的病理复核并考虑是否存在血管畸形等罕见病因。精准的病因诊断是实施针对性治疗(如抗感染、处理原发肝病、手术矫正分流)和改善预后的关键。
参考文献
[1]Susmin Karki, et al. Hansen's Disease Associated with Mesangioproliferative IgA Nephropathy: A Case Report. Poster No.:C0462. 23rd Asian Pacific Congress of Nephrology. Dec 5-7, 2025.
[2]喻倩, et al. Crescentic IgAN and anti-GBM nephritis without linear GBM immunofluorescence: A first report case. Poster No.:C0500. 23rd Asian Pacific Congress of Nephrology. Dec 5-7, 2025.
[3]Wenya Cao, et al. Case report: A Rare Case of IgA Nephropathy Associated with Type II Abernethy Malformation. Poster No.:C0505. 23rd Asian Pacific Congress of Nephrology. Dec 5-7, 2025.
IgA肾病作为最常见的原发性肾小球疾病,其临床表现与病理类型多样,病因机制复杂。除经典的免疫介导途径外,临床实践中常遇到由感染、特殊病理形态或先天血管畸形等罕见因素诱发或共存的病例,为诊断与治疗带来挑战。本文汇编三篇摘要,分别揭示了麻风感染、特殊膜增生样病理形态及先天性肝外门体分流(Abernethy畸形)与IgA肾病的内在关联,旨在拓宽临床视野,强调全面评估与个体化治疗的重要性。
一、麻风病合并系膜增生性IgA肾病:感染与免疫的复杂交织
麻风病是一种慢性细菌性疾病,可引发多种形式的肾脏损害,但系膜增生性IgA肾病作为麻风病的并发症并不常见。这种IgA肾病并非由麻风分枝杆菌直接导致,而是在感染活动期及结节性红斑麻风反应时,免疫复合物相互作用的结果。此外,抗麻风药物也可能造成肾脏损伤。
本病例由来自尼泊尔的Susmin Karki等[1]报道。患者为一名18岁男性麻风病患者,因全身水肿、气短、乏力及尿量减少就诊。患者已根据尼泊尔国家麻风病指南完成了18个月的联合化疗(MDT),药物包括氨苯砜、利福平及氯法齐明,同时耳部存在多发结节(图1)。

图1
尿液分析显示肾病范围蛋白尿,血肌酐进行性升高,抗核抗体(ANA)阳性。皮肤slit涂片检查提示多菌型皮损。肾脏病理检查显示系膜增生性IgA肾病。
直接免疫荧光(DIF)结果:系膜区可见IgA(3+)颗粒状沉积,IgG、IgM阴性;补体C3(3+)颗粒状沉积于系膜区,C1q阴性;κ轻链阴性,λ轻链(2+)颗粒状沉积于系膜区。
经胸超声心动图(TTE)提示心力衰竭伴中值射血分数(HFmrEF),射血分数为45%~50%,合并Ⅲ级左心室舒张功能障碍(LVDD)。患者计划行动静脉内瘘(AVF)成形术以建立血液透析通路。
治疗方案包括:碳酸氢钠、雷尼替丁、醋酸钙、维生素D、哌唑嗪、卡维地洛、硝苯地平、地尔硫卓、铁剂、叶酸、甲钴胺,以及氨苯砜、利福平、氯法齐明,同时联用糖皮质激素并维持血液透析。患者皮肤损害经治疗后好转,但仍需持续依赖透析。
临床启示:随着肾活检的广泛应用,麻风病患者中肾小球肾炎的检出率逐渐升高。本病例提示,年轻麻风病患者可出现复杂的临床表现,合并肾脏损害进而发展为肾病。及时诊断并处理感染及肾脏并发症,对改善患者预后至关重要。
二、膜增生样IgA肾病:肝脏疾病关联与病理特殊性
抗肾小球基底膜(抗GBM)病由循环致病性自身抗体引发,这类抗体特异性靶向表达于器官基底膜的自身抗原。当肾脏受累时,可导致新月体形成及肾小球坏死,免疫荧光通常表现为IgG和C3沿肾小球基底膜呈线性沉积。然而,该病也可表现为寡免疫型肾损伤。
新月体性IgA肾病(IgAN)是IgA肾病的一种特殊亚型,以病情进展迅速、预后差为特征。既往尚无新月体性IgA肾病合并抗GBM肾炎,且无肾小球基底膜免疫复合物沉积的病例报道。
西北大学附属医院/西安市第三医院喻倩等[2]报道了一例病例。患者为34岁男性,主因“肉眼血尿伴发热半月,血肌酐(Scr)升高2天”入院。血清抗GBM抗体阳性,肾活检提示新月体性肾小球肾炎,但免疫荧光显示肾小球基底膜无免疫球蛋白沉积,仅系膜区可见IgA和C3呈团块状沉积(图2)。

图2
最终诊断为新月体性IgA肾病合并抗GBM肾炎。患者接受了静脉甲泼尼龙冲击联合环磷酰胺治疗,并在住院期间完成22次血浆置换,直至抗GBM抗体转阴。患者血肌酐水平未下降,需持续依赖透析治疗。
讨论及启示:该病例是首例报道的“新月体性IgA肾病合并无典型基底膜沉积的抗GBM肾炎”的特殊组合。治疗对血清肌酐降低无应答且需持续透析,凸显了这种共存疾病的复杂性和严重性。需进一步研究以更好地理解其潜在机制,并为这类罕见且具有挑战性的肾脏疾病开发更有效的治疗策略。
三、阿伯内西畸形合并IgA肾病:门体分流绕过肝脏清除的新机制
阿伯内西畸形(Abernethy,AM)是一种罕见的先天性门体分流畸形,极少合并肾小球肾炎。门体分流在IgA肾病(IgAN)发病机制中的因果关联及临床意义尚不明确,尤其是在肝硬化发生前出现的Ⅱ型阿伯内西畸形。
西北大学附属医院/西安市第三医院Wenya Cao等[3]报道的这例阿伯内西畸形合并IgA肾病患者为30岁男性,因肾病综合征就诊,经活检确诊为系膜增生性IgA肾病(Lee氏分级Ⅲ级,牛津分型M1E0S1T0-C1型)。同期诊断为肝硬化(CT:结节性改变、脾肿大、静脉曲张)及后续复发性肝性脑病。
血管造影检查明确诊断为Ⅱ型阿伯内西畸形(图3):存在一条粗大的门静脉-腔静脉分流道,直接引流入下腔静脉,伴门静脉流速减慢及血管走形异常。这是全球范围内少数几例报道的阿伯内西畸形合并IgA肾病的病例之一。

图3
由于试行夹闭分流道存在出血风险,患者于2023年5月接受了腹腔镜下分流道部分封堵术(封堵80%)。术后门静脉流速较基线水平(6~8 cm/s)提升至10~12 cm/s。关键的是,蛋白尿从术前基线水平(0.8~2.1 g/24h)在术后2个月显著降至0.19~0.29 g/24h,且未增加免疫抑制强度。在10个月的随访中,肝性脑病发作次数也明显减少。
讨论
该病例为门体分流直接导致IgA肾病的假说提供了强有力的临床证据,且其机制独立于肝硬化相关因素。分流道部分矫正后,蛋白尿显著且持续下降,分流诱导的肝清除旁路是通过系统性IgA免疫复合物积聚导致肾小球损伤的关键机制。即使存在已形成的肝硬化,这种改善仍发生,表明分流效应可能独立于肝硬化本身或与之叠加。这些结果与既往关于分流矫正后肾脏功能改善的有限观察结果一致。值得注意的是,本病例表明,当因安全性问题无法完全闭合时,部分分流闭塞仍可获得显著的肾脏获益。
这一罕见病例提示,Ⅱ型阿伯内西畸形可能是IgA肾病的潜在病因。靶向分流道干预后蛋白尿的显著减少,为“异常门体分流直接影响IgA肾病活动”提供了确凿的临床证据。尽早干预分流道或可延缓肾小球损伤进展。
这些发现提示:对于原因不明的IgA肾病患者,尤其是合并肝脏异常时,应考虑评估是否存在门体分流;而分流道矫正可能成为一种非免疫抑制的治疗选择。未来需多中心研究进一步证实该方案的长期获益。
小结
以上三个案例从感染、特殊病理、血管畸形不同角度,揭示了IgA肾病病因与表现的多样性。它们共同提示临床医生:对于IgA肾病患者,尤其是临床表现不典型、疗效不佳或合并肝病患者,应拓宽诊断思路,积极寻找潜在感染灶、进行详细的病理复核并考虑是否存在血管畸形等罕见病因。精准的病因诊断是实施针对性治疗(如抗感染、处理原发肝病、手术矫正分流)和改善预后的关键。
参考文献
[1]Susmin Karki, et al. Hansen's Disease Associated with Mesangioproliferative IgA Nephropathy: A Case Report. Poster No.:C0462. 23rd Asian Pacific Congress of Nephrology. Dec 5-7, 2025.
[2]喻倩, et al. Crescentic IgAN and anti-GBM nephritis without linear GBM immunofluorescence: A first report case. Poster No.:C0500. 23rd Asian Pacific Congress of Nephrology. Dec 5-7, 2025.
[3]Wenya Cao, et al. Case report: A Rare Case of IgA Nephropathy Associated with Type II Abernethy Malformation. Poster No.:C0505. 23rd Asian Pacific Congress of Nephrology. Dec 5-7, 2025.
- 推荐文章
聚焦CKM综合管理,恒格列净相关复方制剂赋能心-肾-代谢多重获益
年度盘点丨周晓玲教授:肥胖相关慢性肾脏病的诊治进展
肾例明鉴丨服药后肺肾接连“报警”!20岁女生的惊魂经历:元凶竟是治疗甲亢的丙硫氧嘧啶
谨慎“跟风养生”!Omega-3、生酮饮食、禁糖等营养宣传需辩证对待
肾识百科丨肾友想生娃?4类可怀情况 + 3类禁忌,提前看清不踩坑
警惕身体的“代谢紊乱风暴”!代谢综合征——引人关注的肾脏“杀手”
频繁饮用碳酸饮料与痴呆症风险增加有关
SC0062胶囊:IgA肾病治疗新突破,斩获欧盟孤儿药资格
全球仅报道100余例,“小群体”的隐忧人生——胶原Ⅲ肾病,一种全球罕见的肾病
减重为基,全面获益——中国首个原研GLP-1/GIP双受体激动剂瑞普泊肽重磅来袭
最新进展|自体干细胞疗法(双侧肾脏注射Rilparencel)治疗糖尿病肾病,可显著减缓肾功能下降速率
2026版亚洲儿科肾脏病学会(AsPNA)感染相关性肾小球肾炎管理指南重磅发布
“化繁为简”:司美格鲁肽在临床中的优势选择
首部《IgA肾病临床实践60问(2026版)》专家共识重磅发布,布地奈德肠溶胶囊解锁对因治疗密码
云顶新耀引进全球首创双靶点多肽新药MT1013,肾科布局迈向新阶段
春节护心肾·健康“零”负担——CKM患者佳节饮食管理全攻略
肾例明鉴 | 年轻宝妈产后5天肌酐急剧上升伴抽搐,危难之际揪出罕见真凶,挽救年轻宝妈生命!
三例IgA肾病罕见病因与病理类型的临床启示
家庭血压监测不容忽视,研究提示夜间高血压加速慢性肾病进展
NEJM重磅: VALIANT研究证实Pegcetacoplan有效降低C3肾小球病与免疫复合物型MPGN患者蛋白尿达68%
北大医院赵明辉/崔昭团队专题综述:Hippo通路——新月体肾小球肾炎免疫治疗的潜在靶点
站上心肾代谢的主舞台——2025口服司美格鲁肽年度进展盘点
北大张宏、张月苗教授团队锁定IgA肾病肠-肾轴致病源头:回肠IgA⁺β7⁺细胞扮演重要角色
2026年1月国际肾脏病学领域六大要闻:诊疗与营养策略迎来新变革
心血管-肾脏-代谢综合征的干预新策略:从药物联合到综合管理——来自APCN 2025上的新证据
指南共识丨欧洲抗风湿病联盟(EULAR)关于伴肾脏受累的系统性红斑狼疮的管理建议(2025更新版)解读
寻找最优解:狼疮肾炎的机制探索、靶向新药与跨界疗法丨APCN 2025壁报精选
心肾代谢协同施治:重塑CVD合并糖尿病诊疗新范式——基于中国原研SGLT2i恒格列净的重大突破
年度盘点 | 赵建荣教授:介入肾脏病学研究进展
泰它西普治疗IgA肾病的临床探索:疗效、个体化应用与联合策略新证据
十年肾病治错方向?肾活检误诊,真相竟是代谢性肾病
重磅!近20位肾脏病学者入选爱思唯尔2025“中国高被引学者”榜单
关注!北京大学第一医院2025年度十大新闻
年度盘点丨张涛、程震教授:膜性肾病研究最新进展——PLA2R抗体致病性得到确认,免疫学缓解成为治疗目标
肾例明鉴丨眼底出血+大量蛋白尿,44岁男性恶性高血压的“非典型”病因——动脉粥样硬化性肾动脉狭窄
年度盘点丨心血管-肾脏-代谢(CKM)医学2025年重要进展:从“多病共存”迈向“多器官同步事件链阻断”
年度盘点|范秋灵教授:肿瘤相关性血栓性微血管病的发病机制与诊治进展
肾识百科丨肾脏病与性生活的那些事
创新·共管|沁泽华夏CKM创新大会冰城召开,共话心肾代谢领域新未来
年度盘点丨阳晓教授:腹膜透析相关性腹膜炎的管理策略新进展
最新专家共识解析非奈利酮在老年疾病中的应用
学术纵横|肌少症不仅是肌力低、肌量低,还与DKD相互促进、互为因果
年度盘点丨马坤岭教授:2025年糖尿病肾病发病机制及诊治新进展
KI最新发布:Sefaxersen靶向肝脏中补体B因子的基因,有望成为IgA肾病首个RNA疗法
学术纵横|膜性肾病研究新进展:疾病特征、预后评估与治疗创新
北大张宏、周绪杰教授团队最新成果发现预测IgA肾病激素疗效关键遗传标志物,为个体化治疗铺路
KI最新发布:补体C3-IgA共定位与IgAN及IgAVN患者的肾脏活动性损伤(M+E+C评分)相关
超越传统MRA,非奈利酮在原发性醛固酮增多症中的独特价值与应用前景
肾例明鉴丨八旬老人ANCA又升高、肾功能恶化,一定是血管炎复发吗?重复肾活检揭开罕见新发IgA肾病真相
APCN 2025壁报精选:IgA肾病基础研究进展综述
风暴已至,力挽狂澜——CKM进展期的“攻”与“守”
年度盘点 | 饶佳教授:腺相关病毒载体基因治疗相关血栓性微血管病的研究进展
腹膜透析与营养管理:技术进步与临床挑战
关注晚期CKD的SGLT2i疗效验证与基因治疗新浪潮
年度盘点 | 刘同强教授:血液透析患者不宁腿综合征的研究进展
