- 首页 > 正文
CKD患者血压管理的破局之道——许钟镐教授详解临床“秘籍”
发表时间:2026-02-04 13:27:12
编者按
全球约8.5亿慢性肾脏病(CKD)患者中,80%~85%伴有高血压[1],这不仅加速肾功能下降,还显著增加心血管事件风险。面对不同类型CKD患者的血压控制争议与治疗难点,如何科学设定目标、精准用药、兼顾透析期管理?在本文中,吉林大学第一医院许钟镐教授结合最新指南与循证证据和临床经验,为您呈现CKD血压管理的“破局之道”。
专家简介

许钟镐 教授
大学第一医院肾脏内科主任、教授、博士生导师
中华医学会肾脏病学分会委员
中国医师协会肾内科医师分会常务委员
在国际知名刊物上发表了业内价值较高的系列论文,承担多项国家级、省部级科研项目,获科技成果及医疗成果奖多项
一、CKD患者的血压控制目标及争议
1. CKD患者的血压控制目标不同类型的CKD患者,血压控制目标存在差异,具体见表1[2]。
表1. 不同类型CKD患者的血压控制目标
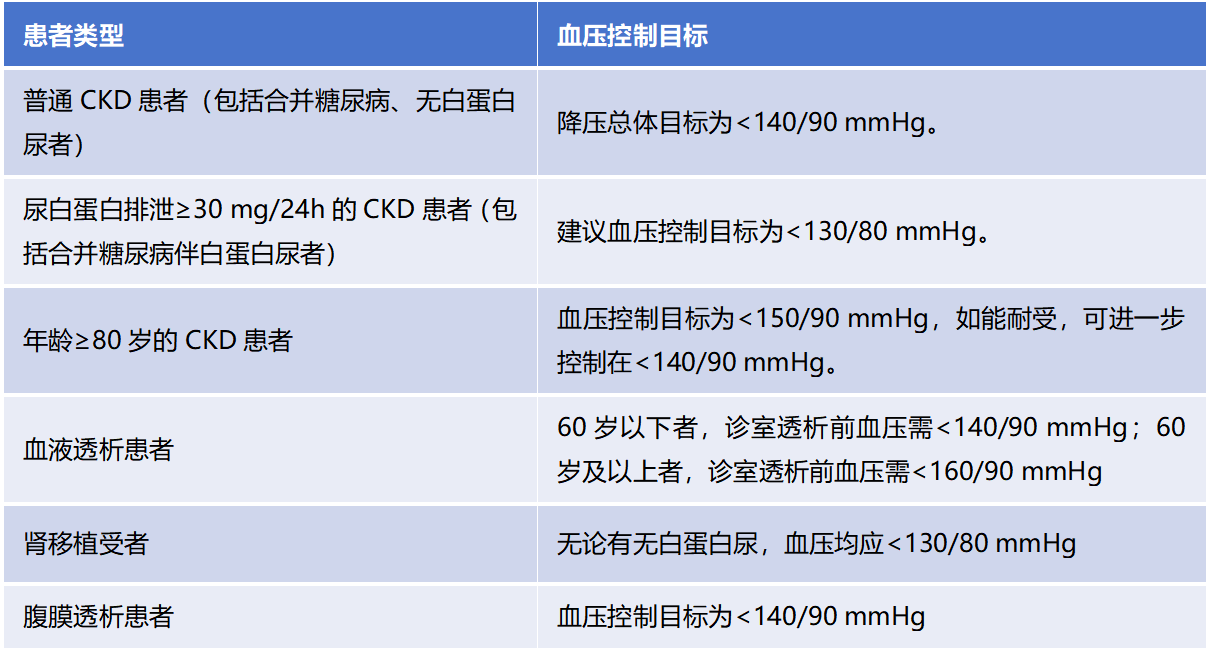
2.CKD患者血压管理目标的争议
SPRINT研究的CKD亚组分析数据表明120 mmHg的控制目标能够带来更多获益,可使全因死亡率降低28%,心血管风险降低43%[3]。但学界对这一研究存在争议。有观点认为该研究的入选人群不能很好地代表现有CKD患者群体,其排除了糖尿病、蛋白尿>1 g/d、重度CKD患者[eGFR<60 ml/(min·1.73m²)]以及50岁以下患者,且研究人群年龄较大、肾功能仅轻度下降,与真实世界的CKD患者群体存在区别。此外,Cochrane循证数据库的一项荟萃研究表明,CKD患者较低的血压控制目标(130/80 mmHg或更低)相比标准目标(140~160/90~100 mmHg或更低),在总死亡率、总严重不良反应事件、总心血管事件、因心血管事件死亡和ESRD进展方面可能并无区别,且提示更低的血压目标可能会降低患者依从性[4]。
二、CKD患者高血压的药物治疗
1.常用降压药物及用药方案
CKD合并高血压的血压管理措施见图1[5]。CKD患者常用的降压药物主要包括血管紧张素转换酶抑制剂(ACEI)/血管紧张素Ⅱ受体拮抗剂(ARB)、钙通道阻滞剂(CCB)、利尿剂。其中,ACEI/ARB是药物治疗的基础,单药治疗时首选ACEI或ARB,双药治疗推荐ACEI/ARB+CCB或利尿剂方案,两药方案控制不佳时,可采用三药联合(ACEI/ARB+CCB+利尿剂),三药方案无效时可加用盐皮质激素受体拮抗剂或其他降压药(如α、β受体阻滞剂)。
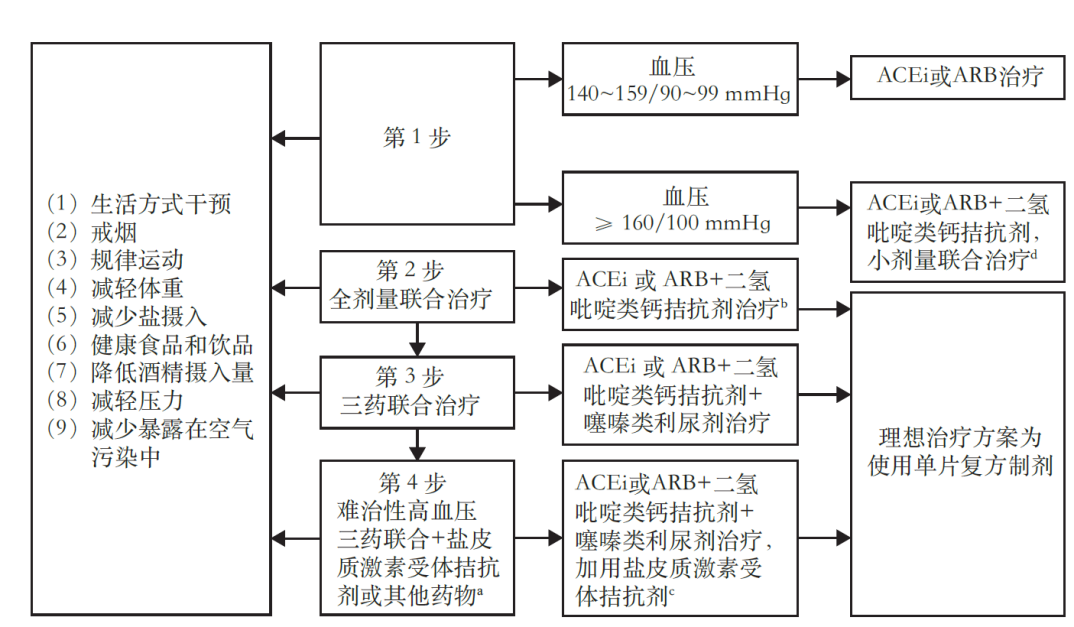
图1. CKD合并高血压的血压管理
应用ACEI/ARB时,应注意:
①需排除禁忌证(双侧肾动脉狭窄、孤立肾伴肾动脉狭窄、高钾血症、妊娠等);
②建议从小剂量开始,对于高血压合并糖尿病肾病者,用至可耐受最大剂量;
③建议CKD3、4期的患者初始剂量减半,严密监测血钾、血肌酐和eGFR并及时调整药物剂量和剂型;
④用药2~4周后血肌酐较基础值升高<30%时仍可谨慎使用,超过30%时可考虑减量或停药;
⑤血液透析患者使用RASi应监测血钾和肌酐水平;
⑥醛固酮拮抗剂与ACEI或ARB联用可能加速肾功能恶化和增加高钾血症风险;⑦不建议ACEI和ARB两药联合应用;不推荐两种RASi联用。
3、晚期CKD患者是否停用ACEI/ARB的争议
尚未进入肾脏替代治疗的晚期CKD患者[eGFR<30 ml/(min·1.73m²)]是否应用RAS抑制剂,目前学术界仍有争议。一项研究将411例患者随机分为继续使用和停止使用RAS抑制剂组,3年后,两组eGFR的差异没有统计学意义,但继续使用组有较好预后的趋势;继续用药组进展为ESKD的风险低于停药组。亚组分析显示,2型糖尿病患者继续应用RAS抑制剂预后更佳,而1型糖尿病患者停止应用有更好趋势,提示1型和2型糖尿病肾病的治疗方式可能需要区别对待[6]。
三、透析患者高血压的管理
血液透析治疗的患者中,高血压的发生与多个因素有关,包括量超负荷、动脉僵硬度、交感神经和肾素-血管紧张素-醛固酮系统活性增强、内皮功能障碍以及促红细胞生成素刺激剂的使用。应在消除或控制危险因素的基础上,对血液透析患者进行容量控制、降压药物选择应用以及透析间期的血压管理,控制透析高血压(图2)[7]。
而对于腹膜透析患者,首先需对残余肾功能和腹膜功能进行评估,对有残余肾功能的患者,使用袢利尿剂有助于减轻水钠潴留;对于残余肾功能丧失者,可以强化腹膜透析,增加葡萄糖透析液的浓度以及适当使用艾考糊精透析液[2]。
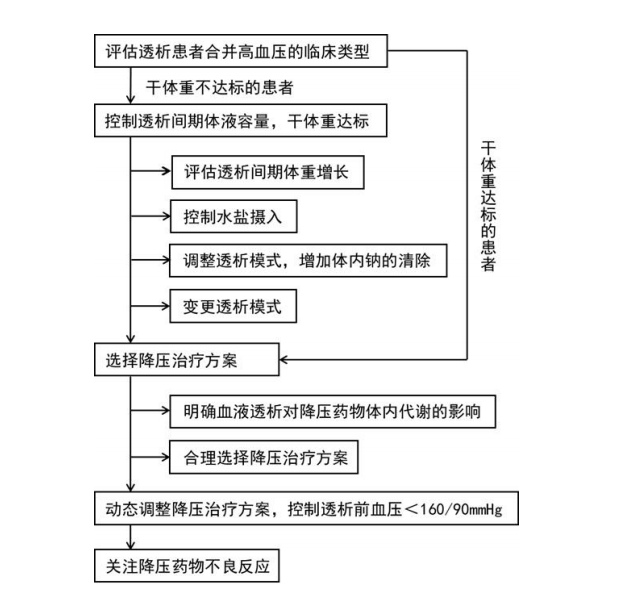
图2. 血液透析患者高血压控制的工作流程
具体而言,血液透析患者高血压的管理应注意以下方面:
1.选择合适降压药物
根据血液透析对降压药物的清除特征选择,影响药物透析性的因素包括蛋白质结合大小、分布容积、分子量、与透析膜/血滤膜的相互作用等。
此外,透析高血压合并心力衰竭的患者可考虑应用血管紧张素受体脑啡肽酶抑制剂(ARNI)。研究表明,ARNI可改善透析合并射血分数减低心力衰竭患者的左心室射血分数和心肌标志物水平[8-9],有效改善维持性血液透析合并CHF患者左室重构[10]。此外,低剂量盐皮质激素受体拮抗剂(MRA)可使心血管死亡率降低54%,且不会显著增加中重度高钾血症[11]。但非奈利酮控制血透患者的血压的循证依据尚缺乏。
2.根据不同临床类型选择透析高血压的治疗方案
容量负荷增多:控制干体重。
容量负荷增多+透析效率过高+心功能不全/交感神经反应不足:控制干体重,降低透析效率,首选透析可清除的ACEI类药物。
容量负荷增多+RAS/交感神经反应增强:控制干体重,首选不宜被透析清除的ACEI、ARB类或α、β受体拮抗剂。
RAS/交感神经反应增强:首选不宜被透析清除的ACEI、ARB类或α、β受体拮抗剂。
心功能不全+RAS/交感神经反应增强:改善心功能,首选不宜被透析清除的ACEI、ARB类。
3.其他治疗方式
低钠透析可改善血液透析后血压,降低发生透析高血压的几率,但需注意引起低血压和肌肉痉挛的风险[12-13]。夜间血液透析是指一周内3~7次于夜间睡眠时进行透析(每次6-10小时),患者无需使用降压药即可达到正常血压[14],但在我国尚未广泛开展。肾去神经术通过消融支配肾脏的交感神经来控制血压,对难治性高血压有一定效果[15]。
4.容量控制
容量控制是防治透析患者高血压的关键环节,所有合并高血压的血液透析患者干体重达标和减少盐摄入量是降压治疗的基础。
容量评估方法包括:体重、血压、颈静脉压、下肢水肿、脑钠肽(BNP)、超声测量下腔静脉直径、血细胞比容监测、组织钠磁共振成像(23Na-MRI)、生物电阻抗分析、肺超声等。其中生物电阻抗分析(BIA)是一种无创且可重复性高的检测技术,通过测量体液和细胞膜的电学特性来评估人体水分总量及其分布。肺部超声中出现的过多B线是长期透析患者细胞外液容量扩张的标志,可用于评估干体重[16];肺超声引导下的干体重下调可以长期有效、安全地降低动态血压水平[17]。
四、透析中低血压的管理
透析中低血压一般指透析中收缩压下降≥20 mmHg或平均动脉压下降10 mmHg以上,同时伴有低血压症状。透析中低血压的危险因素包括年龄较大、透析龄较长、糖尿病、透析前血压较低、白蛋白低、女性、BMI较高。若秀析患者出现困倦、嗜睡、叹息、烦躁、头痛、肌肉痉挛、呼吸困难及胸背疼痛、腹痛、恶心呕吐等[18],应警惕是否出现低血压。
透析低血压一旦发生,可导致组织器官缺血、血管通路闭塞、透析时间缩短及透析不充分等。因此,透析中应积极采取措施,预防其发生(图3)。透析期间进行有氧和无氧运动训练可有效改善身体健康状况、减少透析低血压的发生[19]。

图3. 透析低血压的预防方案
总结
慢性肾脏病患者的血压管理是一个复杂且关键的环节,需要根据患者的具体情况制定个体化的血压控制目标和治疗方案。同时,要重视透析患者的容量管理和低血压预防,以延缓疾病进展、减少并发症发生、提高患者生活质量和生存率。在临床实践中,还需密切关注患者的病情变化和治疗反应,及时调整治疗策略。
参考文献
1. Habas E Sr, Habas E, Khan FY, Rayani A, Habas A, Errayes M, Farfar KL, Elzouki AY. Blood Pressure and Chronic Kidney Disease Progression: An Updated Review. Cureus. 2022 Apr 18;14(4):e24244. doi: 10.7759/cureus.24244. PMID: 35602805; PMCID: PMC9116515.
2. 中华医学会肾脏病学分会专家组. 中国慢性肾脏病患者高血压管理指南(2023年版)[J]. 中华肾脏病杂志, 2023, 39(1): 48-80. DOI: 10.3760/cma.j.cn441217-20220630-00650.
3. SPRINT Research Group, Wright JT Jr, Williamson JD, et al. A Randomized Trial of Intensive versus Standard Blood-Pressure Control [published correction appears in N Engl J Med. 2017 Dec 21;377(25):2506.
4. Erviti J, Saiz LC, Leache L, Pijoan JI, Menéndez Orenga M, Salzwedel DM, Méndez-López I. Blood pressure targets for hypertension in people with chronic renal disease. Cochrane Database Syst Rev. 2024 Oct 15;10(10):CD008564. doi: 10.1002/14651858.CD008564.pub3. PMID: 39403990; PMCID: PMC11475354.
5. 慢性肾脏病高血压管理共识专家组. 非透析和透析慢性肾脏病患者高血压管理的中国专家共识[J]. 中华内科杂志, 2023
6. Bhandari S, Mehta S, Khwaja A, et al. Renin-Angiotensin System Inhibition in Advanced Chronic Kidney Disease. N Engl J Med. 2022;387(22):2021-2032.
7. 国家卫健委. 血液净化标准操作规程(2021版). https://www.nhc.gov.cn/wjw/c100175/202111/0f854f7e65cf49bebd930a0f95c8efad.shtml
8. Sha Fu, et al. Effects of sacubitril‑valsartan in heart failure with preserved ejection fraction in patients undergoing peritoneal dialysis[J]. Front Med (Lausanne),2021, 8: 657067
9. Lee S, Oh J, et al. Sacubitril/valsartan in patients with heart failure with reduced ejection fraction with end‑stage of renal disease[J]. ESC Heart Fail, 2020, 7(3):1125-1129
10. Yang Wen, et al. Effects and safety of Sacubitril/Valsartan (SV) on heart function and blood pressure in maintenance hemodialysis (MHD) patients.[J] .Am J Transl Res, 2022, 14: 3439-3447
11. Yifan Zhu, et al. The safety and efficacy of low-dose mineralocorticoid receptor antagonists in dialysis patients: A meta-analysis.[J] .Medicine (Baltimore), 2021, 100: e24882
12. Nair SV, et al. Effect of low dialysate sodium in the management of intradialytic hypertension in maintenance hemodialysis patients: a single-center Indian experience. Hemodial Int. 2021 Mar 18
13. Radhakrishnan RC, et al. Effects of individualized dialysate sodium prescription in hemodialysis: results from a prospective interventional trial. Indian J Nephrol. 2020 Jan–Feb
14. Roumeliotis, A., Roumeliotis, S., Chan, C., & Pierratos, A. (2021). Cardiovascular Benefits of Extended-Time Nocturnal Hemodialysis. Current vascular pharmacology, 19(1), 21–33
15. Scalise, F., et al. (2020) Renal denervation in patients with end-stage renal disease and resistant hypertension on long-term haemodialysis. Journal of hypertension, 38(5), 936–942
16. Charalampos Loutradis, et al. The effect of dry-weight reduction guided by lung ultrasound on ambulatory blood pressure in hemodialysis patients: a randomized controlled trial. Kidney Int. 2019 Jun;95(6):1505-1513.
17. Charalampos Loutradis, et al. Ambulatory blood pressure changes with lung ultrasound-guided dry-weight reduction in hypertensive hemodialysis patients: 12-month results of a randomized controlled trial.
J Hypertens, 2021, 39: 1444-1452.
18. 中国医药教育协会肾病与血液净化专业委员会血液透析低血压防治专家组. 血液透析中低血压防治专家共识(2022)[J]. 中华内科杂志,2022,61(3):269-281. DOI:10.3760/cma.j.cn112138-20210601-00384.
19. Rhee SY, Song JK, Hong SC, et al. Intradialytic exercise improves physical function and reduces intradialytic hypotension and depression in hemodialysis patients. Korean J Intern Med. 2019 May;34(3):588-598.
- 推荐文章
