- 首页 > 正文
泰它西普治疗IgA肾病的临床探索:疗效、个体化应用与联合策略新证据
发表时间:2026-03-14 08:58:13
编者按
随着对IgA肾病发病机制的深入研究,针对B细胞活化因子(BLyS)和增殖诱导配体(APRIL)的双重抑制治疗,已成为极具前景的治疗新方向。泰它西普(Telitacicept)作为全球首个同类靶向生物制剂,通过同时阻断BLyS和APRIL,旨在从源头减少致病性Gd-IgA1的产生。在第23届亚太肾脏病学大会(APCN 2025)上,多项临床研究壁报展示了泰它西普在IgA肾病治疗中的真实世界应用数据与创新联合方案,为该病的个体化精准治疗提供了新的重要证据。本文旨在综合其中三项关键研究(摘要号C0468、C0480、C0499),对其临床疗效、安全性及治疗策略进行梳理与解析。
一、泰它西普单药治疗的初步疗效与安全性评估
来自中国哈尔滨医科大学附属第二医院的研究(摘要C0468)[1]报告了一项小型真实世界研究,初步评估了泰它西普在14例蛋白尿>2 g/d的活检证实IgA肾病患者中的疗效与安全性。
所有患者接受泰它西普160 mg/周皮下注射,同时接受优化的支持治疗(ACEI/ARB),为期至少6个月。未同时使用激素或其他免疫抑制剂。
研究结果:
蛋白尿显著降低:泰它西普治疗4周时,患者24小时尿蛋白定量平均值即从基线时的4.27±2.63 g/d显著下降至2.61±1.92 g/d;治疗24周时进一步降至1.28±0.75 g/d,降幅显著(P=0.002)。
血尿改善:尿红细胞计数从基线时的(57.11±101.18)/HPF,降至4周时的(20.74±31.83)/HPF(P=0.01),治疗24周时降至(5.53±7.33)/HPF(P=0.002)。
血清白蛋白升高:治疗4周时,平均血清白蛋白水平从基线时的38.92±5.03 g/L升至43.25±4.40 g/L(P=0.01),治疗24周时,升至47.29±8.17 g/L(P=0.002)。
肾功能稳定:治疗期间,患者平均血肌酐和估算肾小球滤过率(eGFR)保持稳定,无显著波动。
安全性良好:所有14例患者在24周随访期间,均未报告感染、注射部位过敏反应等不良反应,亦无疾病复发。所有IgA患者在泰它西普治疗期间均未使用皮质类固醇或免疫抑制剂。
结论
该研究表明,对于IgA肾病患者,在不联合激素或传统免疫抑制剂的情况下,泰它西普治疗能有效降低尿蛋白和血尿,提升血清白蛋白水平,且具有较高的安全性,为IgA肾病患者提供了一种新的治疗选择。
二、泰它西普为合并糖尿病的IgA肾病患者提供“无激素”治疗新选择
对于IgA肾病患者,传统治疗方案(无论是否联合免疫抑制剂)均会增加感染、骨质疏松及糖代谢紊乱的风险。来自中南大学湘雅医院的一例病例报告(摘要C0480)[2]则关注了IgA肾病治疗中的特殊困境——合并糖尿病患者因激素治疗可能导致的血糖控制恶化。该报告展示了一例49岁、糖尿病史超过10年且合并并发症(糖尿病视网膜病变和周围神经病变)的男性患者。
病例特点与挑战:患者表现为大量蛋白尿,24小时尿蛋白排泄量(24h UPE)达9 g。初始临床诊断为糖尿病肾病。采用足量肾素-血管紧张素系统(RAS)抑制剂、钠-葡萄糖协同转运蛋白2(SGLT2)抑制剂和非甾体MRA进行初始治疗,未能降低蛋白尿(24h UPE增至29 g)。肾活检确诊为IgA肾病(Lee分级:Ⅲ级,牛津分型:M1E1S1T0C1)。为避免糖皮质激素诱导的高血糖,治疗团队选择了泰它西普单药治疗。
治疗方案与结果:
治疗:起始予泰它西普240 mg/周皮下注射,后逐渐减量至160 mg/周维持。每月监测蛋白尿、血清白蛋白及安全性标志物。
疗效:经过9个月治疗,患者24h UPE从29 g大幅降至0.75 g,血清白蛋白从24.1 g/L恢复正常,升至42.4 g/L。
安全性:治疗期间IgG水平保持正常,未发生感染、血细胞减少或血糖恶化。
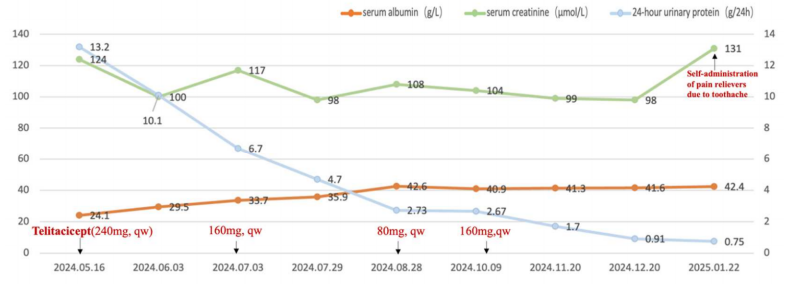
图1. 治疗期间血清白蛋白、肌酐和24小时尿蛋白的变化
启示
该病例表明,对于合并糖尿病、不适合或不愿接受糖皮质激素治疗的IgA肾病患者,泰它西普治疗具有双重优势:能显著降低蛋白尿水平,同时损害血糖控制或增加感染风险,体现了其作为“激素节省”策略的潜力,为这类高风险人群提供了重要的治疗新路径。未来,有必要进一步开展随机试验以验证其作为激素替代药物在这一高风险人群中的作用。
三、泰它西普联合靶向回肠布地奈德治疗晚期难治性IgA肾病取得突破
来自南方医科大学珠江医院的一例创新性联合治疗报告(摘要C0499)[3]尤其引人注目。该病例探索了针对IgA肾病发病中“肠道黏膜免疫源”和“全身B细胞活化”双重机制的联合阻断策略。
病例背景:患者为60岁男性,活检证实为IgA肾病(牛津分型:M1E0S1T1C0,LeeⅣ级),已进展至慢性肾脏病(CKD)4期。基线(2023年8月)血清肌酐为278 μmol/L,24小时尿蛋白4742 mg。
曲折的治疗历程与联合方案的提出:
初始(羟氯喹+沙库巴曲缬沙坦)治疗(2023年8月)及后续的加强治疗(加用泰它西普160 mg/周+达格列净)和挽救治疗(非奈利酮)(2024年2月)均未能有效控制疾病进展。
鉴于患者病情顽固,治疗团队创新性地采用了“泰它西普(80 mg/周)+靶向回肠布地奈德(Nefecon,16 mg/d)”的双靶点联合方案(2024年10月)(图2)。
卓越的联合治疗效果:联合治疗9个月后(至2025年6月):
蛋白尿近乎完全缓解:24小时尿蛋白下降93.8%,从4742 mg/d降至294 mg/d。
肾功能显著逆转:血肌酐下降20.3%(从300 μmol/L降至239 μmol/L),eGFR提升超过30%。
安全性良好:未出现感染、高钾血症或肝毒性等不良反应。
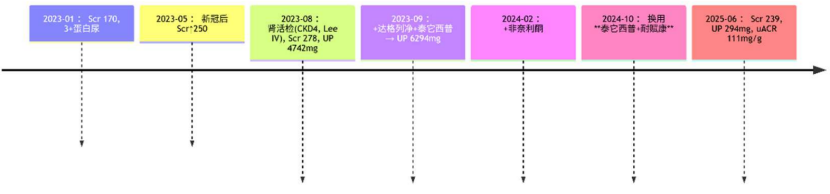
图2. 治疗历程
结论与展望
该病例首次证实,针对晚期、难治性IgA肾病,联合靶向肠道黏膜免疫(耐赋康)和全身B细胞活化(泰它西普)的双重机制治疗,能实现近乎完全的蛋白尿缓解和显著的肾功能改善。这一成功案例为高危、进展性IgA肾病的治疗提供了全新的、强有力的联合策略思路,亟待前瞻性研究的进一步验证。
总结
APCN 2025上披露的这三项关于泰它西普的研究,从不同维度丰富了我们对这一新型生物制剂在IgA肾病治疗中应用的认识:摘要C0468初步验证了其单药治疗的有效性与安全性;摘要C0480凸显了其在特殊人群(如合并糖尿病)中作为激素替代方案的独特价值;而摘要C0499则开创性地展示了基于疾病机制的多靶点联合治疗的巨大潜力,为攻克晚期难治性IgA肾病带来了曙光。随着更多临床数据的积累和治疗方案的优化,泰它西普有望在IgA肾病的个体化、精准化治疗格局中扮演越来越重要的角色。
参考文献
[1] weishiyao, et al. Real-world Study: Efficacy and Safety of Telitacicept in IgA Nephropathy without Hormones or immunosuppressants. Poster No.:C0468. 23rd Asian Pacific Congress of Nephrology. Dec 5-7, 2025.
[2]Qiongjing Yuan, et al. Clinical Efficacy of Telitacicept in the Treatment of IgA Nephropathy complicated by Diabetes Mellitus: A Case Report. Poster No.:C0480. 23rd Asian Pacific Congress of Nephrology. Dec 5-7, 2025.
[3]Tingting Guo, et al. Rapid Renal Recovery with Telitacicept and Nefecon Combination in Advanced IgA Nephropathy: A Case Report. Poster No.:C0499. 23rd Asian Pacific Congress of Nephrology. Dec 5-7, 2025.
随着对IgA肾病发病机制的深入研究,针对B细胞活化因子(BLyS)和增殖诱导配体(APRIL)的双重抑制治疗,已成为极具前景的治疗新方向。泰它西普(Telitacicept)作为全球首个同类靶向生物制剂,通过同时阻断BLyS和APRIL,旨在从源头减少致病性Gd-IgA1的产生。在第23届亚太肾脏病学大会(APCN 2025)上,多项临床研究壁报展示了泰它西普在IgA肾病治疗中的真实世界应用数据与创新联合方案,为该病的个体化精准治疗提供了新的重要证据。本文旨在综合其中三项关键研究(摘要号C0468、C0480、C0499),对其临床疗效、安全性及治疗策略进行梳理与解析。
一、泰它西普单药治疗的初步疗效与安全性评估
来自中国哈尔滨医科大学附属第二医院的研究(摘要C0468)[1]报告了一项小型真实世界研究,初步评估了泰它西普在14例蛋白尿>2 g/d的活检证实IgA肾病患者中的疗效与安全性。
所有患者接受泰它西普160 mg/周皮下注射,同时接受优化的支持治疗(ACEI/ARB),为期至少6个月。未同时使用激素或其他免疫抑制剂。
研究结果:
蛋白尿显著降低:泰它西普治疗4周时,患者24小时尿蛋白定量平均值即从基线时的4.27±2.63 g/d显著下降至2.61±1.92 g/d;治疗24周时进一步降至1.28±0.75 g/d,降幅显著(P=0.002)。
血尿改善:尿红细胞计数从基线时的(57.11±101.18)/HPF,降至4周时的(20.74±31.83)/HPF(P=0.01),治疗24周时降至(5.53±7.33)/HPF(P=0.002)。
血清白蛋白升高:治疗4周时,平均血清白蛋白水平从基线时的38.92±5.03 g/L升至43.25±4.40 g/L(P=0.01),治疗24周时,升至47.29±8.17 g/L(P=0.002)。
肾功能稳定:治疗期间,患者平均血肌酐和估算肾小球滤过率(eGFR)保持稳定,无显著波动。
安全性良好:所有14例患者在24周随访期间,均未报告感染、注射部位过敏反应等不良反应,亦无疾病复发。所有IgA患者在泰它西普治疗期间均未使用皮质类固醇或免疫抑制剂。
结论
该研究表明,对于IgA肾病患者,在不联合激素或传统免疫抑制剂的情况下,泰它西普治疗能有效降低尿蛋白和血尿,提升血清白蛋白水平,且具有较高的安全性,为IgA肾病患者提供了一种新的治疗选择。
二、泰它西普为合并糖尿病的IgA肾病患者提供“无激素”治疗新选择
对于IgA肾病患者,传统治疗方案(无论是否联合免疫抑制剂)均会增加感染、骨质疏松及糖代谢紊乱的风险。来自中南大学湘雅医院的一例病例报告(摘要C0480)[2]则关注了IgA肾病治疗中的特殊困境——合并糖尿病患者因激素治疗可能导致的血糖控制恶化。该报告展示了一例49岁、糖尿病史超过10年且合并并发症(糖尿病视网膜病变和周围神经病变)的男性患者。
病例特点与挑战:患者表现为大量蛋白尿,24小时尿蛋白排泄量(24h UPE)达9 g。初始临床诊断为糖尿病肾病。采用足量肾素-血管紧张素系统(RAS)抑制剂、钠-葡萄糖协同转运蛋白2(SGLT2)抑制剂和非甾体MRA进行初始治疗,未能降低蛋白尿(24h UPE增至29 g)。肾活检确诊为IgA肾病(Lee分级:Ⅲ级,牛津分型:M1E1S1T0C1)。为避免糖皮质激素诱导的高血糖,治疗团队选择了泰它西普单药治疗。
治疗方案与结果:
治疗:起始予泰它西普240 mg/周皮下注射,后逐渐减量至160 mg/周维持。每月监测蛋白尿、血清白蛋白及安全性标志物。
疗效:经过9个月治疗,患者24h UPE从29 g大幅降至0.75 g,血清白蛋白从24.1 g/L恢复正常,升至42.4 g/L。
安全性:治疗期间IgG水平保持正常,未发生感染、血细胞减少或血糖恶化。

图1. 治疗期间血清白蛋白、肌酐和24小时尿蛋白的变化
启示
该病例表明,对于合并糖尿病、不适合或不愿接受糖皮质激素治疗的IgA肾病患者,泰它西普治疗具有双重优势:能显著降低蛋白尿水平,同时损害血糖控制或增加感染风险,体现了其作为“激素节省”策略的潜力,为这类高风险人群提供了重要的治疗新路径。未来,有必要进一步开展随机试验以验证其作为激素替代药物在这一高风险人群中的作用。
三、泰它西普联合靶向回肠布地奈德治疗晚期难治性IgA肾病取得突破
来自南方医科大学珠江医院的一例创新性联合治疗报告(摘要C0499)[3]尤其引人注目。该病例探索了针对IgA肾病发病中“肠道黏膜免疫源”和“全身B细胞活化”双重机制的联合阻断策略。
病例背景:患者为60岁男性,活检证实为IgA肾病(牛津分型:M1E0S1T1C0,LeeⅣ级),已进展至慢性肾脏病(CKD)4期。基线(2023年8月)血清肌酐为278 μmol/L,24小时尿蛋白4742 mg。
曲折的治疗历程与联合方案的提出:
初始(羟氯喹+沙库巴曲缬沙坦)治疗(2023年8月)及后续的加强治疗(加用泰它西普160 mg/周+达格列净)和挽救治疗(非奈利酮)(2024年2月)均未能有效控制疾病进展。
鉴于患者病情顽固,治疗团队创新性地采用了“泰它西普(80 mg/周)+靶向回肠布地奈德(Nefecon,16 mg/d)”的双靶点联合方案(2024年10月)(图2)。
卓越的联合治疗效果:联合治疗9个月后(至2025年6月):
蛋白尿近乎完全缓解:24小时尿蛋白下降93.8%,从4742 mg/d降至294 mg/d。
肾功能显著逆转:血肌酐下降20.3%(从300 μmol/L降至239 μmol/L),eGFR提升超过30%。
安全性良好:未出现感染、高钾血症或肝毒性等不良反应。

图2. 治疗历程
结论与展望
该病例首次证实,针对晚期、难治性IgA肾病,联合靶向肠道黏膜免疫(耐赋康)和全身B细胞活化(泰它西普)的双重机制治疗,能实现近乎完全的蛋白尿缓解和显著的肾功能改善。这一成功案例为高危、进展性IgA肾病的治疗提供了全新的、强有力的联合策略思路,亟待前瞻性研究的进一步验证。
总结
APCN 2025上披露的这三项关于泰它西普的研究,从不同维度丰富了我们对这一新型生物制剂在IgA肾病治疗中应用的认识:摘要C0468初步验证了其单药治疗的有效性与安全性;摘要C0480凸显了其在特殊人群(如合并糖尿病)中作为激素替代方案的独特价值;而摘要C0499则开创性地展示了基于疾病机制的多靶点联合治疗的巨大潜力,为攻克晚期难治性IgA肾病带来了曙光。随着更多临床数据的积累和治疗方案的优化,泰它西普有望在IgA肾病的个体化、精准化治疗格局中扮演越来越重要的角色。
参考文献
[1] weishiyao, et al. Real-world Study: Efficacy and Safety of Telitacicept in IgA Nephropathy without Hormones or immunosuppressants. Poster No.:C0468. 23rd Asian Pacific Congress of Nephrology. Dec 5-7, 2025.
[2]Qiongjing Yuan, et al. Clinical Efficacy of Telitacicept in the Treatment of IgA Nephropathy complicated by Diabetes Mellitus: A Case Report. Poster No.:C0480. 23rd Asian Pacific Congress of Nephrology. Dec 5-7, 2025.
[3]Tingting Guo, et al. Rapid Renal Recovery with Telitacicept and Nefecon Combination in Advanced IgA Nephropathy: A Case Report. Poster No.:C0499. 23rd Asian Pacific Congress of Nephrology. Dec 5-7, 2025.
- 推荐文章
超越KDIGO指南,JAMA重磅综述3组数据+1张表格+3张图吃透IgA肾病临床核心要点与前沿治疗
突破认知!肠道微生物或从根本上改变狼疮肾病的诊断与治疗格局
开幕倒计时7天 | 中华医学会肾脏病学分会第二十届重症肾脏病与血液净化大会
学术纵横|2026年膜性肾病研究前沿:中国学者多项关键研究,涵盖疾病解析、疗效预测与治疗优化
年龄绝非只是数字:CureGN队列揭示肾小球疾病全年龄段的临床轨迹
ESC-HFA 2026重磅速递:CKM领域前沿进展抢先看
学术纵横|尿sCD163预测IgA肾病免疫治疗反应,再次升高较蛋白尿提前2.8个月预警复发;肾单位减少、镜下血尿提示疾病进展
专家共识|2026版儿童连续性肾替代治疗期间抗菌药物治疗方案调整要点一览
CKD患者再入院与死亡风险随eGFR下降呈剂量依赖性升高——基于125万人的大型研究
毛慧娟教授:2024~2026 AKI-CRRT临床研究进展
螺内酯与RAAS抑制剂在终末期肾病患者中的高钾血症风险及临床管理 | NKF SCM 2026
从心肾代谢综合征(CKM)看高血压与心肌重构的综合管理
肾例明鉴 | 蛋白尿飙升至7g/24h!38岁男子肾病综合征,利妥昔单抗如何实现膜性肾病从恶化到完全缓解的惊险逆转
一例18岁PLA2R阳性膜性肾病合并肾静脉血栓患者的诊疗挑战丨NKF SCM 2026
CONFIDENCE含金量还在上升!非奈利酮与SGLT2i同步起始治疗缘何更佳?
涂晓文教授:中晚期糖尿病肾脏疾病临床关注问题
Sparsentan在FSGS患者中的蛋白尿管理新证据——基于DUPLEX研究2项分析的解读 | NKF SCM 2026
轻松应对,安全无虞!非奈利酮与SGLT2i同步起始,如何化解临床顾虑?
罗洋教授:慢性肾脏病铁代谢紊乱的诊疗进展
伊普可泮治疗IgA肾病:APPLAUSE-IgAN 24个月最终结果与美国真实世界应用现状丨NKF SCM 2026
牛津团队领衔,中国医学科学院阜外医院参与!《柳叶刀》发表最新研究:慢性肾脏病患者全程降压,心血管获益同样显著
北大陈旻教授:补体系统失调在DKD发病机制的全新认知与潜在治疗靶点|WCN中国之声
梅奥诊所Farabursen临床研究:可增加尿多囊蛋白水平并减缓ADPKD患者肾脏体积增长,具有全球首创疾病修饰治疗的潜力丨WCN 2026
【会议预热】“和Fogo一起CPC”第三期:一场跨越中美、连接全球肾脏病理顶尖力量的学术对话即将开启!
全球顶尖肾病临床研究团队——Emerald Clinical(原乔治临床)权威专家阵容
热点辩论:异种器官移植与干细胞疗法能否替代人体器官捐献?|WCN 2026
达格列净进军ADPKD领域:1年临床研究证实显著延缓肾囊肿进展、保护肾功能丨WCN 2026
KI Report首次证实:早期B细胞亚群可预测膜性肾病患者利妥昔单抗治疗后的复发风险
常染色体显性多囊肾病精准治疗与研究范式正在革新中|WCN 2026
学术纵横|11项高质量研究展示2026年初狼疮肾炎领域最新进展
最新研究:UACR在预测儿童肾脏病进展方面优于UPCR
致敬传奇!原研司美格鲁肽登陆中国5周年,持续领跑,不断突破!
Jonathan Barratt教授专访:B细胞疗法兴起,生物标志物赋能肾小球疾病精准诊疗
2025版ISN全球肾脏健康地图(ISN-GKHA)重磅更新:从数据追踪到公平诊疗的行动之路|WCN 2026
阿塞西普每周一次皮下注射治疗IgAN疗效显著,PIONEER研究则进一步探索其在自身免疫性肾小球疾病中的价值|WCN 2026
肾例明鉴 | 一场普通感冒后,她的肌酐飙升至583μmol/L!医生:警惕药物埋下的肾损伤陷阱
新月体性IgA肾病合并无肾小球基底膜线性免疫荧光的抗GBM肾炎:首例病例报道
当狼疮“突袭”肾与脑:多学科协作成功救治一例重症系统性红斑狼疮活动发作
肾域华章 | 真实世界研究REVEAL重磅发布:司维拉姆显著降低ND-CKD患者透析与心血管事件风险
2026 AACE年会公布重要研究:恩格列净相较于达格列净,可降低2型糖尿病患者心肾事件风险
FDA受理奥妥珠单抗治疗系统性红斑狼疮的补充生物制剂许可申请
重磅!瑞利珠单抗两月一针,治疗IgA肾病Ⅲ期I CAN研究中期分析圆满达标
一“比”了然:高血清IgA/C3比值意味着更差的蛋白尿控制
议通知 | 4月24—26日:2026年第二十五届北京肾脏病学术会议
联合用药亦稳定:非奈利酮持续降低2型糖尿病合并CKD患者尿白蛋白——FIVE‑STAR试验二次分析
狼疮肾炎临床缓解期无症状血清学复阳:预防性强化免疫抑制治疗还是观察等待?
限盐也能预防心衰?证据来了!
外周血与肾间质T细胞谱:狼疮肾炎治疗反应的关键预测指标
运动使死亡风险降低46%!82项RCT的荟萃分析证实体育锻炼对CKD的7大获益
初夏相约,共赴京华——北大医院肾脏病精准医学学术会议第一轮通知
超1.5亿人受累!中国30年慢性肾脏病负担特征与变迁给未来防控带来哪些启示
中国台湾IgA肾病患者经扁桃体切除联合激素冲击治疗实现尿学缓解一例
指南共识丨ERA提出急性肾损伤患者出院后管理的十大核心建议
意外发现:常见心脏标志物BNP,竟是糖尿病患者肾脏功能下降的“预警信号”
秉持以心肾结局为中心的治疗策略:一例蛋白尿明显好转但肾功能持续下降DKD患者的诊疗启示
