- 首页 > 正文
"磷"危时刻——李贵森教授带你了解透析患者高磷血症管理策略与临床新进展
发表时间:2026-02-04 13:44:54

高磷血症作为透析患者最常见的CKD-矿物质骨代谢紊乱(CKD-MBD)表现之一,其危害性不容忽视。我国透析患者的血磷控制现状令人忧心——根据DOPPS研究数据,我国透析患者中血清磷在5.6~7.0 mg/dl的患者占28.3%,血清磷>7.0 mg/dl的患者比例高达23.1%[1]。更值得关注的是,年轻患者的血磷控制情况更差,<45岁患者中35.2%血清磷>7.0 mg/dl[1]。血清钙、磷及甲状旁腺激素三项指标的综合达标率甚至<10%[2]。
长期高磷血症可带来严重危害:①加速CKD进展,形成恶性循环;②高磷血症是血管钙化的重要促进因素;③显著增加心肌梗死、心力衰竭、脑卒中等严重心血管事件的风险,导致全因死亡率和心血管死亡率显著升高。一项纳入22 937例新入血液透析患者的队列研究显示,磷、钙、PTH达标项越少,患者的死亡风险越高[3],而综合达标减轻透析患者CAC进展风险[4],这充分说明了综合管理CKD-MBD指标的重要性。
二、高磷血症管理的"4D"原则与现状
长期以来,临床强调CKD-MBD管理需遵循"4D"综合干预原则:
低磷饮食(Diet):通过限制磷摄入控制血磷水平。研究显示,焯水并去掉汤汁可有效减少食物中的磷含量。然而,过度限制磷摄入可能导致营养不良,反而增加死亡风险。
充分透析(Dialysis):增加透析剂量可提高磷清除,但会带来更沉重的经济负担,且必须考虑PTH对骨骼的影响。
合理使用降磷药物(Drugs):这是临床管理的关键手段。2022年数据显示,美国Medicare Part D系统为降磷药花费巨大,磷结合剂在血液透析患者中的使用率位列第一(63.3%)且花费最高,其中碳酸司维拉姆使用占比最高(39.3%),其次是醋酸钙(20.3%)[5]。然而,我国磷结合剂使用情况调查结果显示,超过一半的透析中心非钙磷结合剂使用率低于30%[6]。
控制继发性甲状旁腺功能亢进(Decrease PTH):SHPT的控制对整体骨矿物质代谢平衡至关重要。
尽管"4D"原则明确,但在临床实践中仍面临诸多挑战。一项纳入77项研究、12 562例CKD患者的Meta分析显示,与含钙磷结合剂相比,司维拉姆可降低CKD患者全因死亡率,但与安慰剂相比,所有的磷结合剂均不能显著改善患者的死亡和心血管不良事件预后[7]。另有研究表明,非钙降磷治疗可减少非透析成人CKD患者血清磷酸盐和尿磷酸盐排泄,但对临床结局和中间心血管终点的影响尚不清楚。这提示我们需要重新审视当前的高磷血症管理策略[8]。
三、降磷药物的迭代与新型药物进展
降磷药物经历了多次迭代更新。早期含铝磷结合剂因铝蓄积中毒风险已基本退出临床。目前常用药物包括含钙磷结合剂(如碳酸钙、醋酸钙)和非钙非金属磷结合剂(如司维拉姆、碳酸镧)。近年来,多种作用机制迥异的新型降磷药物不断涌现。
含铁磷结合剂:如枸橼酸铁、蔗糖羟基氧化铁、己二酸三氧化二铁。中国Ⅲ期开放标签活性药物对照研究显示,枸橼酸铁在降磷效果上与司维拉姆相当[9]。另一项纳入286例中国透析高磷血症患者的Ⅲ期研究证实了蔗糖羟基氧化铁不劣于司维拉姆的良好疗效[10]。蔗糖羟基氧化铁在真实世界的结果与Ⅲ期研究一致,且每日药物负担较低[11]。 VS-505是一种新型磷酸盐结合剂,耐受性良好,安全性可控,可有效且剂量依赖性地降低接受维持性血液透析(MHD)治疗的高磷血症CKD患者的血清磷[12]。
抑制肠道磷吸收剂:如烟酰胺,通过抑制肠道上皮细胞钠依赖性磷酸盐协同转运蛋白减少磷吸收。
肠道钠氢离子交换体3抑制剂:如替那帕诺(Tenapanor),通过抑制NHE3增加肠道钠离子浓度,进而减少磷吸收并增加粪便磷排泄。AMPLIFY研究显示,纳入236例已接受磷结合剂治疗的高磷血症的MHD患者,随机分配接受替那帕诺 30mg Bid治疗和安慰剂,为期4周,结果显示,替那帕诺和磷酸盐结合剂的双机制治疗可改善MHD患者对高磷血症的控制[13]。NORMALIZE研究也显示,替那帕诺改善MHD患者高磷血症的长期控制[14]。
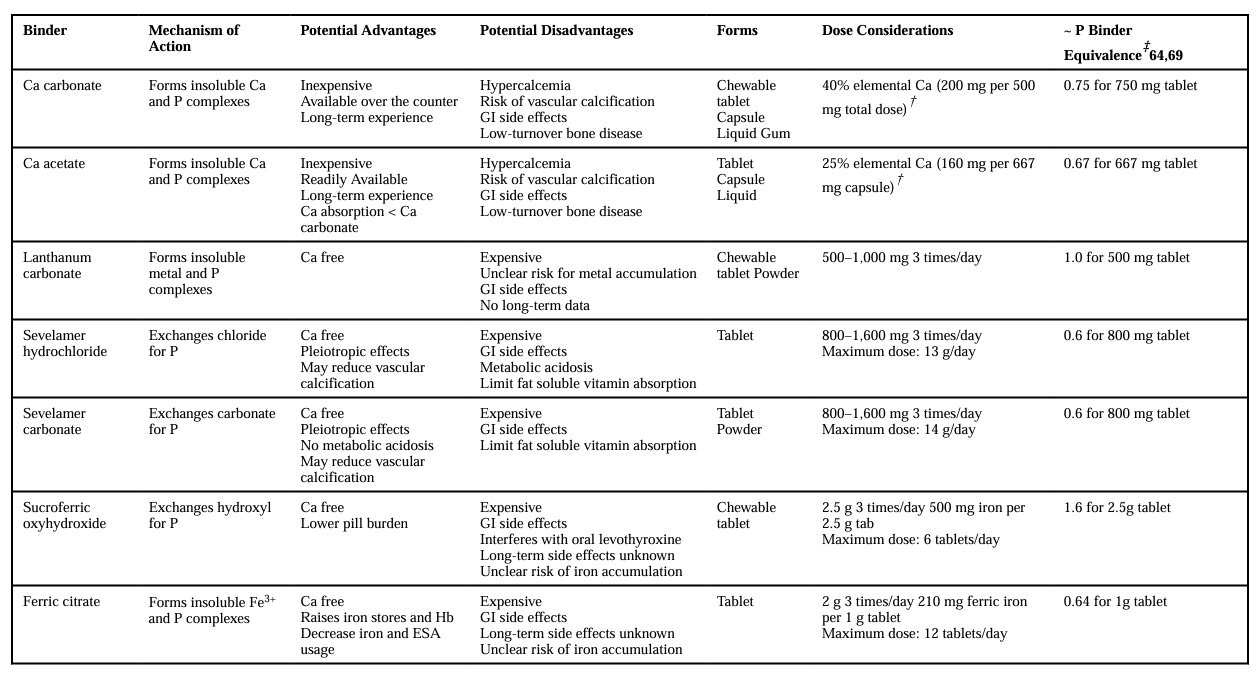
目前在美国长期使用的磷结合剂的临床特征比较见表1[15]。
表1. 美国长期使用的磷结合剂的临床特征比较
泛磷转运蛋白抑制剂:如AP306(EOS789),能同时抑制NaPi-IIb、PiT-1和PiT-2三种磷转运蛋白。Ⅱ期临床试验表明,AP306单药治疗显著降低血液透析高磷血症患者的血清磷酸盐水平,显著提高了血清磷酸盐控制率,且安全和耐受性良好[16]。
目前,枸橼酸铁、蔗糖羟基氧化铁、替那帕诺等已在中国完成临床试验并获批上市。这些新型药物为高磷血症管理提供了更多选择,但同时也带来了新的问题:如何更好地运用这些药物促使临床达标?目前国内对这些新药的临床应用经验普遍尚浅,其长期使用的安全性、耐受性及对骨代谢的长期影响,特别是对患者"硬终点"(即是否能显著降低全因死亡率、心血管死亡率和主要心血管事件发生率)的改善作用,尚缺乏循证证据。最新Cochrane系统评价纳入134项研究(涉及20 913例成人患者),与安慰剂/常规治疗相比,司维拉姆对全因死亡可能影响很小或没有影响;对高钙血症和恶心的影响不确定,但可能会增加CKD患者便秘的风险;降磷和CAC的影响可能很小或没有影响;对心血管死亡的影响无法估计[17]。因此,我们仍需深入探索。
四、争议与思考:血磷水平是否需要"正常化"?
当前关于高磷血症管理存在一个重要争议:是否需要将血磷水平"正常化"?现有证据显示,高磷血症和不良结局之间的关系主要是相关性而非因果性,没有RCT研究证明降低血磷能在临床相关终点带来任何益处。更值得关注的是,过度限制血磷的饮食可能导致营养不良和死亡率增加,而磷结合剂的使用也可能带来药物负担、不良反应、生活质量降低等问题,尤其是含钙磷结合剂还可能促进血管钙化。
日本学者Hamano和Fukagawa在Kidney International上发表的观点指出,我们可能需要重新思考当前严格降磷的策略。他们认为,对于不同风险分层的患者,可能需要个体化的血磷管理目标,而非一刀切地追求"正常化"[18]。
总结及未来展望
高磷血症作为透析患者常见且危害严重的并发症,其管理面临诸多挑战。虽然新型降磷药物不断涌现,但我们仍需清醒认识到,单纯依靠药物难以解决所有问题。未来需要在"4D"综合管理原则指导下,结合患者具体情况,制定个体化治疗方案。
未来,我们仍需在以下方面继续努力:①深入理解药物的作用机制、适用人群及潜在相互作用;②加强新型降磷药物长期疗效和安全性,特别是其对患者硬终点益处的循证证据积累;③期待更多中国透析人群的真实世界研究数据,提供本土化证据;④坚持“4D”原则基础上,探索新的药物组合和干预手段,同时重视患者教育。最终目标是显著提升透析患者血磷达标率及CKD-MBD整体管理水平,切实改善患者预后。
参考文献
1.赵新菊. DOPPS中国血磷控制现状(数据尚未发表).
2.Zhan Y, ……, Li G. Sci Rep. 2022; 12(1):16694
3.Danese MD, et al. Clin J Am Soc Nephrol, 2008,3(5):1423-1429.
4.Zhang H, Li G, …, Liu Z; CDCS Group. JAMA Netw Open. 2023; 6(5):e2310909
5.USRDS 2025. Prescription Drug Coverage in Patients with ESRD. https://usrds-adr.niddk.nih.gov/2023/end-stage-renal-disease/10-prescription-drug-coverage-in-patients-with-esrd?utm_source=chatgpt.com
6.Zhan Y, …, Li G. Sci Rep. 2022; 12(1):16694
7.Palmer SC, et al. Am J Kidney Dis, 2016, 68(5): 691-702.
8.Lioufas NM, et al. J Am Soc Nephrol. 2022; 33(1):59-76
9.Wang Y, et al. Am J Nephrol. 2023; 54(11-12):479-488
10.Liu J, et al. Nephron. 2024;148(1): 22-33
11.Vervloet MG, et al. Clin Kidney J. 2021;14(7):1770-79
12.Zhuang B, et al. Nephrol Dial Transplant. 2024 Sep 27;39(10): 1649-1661
13.Pergola PE, et al. J Am Soc Nephrol. 2021;32(6):1465-1473
14.Silva AL, et al. Kidney360. 2023; 4(11):1580-1589
15.Scialla JJ, et al. Am J Kidney Dis. 2021; 77(1): 132–141
16.Wang L, et al. Kidney Int Rep, 2025, 10(4): 1143-1151
17.Natale P, et al. Cochrane Database Syst Rev. 2025; 6(6):CD006023
18.Hamano T, Fukagawa M. Kidney Int. 2024; 106(2):191-195
- 推荐文章
