- 首页 > 正文
ASN壁报精选 | 研究者解读:混合效应回归模型揭示肾小球疾病eGFR下降规律
发表时间:2026-01-31 11:07:42
在2025年美国肾脏病学会年会(ASN 2025)上,美国西北大学范伯格医学院的Sriyans Gadde博士团队以壁报形式展示了一项题为“肾小球疾病中估算肾小球滤过率的混合效应回归模型”(FR-PO0862)的研究,深入探讨了非糖尿病肾小球疾病患者估算肾小球滤过率(eGFR)的下降模式及影响因素,为临床风险预测和疾病管理提供了新视角。肾医线邀请研究第一作者Sriyans Gadde博士对此研究进行了解读。

一、研究背景及方法
传统观点认为,非糖尿病肾小球疾病的病情进展以 eGFR 线性下降为特征,但临床中部分患者的 eGFR 下降存在非线性特征,这一现象尚未得到充分关注。基于此,研究团队旨在通过更精准的统计模型,揭示不同人群中 eGFR 的真实下降轨迹,为个体化诊疗提供依据。
Gadde博士介绍,研究纳入了来自“治愈肾小球疾病网络”(CureGN)的2790例参与者,涵盖微小病变肾病(MCD)、局灶节段性肾小球硬化(FSGS)、膜性肾病(MN)以及IgA肾病/血管炎(IgAN/V)四种肾小球疾病,所有参与者均至少有2次eGFR检测记录。
本研究有两个核心目标:
第一,按年龄、性别、APOL1风险等位基因状态、高血压状态和体重状态进行分层分析,对比不同临床和人口统计学亚组的估算肾小球滤过率(eGFR)下降速度;
第二,通过似然比检验评估加入二次项后模型拟合度的潜在改善情况,即是否比简单的线性模型更能精准拟合eGFR变化轨迹。为此,研究采用了同时具有随机截距和斜率的混合效应线性回归模型。
二、核心研究结果
2790例受试者中,34%为儿科,43%为女性,分别为27%和35%为超重和肥胖,44%为高血压。
1.整体下降趋势与疾病亚型差异
所有参与者的eGFR年平均下降率为-1.3 ml/(min·1.73m²),不同疾病亚型间差异显著:MCD患者下降最慢,年下降率仅为-0.2 ml/(min·1.73m²);FSGS患者下降最快,年下降率达-2.0 ml/(min·1.73m²)。
2.人口学与健康因素的影响
在第一个目标的分析中,观察到一些预期规律(图1),具体表现在:
男性和女性之间的eGFR下降速度没有显著差异。
体重状态方面,超重和肥胖参与者的eGFR下降速度显著快于正常体重者,年下降率分别为-1.6、-1.4和-0.8 ml/(min·1.73m²)(P=0.02)。
高血压状态方面,1期和2期高血压患者的eGFR年下降率分别为-1.5和-2.2 ml/(min·1.73m²),远高于血压正常者的-0.7 ml/(min·1.73m²)(P<0.001)。
年龄因素上,12岁以下入组患者的eGFR呈现特殊变化,部分IgAN/V患儿的eGFR甚至每年提升1.072 ml/(min·1.73m²),也就是说这个亚组的肾功能在初期似乎有所恢复。
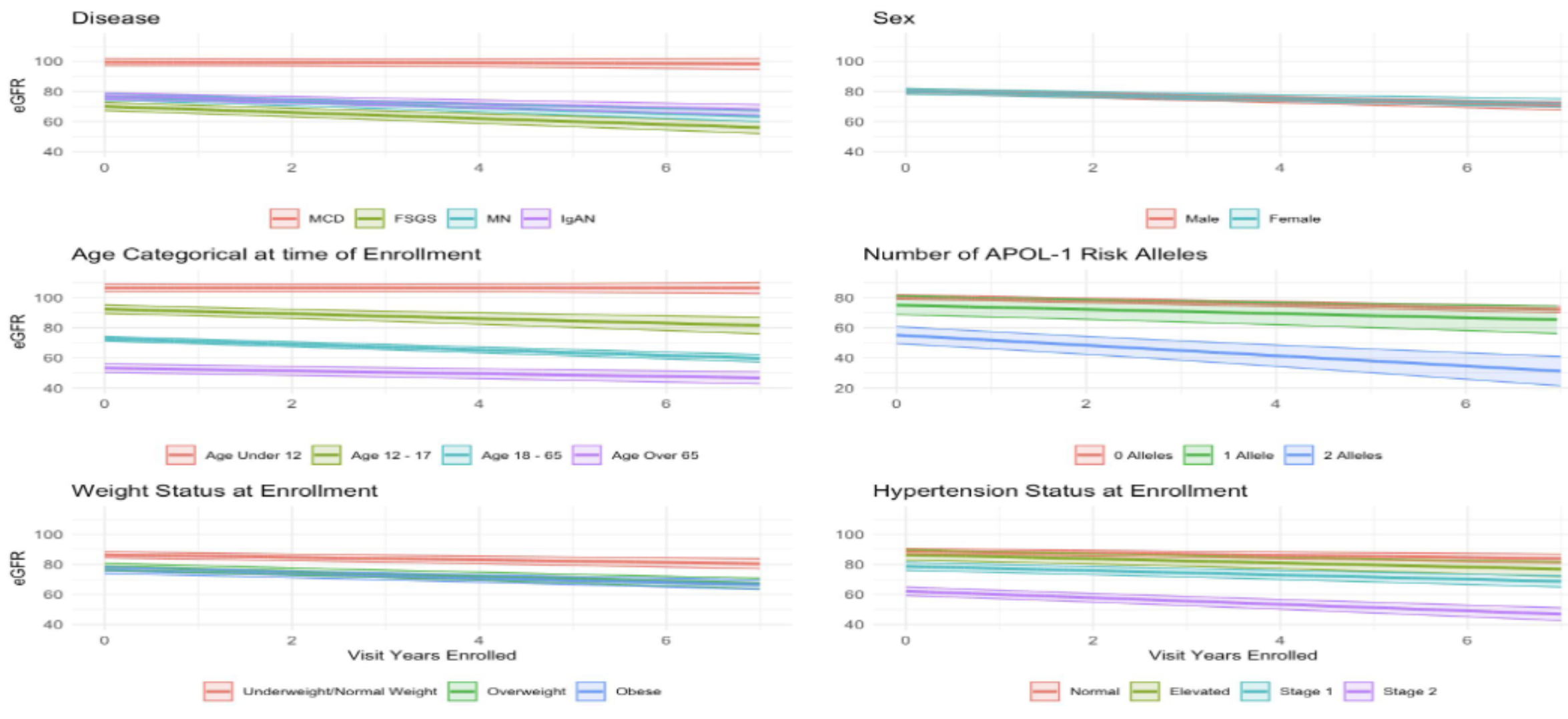
图1. 按人口统计学和临床因素比较eGFR下降情况线性混合效应模型比较显示,eGFR轨迹随时间变化,按疾病类型、年龄组、APOL1风险等位基因、体重状态和高血压状态分层。每个面板展示不同人口统计学和临床亚组的eGFR轨迹。阴影区域代表随访年数的95%置信区间。该分析旨在评估不同亚组间eGFR变化率的差异,通过线性回归模型的回归线和置信区间体现。图中展示了不同人口统计学和临床因素下eGFR下降率的差异
3.非线性下降模式的关键发现
第二个目标的分析中,研究发现仅有部分亚组采用二次项模型比线性模型的拟合度更优(图2),提示这些亚组的eGFR随时间呈非线性变化。
MCD患者、12岁以下儿童、正常体重者以及血压正常或升高人群中,时间二次项具有统计学意义(取值范围-0.5至-0.12),表明这些人群的eGFR整体呈现“初始稳定,随后下降”的非线性轨迹。
膜性肾病(MN)组,以及在接受基因检测的亚组中,携带2个APOL1风险等位基因的患者(121/1959),病情进展更快,年eGFR下降率达-3.2 ml/(min·1.73m²),且二次项系数为0.42,提示其eGFR呈现“早期快速下降,随后趋于稳定”的特征。
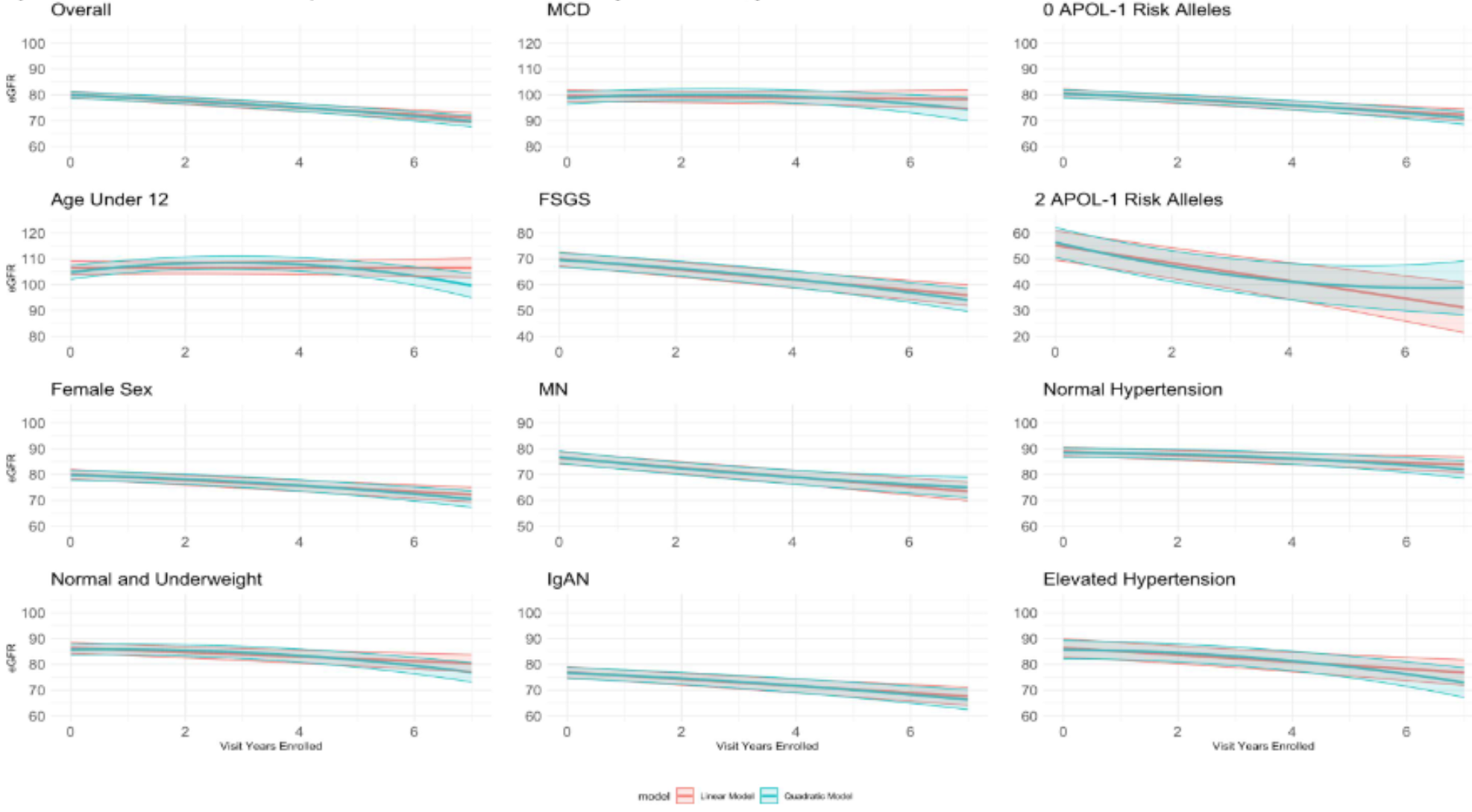
图2. 线性与二次模型比较比较线性和二次混合效应模型的eGFR轨迹,按人口统计学和临床亚组分层。亚组包括总体队列、罕见肾病(0或2个APOL1风险等位基因)、12岁以下患者、女性、正常体重和超重患者、高血压患者。每个面板展示这些亚组之一,eGFR随入组后年数的变化,分别采用线性(蓝色)和二次(红色)混合效应模型。阴影区域代表95%置信区间。
临床意义与研究结论
Gadde博士指出,传统上,eGFR下降一直采用线性模型进行预测,这意味着临床医生通常认为患者的肾功能每年会以相对恒定的速度下降。
然而,本研究证实,肾小球疾病患者的eGFR变化并非均一模式,而是受疾病亚型、年龄、体重、高血压状态及APOL1基因状态等多种因素调控。有些患者早期eGFR下降速度极快,而另一些患者则在疾病后期才出现肾功能快速恶化。传统线性模型难以准确捕捉部分人群的非线性下降特征,而针对性采用非线性模型可显著提升风险预测的准确性。
因此,“从患者确诊开始,我们就需要明确其eGFR是呈稳定变化,还是在特定节点出现加速下降或趋于稳定的情况。”Gadde博士强调。
总而言之,该研究对临床实践具有重要指导价值:临床医生需关注不同人群的eGFR变化规律,针对高风险阶段(如APOL1风险基因携带者的早期病程、高血压患者的全程)加强监测;同时,在制定治疗方案时,应综合考量患者的体重、血压、基因状态、年龄等个体特征,优化个体化患者管理方案,从而更有效地延缓肾功能恶化。
- 推荐文章
