- 首页 > 正文
J Hypertens发表中国团队研究:揭示非奈利酮心脏保护的分子机制!
发表时间:2026-01-31 13:59:39
编者按
非奈利酮作为一种新型非甾体类盐皮质激素受体拮抗剂(nsMRA),在心力衰竭、糖尿病肾病领域表现出显著的心血管和肾脏保护作用。有研究显示,非奈利酮可改善心脏结构与功能参数[1,2],但其在心室重构中的作用及机制尚不明确。近期,一项发表于Journal of Hypertension的中国团队研究对此进行了探索,并首次揭示非奈利酮心脏保护的全新分子机制:通过调控内质网(ER)应激关键通路——IRE1/XBP1与IRE1/TRAF2,从而改善心室重构与心功能[3]。本刊特邀研究通讯作者、天津市人民医院齐新教授进行点评。

基础研究新进展:非奈利酮改善心室重构与心功能的分子机制
研究方法
该研究采用经典的“两肾一夹”(2K1C)方法构建Sprague-Dawley大鼠高血压模型,将其随机分为假手术组、2K1C模型组和非奈利酮治疗组(2 mg/kg/d,经口灌胃,持续8周)。通过动态监测血压、超声心动图评估心功能,以及检测与心血管重构相关的生化指标和内质网应激标志物,以系统评价非奈利酮的心血管保护作用。同时,体外实验采用血管紧张素II(Ang-II)诱导H9C2心肌细胞损伤模型,进一步探索非奈利酮对心肌细胞凋亡及内质网应激反应的调控作用[3]。
主要结果
1)表型改善:非奈利酮显著改善血压与心功能指标
血压:模型组大鼠血压显著高于假手术组,且模型大鼠能够维持稳定的高血压状态。非奈利酮治疗8周后,治疗组大鼠的收缩压(SBP)和舒张压(DBP)水平均明显低于模型组(图1a)[3]。
心功能指标:超声心动图结果显示,与模型组相比,非奈利酮治疗组的左室射血分数(LVEF)、左室缩短分数(LVFS)及E/A比值显著升高,左室舒张末期内径(LVEDD)显著降低(图1b)。而且,非奈利酮还可改善心肌肥厚,表现为心脏重量和心脏质量指数均较模型组明显下降(图1c)[3]。
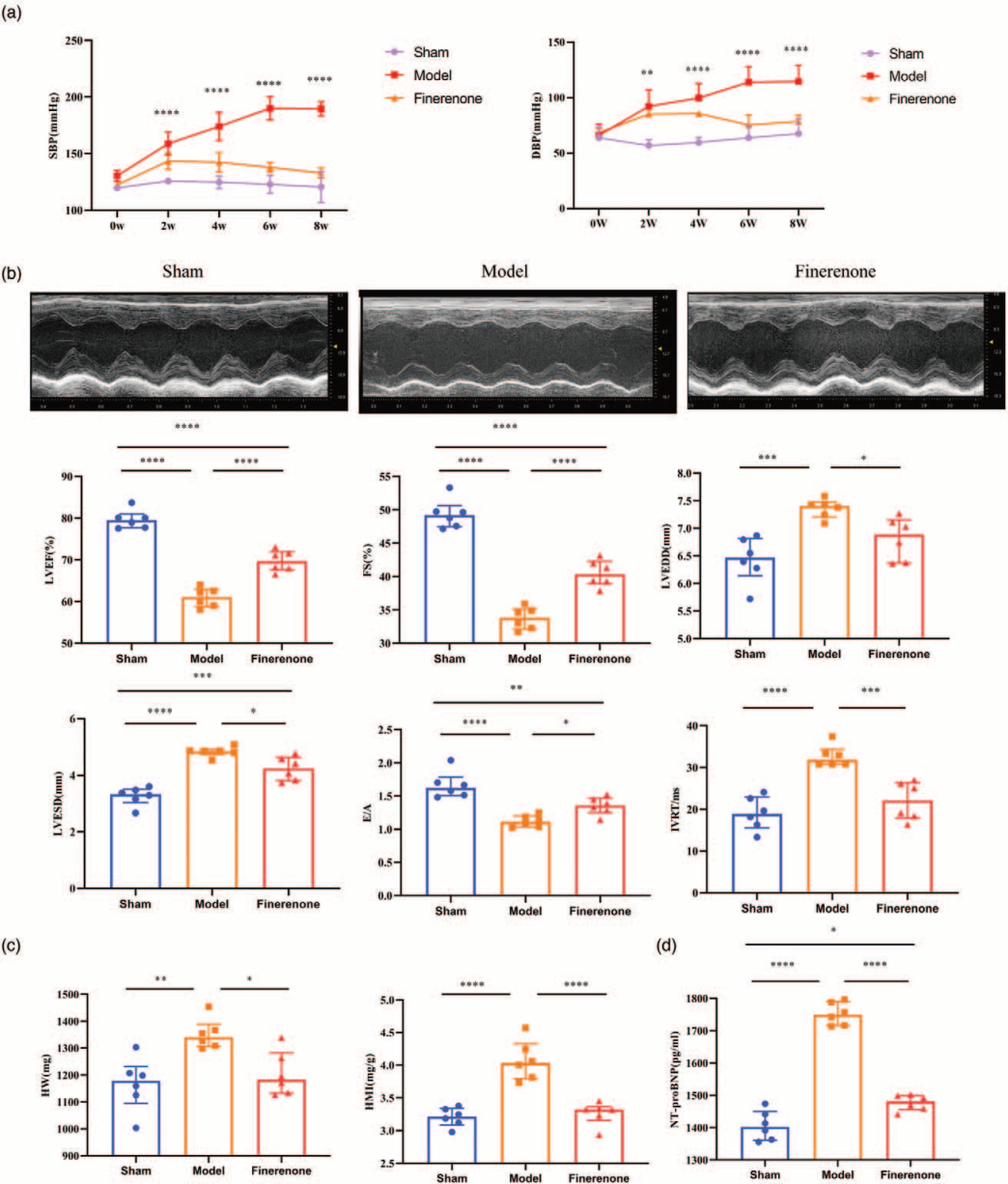
图1. 非奈利酮缓解高血压大鼠模型的血压升高和心功能损伤
2)病理生理:非奈利酮抑制心肌纤维化与炎症反应,改善心室重构
非奈利酮显著改善高血压大鼠模型的心室重构(图2)。组织病理学分析(HE、Masson及天狼星红染色)显示非奈利酮显著减轻心肌细胞排列紊乱、降低心肌细胞的横截面积及心肌组织胶原沉积(胶原容积分数[CVF]降低)。同时,非奈利酮组心肌组织中Ang-II、可溶性生长刺激表达基因2蛋白(sST2)、IL-6和TNF-α水平均显著下降,表明非奈利酮具有明确的抗纤维化/抗炎作用[3]。
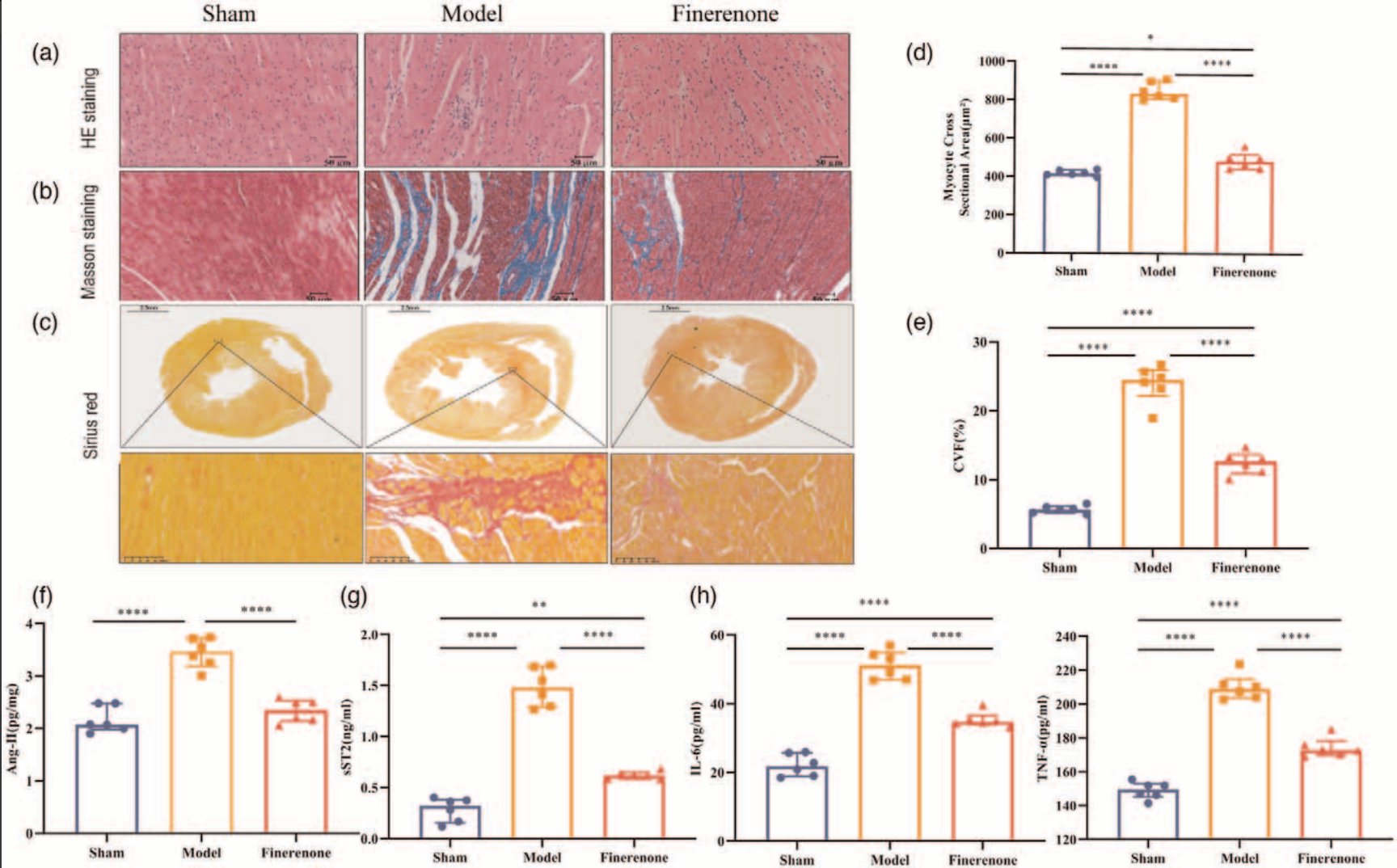
图2. 非奈利酮改善高血压大鼠模型的心室重构
3)分子机制:非奈利酮通过IRE1通路抑制内质网应激与心肌细胞凋亡
IRE1是一种存在于内质网膜上的跨膜蛋白,其介导的IRE1通路是调控内质网应激的重要凋亡通路之一。在应激状态下,IRE1自磷酸化后可分别激活XBP1(调控未折叠蛋白反应)和招募TRAF2(激活凋亡信号)。高血压大鼠心肌组织中内质网应激标志物GRP78表达显著升高,同时IRE1磷酸化(p-IRE1)、XBP1及TRAF2蛋白水平亦明显上调。非奈利酮治疗后,上述蛋白表达均显著下调,提示其有效缓解心肌内质网应激[3]。
在H9C2细胞实验中,Ang-II诱导的细胞凋亡率显著升高,Bax/Bcl-2比值及Caspase-12表达增加;而非奈利酮可显著逆转上述变化。Western blot进一步证实,非奈利酮可抑制GRP78、p-IRE1、XBP1、TRAF2及Caspase-12的表达,从而阻断IRE1/TRAF2/Caspase-12凋亡通路[3]。
本研究首次证实,非奈利酮通过调节IRE1/XBP1通路以及IRE1/TRAF2复合物的生成,来抑制内质网应激、并减少心肌细胞凋亡,从而改善心室重构、减轻心肌损伤。
专家点评
齐新教授天津市人民医院
非奈利酮心血管保护谱进一步拓宽,临床应用前景广阔
研究意义:首次揭示非奈利酮心脏保护的新分子机制
在糖尿病和慢性肾脏病模型中,非奈利酮可减轻心肌细胞凋亡和心室重构,改善心肌纤维化,改善心脏收缩和舒张功能[4-6]。大规模临床研究也证实其心脏保护作用,对于2型糖尿病相关慢性肾脏病患者,非奈利酮可显著降低心血管事件和心血管死亡风险[7]。
近期发表的一项德国小规模真实世界研究显示,糖尿病肾病患者应用非奈利酮治疗6个月,心脏结构和功能参数明显改善,左心房容积指数(LAVI)在治疗4周后即显著下降,其中对于合并射血分数保留或轻度降低的心力衰竭(HFpEF/HFmrEF)患者,除LVAI下降外,舒张功能指标E/e'也显著下降,提示非奈利酮有效降低了左心室充盈压[2]。这与本研究中非奈利酮改善心功能指标的结果相一致。
在心血管疾病发生发展中,高血压是一个关键风险因素,醛固酮水平升高被认为是介导高血压心肌损伤的重要因素。然而,非奈利酮对高血压心室重构的影响及其潜在分子机制尚不清楚,因此我们开展了这项研究,通过动物和细胞实验进行探索,首次揭示了非奈利酮改善高血压心室重构和心功能的分子机制。这不仅为nsMRA心血管获益提供新机制和支持证据,拓展了非奈利酮的心血管保护谱,也为高血压靶器官损伤的干预策略提供新思路。
机制启示:非奈利酮通过多种途径发挥心脏保护作用
该研究观察到非奈利酮的心脏保护作用,可有效改善血压和心功能,同时减轻病理性心室重构和炎症反应。非奈利酮可直接抑制盐皮质激素受体(MR)过度活化,减少炎性反应和纤维化过程,从而对心血管和肾脏起到保护作用,延缓心肾疾病进展[8]。既往研究发现,MR激活可在心血管疾病中诱导内质网应激,而氧化应激和炎症反应都是已知的内质网应激触发因素,并与心肌细胞凋亡密切相关。我们这项研究支持MR与内质网应激通路之间存在功能联系,发现非奈利酮可能通过调节MR和内质网应激之间的串扰来减轻心室重构、发挥心脏保护作用。
我们在“两肾一夹”SD大鼠模型中观察到非奈利酮的降压作用,但内质网应激与降压作用的关联仍需进一步研究。既往研究发现,MRA通过抗炎、抗氧化应激和抗纤维化机制发挥直接的细胞保护作用,且这些作用部分独立于降压[9,10]。因此我们推测,非奈利酮可能通过多种途径发挥心脏保护作用,包括降压减轻负荷、抑制MR过度激活介导的内质网与氧化应激、炎症等,显示其多靶点、多通路的有益作用。
临床展望:非奈利酮在心血管领域的应用前景广阔
非奈利酮作为nsMRA的代表药物,在心血管领域的应用价值正在不断拓展之中。
在心血管风险管理领域,美国食品药品监督管理局(FDA)最初于2021年批准其用于降低2型糖尿病相关慢性肾脏病成人患者的心血管死亡、心力衰竭住院、非致命性心肌梗死及延缓肾病进展风险。目前,非奈利酮作为2型糖尿病相关慢性肾脏病的标准治疗药物,已成为心肾共治、改善心血管风险管理的有力武器。在心衰领域,FDA于2025年7月宣布扩大非奈利酮的适应证,将其适用范围扩展至左心室射血分数(LVEF)≥40%的心力衰竭患者,填补了HFpEF/HFmrEF的治疗空白。目前更多研究正在进行中,以进一步探索其在更广泛心衰患者中的应用价值,包括REDEFINE-HF研究、CONFIRMATION-HF研究和FINALITY-HF研究等。在高血压领域,非奈利酮在难治性高血压中展现出一定治疗潜力,而高血压也是HFpEF/HFmrEF心衰发生发展的重要原因。
总之,我们这项研究为非奈利酮的心脏保护作用提供了新的分子机制,也为其在高血压性心脏病中的应用提供了新的视角和依据。期待将来开展更多研究,进一步探索非奈利酮的作用机制及其在心血管领域的临床应用价值。

参考文献
1. Luettges K, et al. Am J Nephrol. 2022; 53(7): 552-564.
2. Hellenkamp K, et al. ESC Heart Fail. 2025 Sep 22. doi: 10.1002/ehf2.15424. Online ahead of print
3. An Y, et al. J Hypertens. 2025 Sep 25. doi: 10.1097/HJH.0000000000004167. Online ahead of print
4. Jin T, et al. Diabetol Metab Syndr. 2023; 15:87.
5. Lavall D, et al. Biochem Pharmacol. 2019; 168:173-183.
6. Bonnard B, et al. J Mol Cell Cardiol. 2018; 121:124-133.
7. Pitt B, et al. N Engl J Med. 2021; 385:2252-2263.
8. 《非奈利酮临床应用与药学监护中国专家共识》专家组. 中国药业. 2025;34(15):1-14.
9. Kuyama N, et al. J Am Heart Assoc. 2024; 13:e030941.
10. Thuzar M, et al. J Endocrinol. 2024; 263:e240119.
- 推荐文章
