- 首页 > 正文
周晓霜教授:KICU镇痛镇静实践经验
发表时间:2026-02-03 11:46:00

ICU患者的痛苦主要源自两方面:
(1)疾病与环境因素:患者因严重疾病难以自理,各种有创诊治操作带来疼痛。ICU环境嘈杂,昼夜不分,患者被约束于病床上,睡眠剥夺,邻床患者的抢救或去世等都会增加患者的痛苦。这些因素使患者感到极度的“无助”和“恐惧”,甚至危及生命安全。
(2)隐匿性疼痛与心理因素:气管插管及其他各种插管、长时间卧床等隐匿性疼痛常被忽视;患者对未来命运的忧虑,如对疾病预后的担心、死亡的恐惧以及对家人的思念与担心,这些心理因素与隐匿性疼痛相互作用,进一步加剧患者的焦虑与躁动,增加各器官的代谢负担,影响治疗效果。
因此,有效的镇痛镇静治疗可减轻患者的心理压力,促进康复,改善预后。镇痛和镇静治疗应作为ICU患者的常规治疗。在KICU临床实践中,下列情况下常需要应用镇静药物,例如:机械通气时、抗生素或抗帕金森药物等蓄积、老年性精神病、狼疮脑、脑膜炎等疾病。
二、镇痛镇静实施方法
KICU患者的镇痛镇静治疗需遵循规范的实施流程(图1)。根据2018年的指南,ICU患者镇痛镇静管理时应采取非药物措施,如减少声光刺激、改善睡眠、早期活动,改善患者舒适性。使用疼痛数字评分表(NRS)、行为疼痛量表(BPS)、重症监护疼痛观察量表(COPT)、Richmond躁动-镇静评分(RASS)、为镇静-躁动评分(SAS)、ICU患者意识模糊评估法(CMA-ICU)及重症监护谵妄筛查量表(ICDSC)等进行评估,并根据评估结果进行对症治疗。
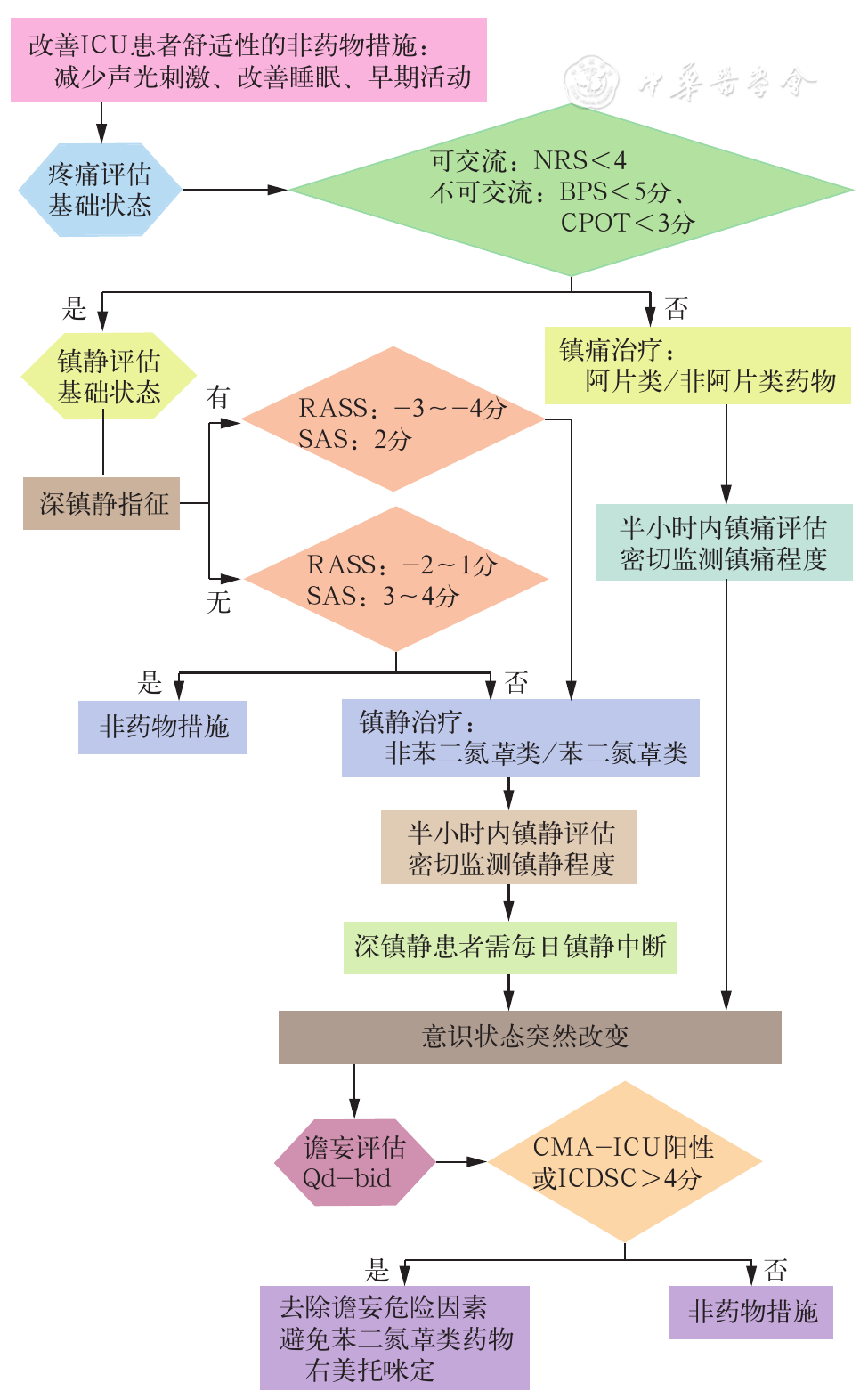
图1. 镇痛镇静实施流程
1、疼痛评估
疼痛评估患者基础状态。对于可交流的患者,当NRS<4 分,对于不可交流的患者,当BPS<5 分、CPOT<3 分时,进行镇静评估,否则需使用阿片类或非阿片类药物进行镇痛治疗,治疗后半小时内需再次评估镇痛程度,并密切监测。
2. 镇静评估
镇静深度的选择
保持危重症患者处于最舒适和安全的镇静状态是 ICU 镇静治疗的重要目标之一。因此需要定时评估患者的镇静程度以便确定镇静深度以及调整治疗方案,尽可能扬利抑弊。
对于器官功能相对稳定,恢复期的患者,应给予浅镇静,以减少机械通气时间和住 ICU 时间。而对处于应激急性期, 器官功能不稳定的患者,宜给予较深镇静以保护器官功能,这些情况包括:1)机械通气人机严重不协调者;(2)严重急性呼吸窘迫综合征早期短疗程神经-肌肉阻滞剂、俯卧位通气、肺复张等治疗时作为基础;(3)严重颅脑损伤有颅高压者;(4)癫痫持续状态;(5)外科需严格制动者。
镇静评估方法及治疗
RASS和SAS评分法简单、易操作、指示性好,是评估镇静深度及镇静质量最有效和可靠的方法。浅镇静时,RASS -2~1分,SAS 3~4分,采取非药物措施;较深镇静时,RASS -3~-4分,SAS 2分;当合并应用神经-肌肉阻滞剂时,RASS -5分,SAS 1分。深镇静时,采用非苯二氮䓬类或苯二氮䓬类进行镇静治疗。
镇静监测与镇静中断
治疗后半小时内需评估镇静程度并密切监测,深镇静患者还需实施每日镇静中断(DIS)。需注意,目前无证据显示DSI对患者有益。
3、谵妄评估及干预
谵妄评估与干预是镇痛镇静治疗的重要组成部分。谵妄综合征是一种急性精神错乱状态,分为活动亢进型、多动抑制性和混合型,老年患者多见。活动亢进型表现为高警觉、躁动不安;抑制性表现为不易被唤醒、嗜睡等,症状易被忽视。KICU患者因焦虑、手术麻醉、代谢异常、缺氧、循环不稳定、神经系统病变及ICU特殊环境等原因,易出现谵妄症状。对于RASS评分≥-2分且具有谵妄相关危险因素的患者,应常规使用CAM-ICU或ICDSC进行评估。
对于CMA-ICU阳性或者ICDSC>4分的患者,需去除谵妄危险因素。例如,改善睡眠的时间及质量,治疗脱水、心衰、电解质紊乱、感染、贫血、低氧、低血压等,安排专人陪护,协助活动和物理治疗,减少环境嘈杂,创造舒适环境。右美托咪定可减少谵妄发生,不建议应用氟哌啶醇、他汀类药物等预防及治疗谵妄。
三、镇痛镇静药物特点
1、镇痛药物
阿片类药物
CU患者非神经性疼痛,建议首选阿片类药物作为镇痛药物。阿片类药物为强效中枢镇痛剂之一,具有镇痛效果强、起效快、可调性强、价格低廉等优点。
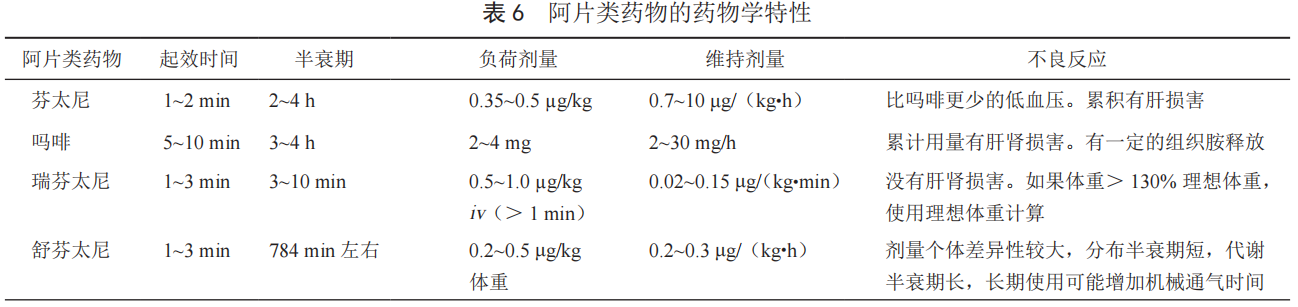
常用阿片类药物及其特性见表1,需根据每类药物的特点用药。芬太尼镇痛效价是吗啡的100~180倍,但蓄积性强,不宜作为长期镇痛治疗药物。瑞芬太尼起效快,维持时间短,能明显缩短机械通气时间和ICU住院时间。舒芬太尼镇痛作用很强,为芬太尼的5~10倍,近年来在ICU重症患者中的应用逐渐增多。
表1. 常用阿片类药物的药物学特性
非阿片类药物的联合应用
近年逐渐有研究表明氯胺酮、非甾体类抗炎药、奈福泮和加巴喷丁等非阿片类镇痛药物能有效减轻重症患者的非神经性疼痛。建议联合应用非阿片类镇痛药物以减少阿片类药物的用量和相关不良反应。其中加巴喷丁对神经性疼痛疗效显著,联合使用阿片类药物可提高镇痛效果,降低阿片剂量需求,减少恶心、呕吐等副作用。
2、镇静药物
对于镇静药物,需根据每类药物的特点用药(表2)。
表2. 常用镇静药物特点
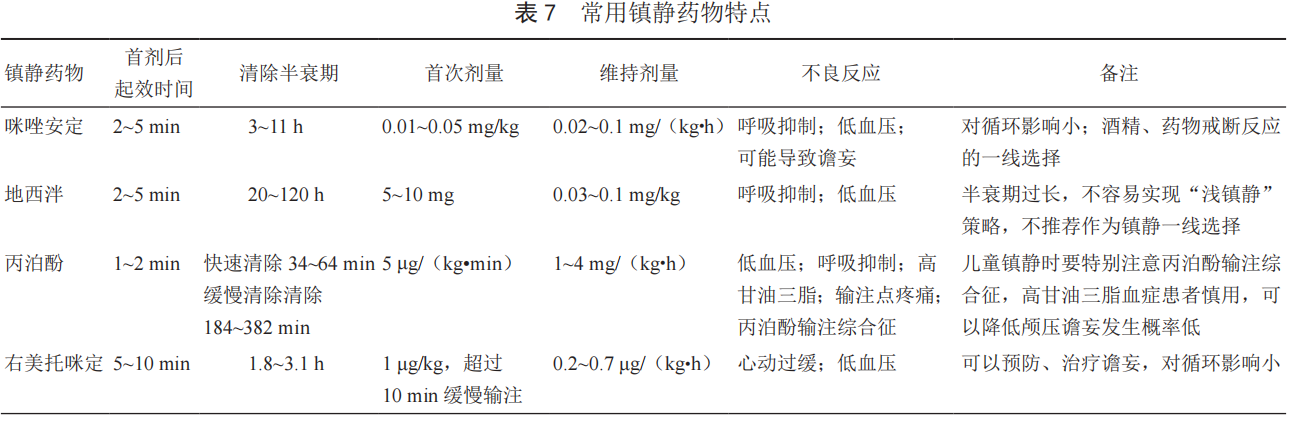
苯二氮卓类和丙泊酚仍然应作为目前镇静治疗的基本药物。
苯二氮卓类(咪达唑仑、地西泮等)是中枢神经系统γ氨基丁酸受体激动剂,具有抗焦虑、遗忘、镇静、催眠和抗惊厥作用,但易引起蓄积、代谢较慢,增加镇静深度,从而进一步延长机械通气时间及住院时间。
丙泊酚起效快、作用时间短,撤药后能快速清醒,且镇静深度呈剂量依赖性;但其使用时可出现外周静脉注射痛,长期使用后可能出现诱导耐药。
右美托咪定通过拮抗中枢及外周儿茶酚胺的作用,兼具轻度镇静和镇痛效果,与其他镇痛镇静药物具有协同作用,可以减少机械通气时间和ICU住院时间,但会增加心动过缓和低血压事件的发生。使用时需注意输注速度,必要时可适当延长输注时间。
镇静药物选择应根据患者的具体病情、器官功能状态以及治疗目标,综合考虑药物的特点和潜在风险,个体化地制定镇静治疗方案。
3. 镇痛与镇静的关系
疼痛是引起患者躁动的重要原因,应优先镇痛。镇痛不足时,单纯镇静难以达到理想效果。优先镇痛有助于减少镇静药物用量,降低镇静相关并发症,提高患者舒适度,促进早期康复。临床实施中,患者入 ICU 即应进行疼痛评估,及时给予镇痛治疗,并动态监测疼痛变化,适时调整治疗方案。
四、KICU实践总结与常用药方案
KICU根据不同疼痛与镇静需求制定了规范化给药方案。
常用的镇痛药物中,瑞芬太尼的常用配置方式为2 mg瑞芬太尼加入50 ml的0.9 NS中微量泵泵入(1.8~13.5 mg/h),控制剂量在0.02~0.15 μg/kg/min。
镇静常用药物种类较多:丙泊酚规格为50 ml/500 mg,使用原液,以1.8 ml~24 ml/h的速度泵入,每小时剂量控制在0.3~4 mg/kg;右美托咪定首剂1 μg/kg静推(>10 min),后续维持0.2~0.7 μg/kg/h;咪达唑仑的常用配置方式为0.9% NS 40 ml加米达唑仑50 mg,以 1~7ml/h 的速度泵入。
非传统意义上的镇静药物利培酮、奥氮平等亦根据药物剂型及具体指征使用,剂量调整依患者反应灵活设定。例如,利培酮口服液(30 mg/30 ml),对于成年患者,起始剂量为1 mg/次,一日2次,第2和第3日可依次增加至2 mg/次、3 mg/次。对于老年或肝功异常病和肾病患者,起始剂量为0.5 mg/次;奥氮平国内常见规格为片剂2.5 mg、5 mg、10 mg,对肾、肝脏功能损害的患者应考虑较低的起始剂量(5 mg),并慎重加量。
总结及展望
KICU镇痛镇静治疗是一个复杂而重要的医疗过程,未来仍有诸多方面值得进一步探索与改进,包括:更加注重根据患者的个体差异(如年龄、性别、基础疾病等)制定个性化的镇痛镇静治疗方案;积极关注并引进新型镇痛镇静药物,尤其是低副作用药物;加强与麻醉科、神经内科、心内科等多学科的协作,共同探讨镇痛镇静治疗在复杂疾病中的应用策略;利用人工智能、大数据等先进技术,开发更加智能、精准的镇痛镇静评估与监测工具,提高治疗效率与效果;加强对患者的教育与心理支持,提高其对镇痛镇静治疗的认知与接受度,促进患者积极配合治疗,加速康复进程。
- 推荐文章
