- 首页 > 正文
ALIGN研究事后分析揭示阿曲生坦对IgA肾病亚组蛋白尿的降低作用
发表时间:2025-08-19 16:47:06
编者按:在第62届欧洲肾脏协会大会(ERA 2025)上,荷兰格罗宁根大学医学中心Hiddo J.L. Heerspink博士分享了ALIGN研究事后分析的数据。阿曲生坦作为强效、高选择性内皮素A受体拮抗剂,在IgA肾病Ⅲ期试验中已展现降低蛋白尿的潜力。此次聚焦MEST-C评分、基线血尿及UPCR等亚组的分析,进一步验证其在不同疾病表型IgAN患者(含蛋白尿程度较低者)中降低尿蛋白的疗效,为阿曲生坦治疗IgA肾病提供更细化证据,也助力临床精准管理这类疾病,其加速获批也彰显该疗法在肾病领域的应用前景,值得肾脏病学界关注与深入探讨。
引言
阿曲生坦是一种强效、高选择性的内皮素A(ETA)受体拮抗剂,可抑制由蛋白尿和足细胞损伤激活的ETA受体。通过选择性阻断ETA受体,阿曲生坦有潜力减少肾脏足细胞应激、内皮系统激活等情况。在IgA肾病(IgAN)的Ⅲ期ALIGN(NCT05734710)全球试验中,阿曲生坦(1.39 mg,每日一次)相较于安慰剂,在36周时显著且具临床意义地降低了蛋白尿,降幅达36.1%(95%CI:29.4%~41.9%),安全性和耐受性良好(中期分析)。
目的
这些事后分析的目的是通过已知的疾病进展预后指标,评估阿曲生坦的疗效。具体而言,依据从基线到第36周时24小时尿蛋白肌酐比(UPCR)的变化来进行评估,涉及的疾病进展预后指标包括基线蛋白尿(UPCR<1或≥1 g/g)、MEST - C 评分以及基线血尿情况。
方法
ALIGN试验纳入经活检证实为IgA肾病、尿蛋白排泄量经优化治疗(最大耐受肾素-血管紧张素系统抑制剂和稳定剂量他汀类药物)后仍≥1 g/d的成人患者。
在ALIGN中,用24小时UPCR(而非24小时尿蛋白定量)来定义纳入标准(即eGFR≥30 ml/(min·1.73m2)且尿蛋白排泄量≥1g/天,通过24小时UPCR评估),以评估阿曲生坦的疗效。将基线24小时UPCR<1 g/g的患者排除在主要疗效分析(即基于尿蛋白排泄量≥1 g/d的分析)之外。
患者被随机分配接受阿曲生坦0.75 mg或安慰剂治疗,每日一次,持续36周。
这些事后分析基于中期分析数据(采用MRMN[多变量重复测量模型],使用前270例入组主要试验的患者数据)。亚组分析聚焦于基线时有MEST-C评分可用的患者(即纳入那些基线有MEST-C评分数据的患者)。
结果
无论基线尿蛋白肌酐比(UPCR)水平(<1 或≥1g/g)、MEST - C 评分如何,也不管基线血尿水平怎样,阿曲生坦在 36 周时均能使 UPCR 实现具有临床意义的降低(相较于安慰剂)。
基线蛋白尿:基线时,分别有56例和208例患者的UPCR<1.0 g/g和≥1.0 g/g。对于基线UPCR<1.0 g/g和≥1.0 g/g的患者,相较于安慰剂,36周时蛋白尿的百分比变化分别为-28.7(95%CI:-47.5~-3.2)和-38.3(95%CI:-47.4~-27.5)(图1和图2)。
基线MEST-C评分:MEST-C亚组分析结果显示,无论基线肾活检时是否存在系膜细胞增生(M1/M0)、内皮细胞增生(E1/E0)、节段性肾小球硬化(S1/S0)、肾小管萎缩/间质纤维化(T1-T2/T0)或新月体(C1-C2/C0),阿曲生坦(相较于安慰剂)均显示出优势(图1)。
基线血尿:基线时,129例患者无血尿/仅有微量血尿,116例患者血尿等级为1+或更高。对于无/微量、中度和重度血尿水平的患者,相较于安慰剂,36周时蛋白尿的百分比变化分别为-30.0(95%CI:-43.1~-13.9)、-40.7(95%CI:-43.1~-13.9)、-40.7(95%CI:-53.9~-23.6)和-53.1(95%CI:-70.9~-24.2)(图1)。
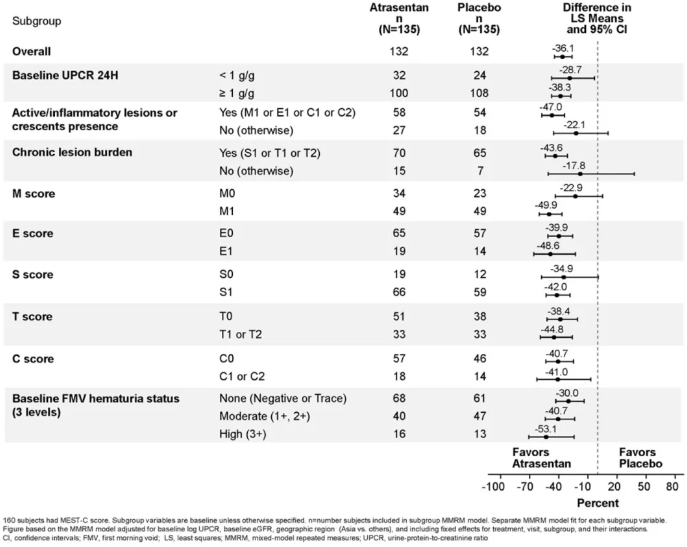
图1. 基于基线蛋白尿水平、MEST-C评分及基线血尿情况,采用多变量重复测量模型(MMRM)分析第36周时尿蛋白肌酐比(UPCR)相对安慰剂的百分比变化
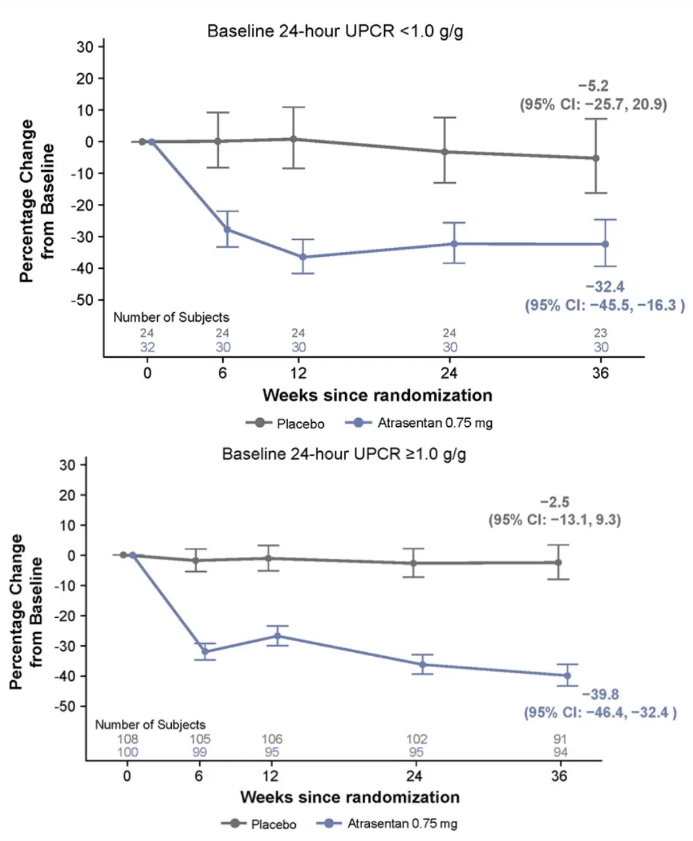
图2. 按基线蛋白尿(24小时尿蛋白肌酐比<1.0 g/g和≥1.0 g/g)分层,采用多变量重复测量模型(MMRM)分析从基线到第36周尿蛋白肌酐比(UPCR)的百分比变化
结论
这些亚组分析的结果与 36 周时的主要分析结果一致;无论基线 24 小时尿蛋白肌酐比(UPCR)(<1 g/g 和≥1 g/g )、MEST - C 评分以及基线血尿情况如何,在 IgA 肾病(IgAN)患者中均观察到了阿曲生坦的疗效(基于 UPCR 百分比变化与安慰剂对比 )。
这些数据支持阿曲生坦作为广泛 IgA 肾病患者基础治疗的潜力,涵盖蛋白尿程度较低以及疾病表型不同的患者。
基于正在进行的 Ⅲ 期 ALIGN 研究的预先指定中期分析,阿曲生坦(VANRAFIA? )于 2025 年 4 月 2 日获得美国 FDA 针对原发性 IgA 肾病的加速批准 。
引言
阿曲生坦是一种强效、高选择性的内皮素A(ETA)受体拮抗剂,可抑制由蛋白尿和足细胞损伤激活的ETA受体。通过选择性阻断ETA受体,阿曲生坦有潜力减少肾脏足细胞应激、内皮系统激活等情况。在IgA肾病(IgAN)的Ⅲ期ALIGN(NCT05734710)全球试验中,阿曲生坦(1.39 mg,每日一次)相较于安慰剂,在36周时显著且具临床意义地降低了蛋白尿,降幅达36.1%(95%CI:29.4%~41.9%),安全性和耐受性良好(中期分析)。
目的
这些事后分析的目的是通过已知的疾病进展预后指标,评估阿曲生坦的疗效。具体而言,依据从基线到第36周时24小时尿蛋白肌酐比(UPCR)的变化来进行评估,涉及的疾病进展预后指标包括基线蛋白尿(UPCR<1或≥1 g/g)、MEST - C 评分以及基线血尿情况。
方法
ALIGN试验纳入经活检证实为IgA肾病、尿蛋白排泄量经优化治疗(最大耐受肾素-血管紧张素系统抑制剂和稳定剂量他汀类药物)后仍≥1 g/d的成人患者。
在ALIGN中,用24小时UPCR(而非24小时尿蛋白定量)来定义纳入标准(即eGFR≥30 ml/(min·1.73m2)且尿蛋白排泄量≥1g/天,通过24小时UPCR评估),以评估阿曲生坦的疗效。将基线24小时UPCR<1 g/g的患者排除在主要疗效分析(即基于尿蛋白排泄量≥1 g/d的分析)之外。
患者被随机分配接受阿曲生坦0.75 mg或安慰剂治疗,每日一次,持续36周。
这些事后分析基于中期分析数据(采用MRMN[多变量重复测量模型],使用前270例入组主要试验的患者数据)。亚组分析聚焦于基线时有MEST-C评分可用的患者(即纳入那些基线有MEST-C评分数据的患者)。
结果
无论基线尿蛋白肌酐比(UPCR)水平(<1 或≥1g/g)、MEST - C 评分如何,也不管基线血尿水平怎样,阿曲生坦在 36 周时均能使 UPCR 实现具有临床意义的降低(相较于安慰剂)。
基线蛋白尿:基线时,分别有56例和208例患者的UPCR<1.0 g/g和≥1.0 g/g。对于基线UPCR<1.0 g/g和≥1.0 g/g的患者,相较于安慰剂,36周时蛋白尿的百分比变化分别为-28.7(95%CI:-47.5~-3.2)和-38.3(95%CI:-47.4~-27.5)(图1和图2)。
基线MEST-C评分:MEST-C亚组分析结果显示,无论基线肾活检时是否存在系膜细胞增生(M1/M0)、内皮细胞增生(E1/E0)、节段性肾小球硬化(S1/S0)、肾小管萎缩/间质纤维化(T1-T2/T0)或新月体(C1-C2/C0),阿曲生坦(相较于安慰剂)均显示出优势(图1)。
基线血尿:基线时,129例患者无血尿/仅有微量血尿,116例患者血尿等级为1+或更高。对于无/微量、中度和重度血尿水平的患者,相较于安慰剂,36周时蛋白尿的百分比变化分别为-30.0(95%CI:-43.1~-13.9)、-40.7(95%CI:-43.1~-13.9)、-40.7(95%CI:-53.9~-23.6)和-53.1(95%CI:-70.9~-24.2)(图1)。

图1. 基于基线蛋白尿水平、MEST-C评分及基线血尿情况,采用多变量重复测量模型(MMRM)分析第36周时尿蛋白肌酐比(UPCR)相对安慰剂的百分比变化

图2. 按基线蛋白尿(24小时尿蛋白肌酐比<1.0 g/g和≥1.0 g/g)分层,采用多变量重复测量模型(MMRM)分析从基线到第36周尿蛋白肌酐比(UPCR)的百分比变化
结论
这些亚组分析的结果与 36 周时的主要分析结果一致;无论基线 24 小时尿蛋白肌酐比(UPCR)(<1 g/g 和≥1 g/g )、MEST - C 评分以及基线血尿情况如何,在 IgA 肾病(IgAN)患者中均观察到了阿曲生坦的疗效(基于 UPCR 百分比变化与安慰剂对比 )。
这些数据支持阿曲生坦作为广泛 IgA 肾病患者基础治疗的潜力,涵盖蛋白尿程度较低以及疾病表型不同的患者。
基于正在进行的 Ⅲ 期 ALIGN 研究的预先指定中期分析,阿曲生坦(VANRAFIA? )于 2025 年 4 月 2 日获得美国 FDA 针对原发性 IgA 肾病的加速批准 。
- 推荐文章
肾例明鉴 | 老年男性ANCA相关性血管炎伴口干、眼干:只是非特异性抗体阳性?还是重叠综合征?——1例病例报告并文献综述
恩格列净+非奈利酮联用,高钾血症风险几何?CONFIDENCE试验二次分析结果揭晓
人人享有肾脏健康:关爱生命,守护地球——2026年世界肾脏日公益活动举行
14:00直播!2026年世界肾脏日公益活动即将开始——人人享有肾脏健康:关爱生命,守护地球
血液透析的环境挑战与可持续发展路径探索——2026世界肾脏日特别关注
特别策划 | 世界肾脏日:您真的了解肾脏健康吗?
肾域华章 | 儿童增殖性狼疮肾炎初始治疗添安全新选:多中心RCT证实吗替麦考酚酯非劣效于环磷酰胺选
2026世界肾脏日 | 绿色肾移植十策:让肾移植告别等待,共护双肾与地球
靶向清除“僵尸细胞”,达沙替尼联合槲皮素为糖尿病肾病治疗开辟新路径
慢性肾脏病与认知障碍:肾病越重,认知风险越高?——基于CRIC研究的新发现
膜性肾病精准诊疗的新证据:生物标志物和临床病理特征研究进展
eGFR百分位数:CKD早期识别的个性化新工具
PI解读:FSGS治疗新曙光——靶向药物迎来突破性进展
突破性进展:靶向补体因子B的RNA疗法为IgA肾病治疗带来新希望
利妥昔单抗血药浓度:膜性肾病早期治疗反应的预测标志物
肾例明鉴|43岁男子双下肢水肿、肌酐飙升,背后竟是两种肾病罕见叠加作祟!膜性肾病合并抗GBM病该如何破局?
Richard Lafayette教授:新型补体抑制剂时代下荚膜菌感染的防控指南
孙英贤教授牵头多中心研究:CRHCP事后分析揭秘CKM综合征不同分期强化降压价值
肾识百科|娃的肾病竟是遗传的?6种遗传性肾病家长必知!
护肾先护肠?1.2万人的迄今最大研究发现:肠道菌群及其代谢产物参与肾功能早期变化
肥胖与慢性肾脏病:不可忽视的“代谢多米诺”
《柳叶刀》:TRPC6抑制剂BI 764198治疗FSGS的Ⅱ期临床试验取得积极结果,为其足细胞靶向治疗提供首个有效证据
长期血透别忽视疼痛!平均8个部位受累,84%病程超1年、75%每日受折磨,肌肉骨骼和神经病理性痛为主要类型
近16万人数据:这样吃,大脑更年轻
美国麻省总医院最新综述:CKD-aP的诊疗进展与未来方向
超88%患者未获诊疗!Ⅲ期研究首证中国血透CKD-aP人群可从Difelikefalin治疗中获益
睡不好,血糖更难控?最新研究揭示:睡眠障碍正在悄悄扰乱你的“升糖”与“降糖”激素!
KDIGO肾小球疾病指南工作组主席Jürgen Floege教授:补体旁路途径是驱动CMKDs肾小球炎症的核心引擎
沉默的神偷!无声无息偷走小孩子肾脏功能的遗传性肾病——Dent病
国际组织在行动:CKM综合征、新型超级专科与“关爱肾脏”倡议
白蛋白尿——盐皮质激素受体拮抗剂带来肾脏获益的核心驱动因素
补体靶向时代:IgA肾病新疗法的疗效排名与精准化探索
从认知到实践:中国肾脏科医生IgA肾病诊疗现状与差距
肾例明鉴丨年轻痛风不是小事!19岁小伙关节痛3年,没控尿酸把肾“熬”成慢性肾病Ⅲ期
尿酸与非酒精性脂肪肝的“隐秘关联”:高血压人群需警惕的代谢信号
狼疮肾炎患者妊娠:她安然度过,她产后风暴骤起——来自两个临床病例研究的启示
罕见的先天性肾脏发育不良疾病——肾小球巨大而又稀少的“寡巨肾”,你听说过吗?
阿塞西普:IgA肾病治疗的新曙光——ORIGIN 3试验中期数据深度剖析
生殖史如何塑造年轻女性的心肾代谢风险?
指南共识丨《IgA肾病临床实践60问(2026版)》核心要点与临床实践解读(附原文)
司美格鲁肽获批治疗2型糖尿病合并慢性肾脏病1周年:糖尿病、肾脏与心脏疾病领域的变革
佳节健康“喝”出来——咖啡与茶,提神背后的健康双面性
春节期间重磅新闻速递:膜性肾病、IgA肾病、卵巢功能早衰领域迎来治疗新进展
“钾”在悄悄溜走,肾脏在喊“救命”!一种罕见的遗传性失盐性肾小管疾病
冬季假期真的会“悄悄让人发胖”吗?
肾友过年“四大护法”!作息·出行·娱乐·情绪,这份春节健康手册请收好
新春护肾,安心团圆:肾友及四高人群春节健康全攻略
学术纵横|多维靶向,精准护肾:小干扰RNA、ASI、nsMRA、GLP-1RA等新型药物均可为CKD患者保驾护航
尿糖阳性=糖尿病?那可不一定!这种罕见肾病会遗传尿糖,别当成普通糖尿病来治
聚焦CKM综合管理,恒格列净相关复方制剂赋能心-肾-代谢多重获益
年度盘点丨周晓玲教授:肥胖相关慢性肾脏病的诊治进展
肾例明鉴丨服药后肺肾接连“报警”!20岁女生的惊魂经历:元凶竟是治疗甲亢的丙硫氧嘧啶
谨慎“跟风养生”!Omega-3、生酮饮食、禁糖等营养宣传需辩证对待
肾识百科丨肾友想生娃?4类可怀情况 + 3类禁忌,提前看清不踩坑
警惕身体的“代谢紊乱风暴”!代谢综合征——引人关注的肾脏“杀手”
