- 首页 > 正文
Nature最新荟萃分析:再次确认白蛋白尿变化作为CKD临床试验的替代终点——基于48项RCTs、85 681例样本量
发表时间:2026-01-30 12:08:17
引言
CKD影响全球逾8.4亿人,是肾衰竭、心血管事件和早亡的首要原因之一。继肾素-血管紧张素系统抑制剂(RASi)后,SGLT2i、nsMRA等新药相继进入临床,患者残余风险依然显著。传统“硬终点”——肾衰竭或估算肾小球滤过率(eGFR)持续下降≥50%——往往需长期随访,早期疗效评估因此成为新药开发的瓶颈。UACR因与肾小球基底膜损伤、肾小管间质炎症及远期预后密切相关,被持续探讨作为替代终点,但既往证据多局限于RASi类药物,且缺乏跨病因、跨干预手段的大规模验证。
研究在既往41项随机对照试验(RCT)基础上,补充2020~2025年发表的7项新试验,最终纳入48项RCT、85681例参与者,涵盖糖尿病肾病、非糖尿病CKD及IgA肾病三大病因;其中女性占34%,基线eGFR 45.6~71.4 ml/(min·1.73㎡),中位UACR 213~1069 mg/g,具有广泛代表性(表1)。
作者采用两阶段贝叶斯模型:首先利用个体参与者数据计算每项试验的6个月UACR几何均数比(GMR)与硬终点风险比(HR),再以试验为单元进行荟萃回归,评估斜率、截距、决定系数(R2)及残差均方(RMSE),并定义R2<0.49、0.49~0.72、>0.72分别为弱、中、强替代证据。硬终点统一为“肾衰竭[eGFR<15 ml/(min·1.73㎡)、长期透析或肾移植]或血清肌酐持续倍增”;敏感性分析采用“单纯肾衰竭”。
结果显示,48项试验中,治疗导致UACR较基线降低25%(GMR 0.75;95%CI:0.71~0.79),硬终点风险降低24%(HR 0.76;95%CI:0.71~0.82)。meta回归斜率0.68(95% BCI 0.17~1.19),提示几何平均数UACR每降低30%,硬终点风险平均降低19%(95% BCI 5~30%)。R2中位数0.66(95% BCI 0.06~0.98),后验概率45%达到“强替代”,28%为“弱替代”,截距-0.05,基本通过零点,符合“无UACR变化即无平均临床获益”的因果前提。
亚组分析表明,糖尿病肾病18项(n=72 309)、非糖尿病CKD 23项(n=12 335)、IgA肾病7项(n=1037)中,UACR变化与临床终点的治疗效益的关联性(HR)依次为0.65、0.66、1.35(图1),IgA肾病点估计最高,但95%贝叶斯可信区间(BCI)宽泛,尚不能认定异质性。以基线eGFR 45、60、75 ml/(min·1.73㎡)分层,斜率随肾功能改善而增大(0.58→1.57),R2亦升高(0.67→0.94),提示肾功能较好人群白蛋白尿变化对远期结局预测价值更高;基线UACR水平及eGFR年下降速率未显著改变斜率。
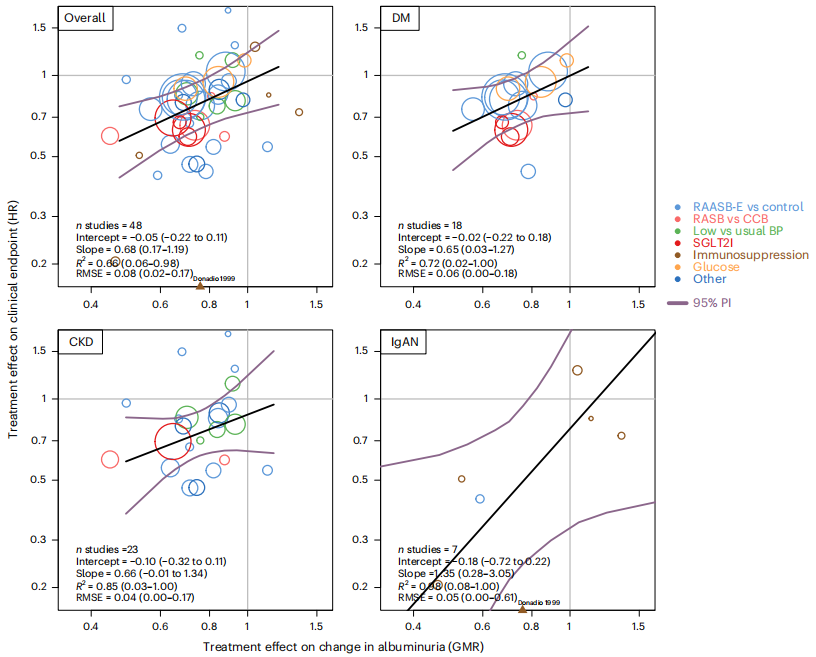
图1. UACR的治疗效益与临床终点的治疗效益的关联性分析
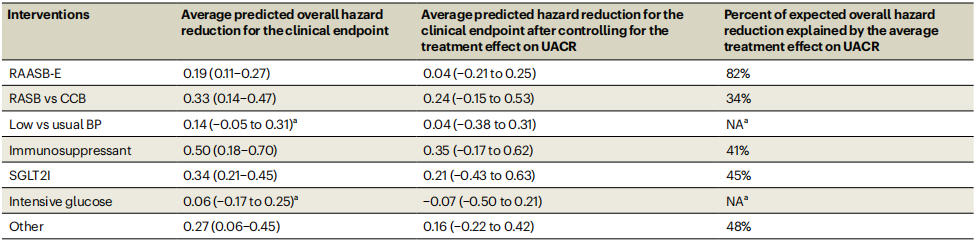
药物类别层面,RAAS阻断剂/内皮素拮抗剂(RAASB-E)类82%的硬终点获益可通过UACR下降解释;SGLT2i、免疫抑制剂、RASI vs. 钙通道阻滞剂分别解释45%、41%、34%(表2),提示后者存在非白蛋白尿途径的肾保护机制。以200例样本为例,若治疗组UACR下降30%,硬终点HR预测中位数0.75,95%预测区间0.57~0.95,临床获益(HR<1)概率>99%;如要求97.5%的把握度,UACR降幅需达约27%。
作者指出,Ⅱ期试验若观察到25%以上UACR下降,可高概率推断Ⅲ期获益,为剂量选择、Go/No-go决策提供量化阈值;在IgA肾病或儿科人群中,可将6个月UACR变化作为条件终点,结合后续安全性与硬终点事件,实现“先批准后验证”。对于抗炎、抗纤维化等机制未明药物,建议同步测量UACR与eGFR斜率,采用近期发表的“双终点”贝叶斯框架,提高预测精度。RAASB-E类获益与UACR下降高度重合,可优先采用白蛋白尿作为主要终点;SGLT2i、GLP-1受体激动剂、nsMRA等药物需关注血糖、血流动力学、炎症等多通路效应,白蛋白尿仅部分反映疗效。
研究优势在于个体水平数据保证终点定义一致;覆盖新机制药物及不同病因;贝叶斯方法量化不确定度;提供样本量-预测区间-获益概率一站式表格,直接服务试验设计。局限包括部分试验因数据共享限制未纳入;女性、青少年及进展较慢(eGFR年下降<2 ml/(min·1.73㎡))人群代表性不足;白蛋白尿检测方法、随访时长存在异质;R2置信区间仍宽,需继续积累试验。
综上,该研究在迄今最大规模、最多样化的CKD试验荟萃中证实:6个月UACR降低30%与肾衰竭风险降低19%稳健相关,跨病因、跨药物类别一致。未来工作将纳入更多IgA肾病、局灶节段性肾小球硬化及儿童试验,结合eGFR斜率与生物标志物组学,建立多维度、动态更新的替代终点体系,为CKD新药快速上市与精准治疗奠定循证基础。
近期,一项最大规模荟萃证实:在慢性肾脏病(CKD)患者中,6个月尿白蛋白/肌酐比(UACR)降低30%与临床肾脏硬终点事件风险降低19%显著相关,同时RAAS阻断剂/内皮素受体拮抗剂类药物82%的硬终点获益由UACR下降驱动,而钠-葡萄糖共转运蛋白2抑制剂(SGLT2i)、GLP-1受体激动剂、非甾体类盐皮质激素受体拮抗剂(nsMRA)等新型药物需关注血糖、血流动力学、炎症等多通路效应,白蛋白尿仅部分反映疗效。
研究背景
CKD影响全球逾8.4亿人,是肾衰竭、心血管事件和早亡的首要原因之一。继肾素-血管紧张素系统抑制剂(RASi)后,SGLT2i、nsMRA等新药相继进入临床,患者残余风险依然显著。传统“硬终点”——肾衰竭或估算肾小球滤过率(eGFR)持续下降≥50%——往往需长期随访,早期疗效评估因此成为新药开发的瓶颈。UACR因与肾小球基底膜损伤、肾小管间质炎症及远期预后密切相关,被持续探讨作为替代终点,但既往证据多局限于RASi类药物,且缺乏跨病因、跨干预手段的大规模验证。
研究目的
Heerspink等代表CKD-EPI临床试验协作组,系统更新并扩大样本,检验“治疗6个月内UACR变化”与“硬终点”之间的量效关系是否在不同病因、不同药物类别及不同疾病严重程度中保持一致,为监管审批与Ⅲ期试验设计提供量化依据。
研究方法
研究在既往41项随机对照试验(RCT)基础上,补充2020~2025年发表的7项新试验,最终纳入48项RCT、85681例参与者,涵盖糖尿病肾病、非糖尿病CKD及IgA肾病三大病因;其中女性占34%,基线eGFR 45.6~71.4 ml/(min·1.73㎡),中位UACR 213~1069 mg/g,具有广泛代表性(表1)。
表1. 荟萃分析纳入的患者基线特征与肾病种类
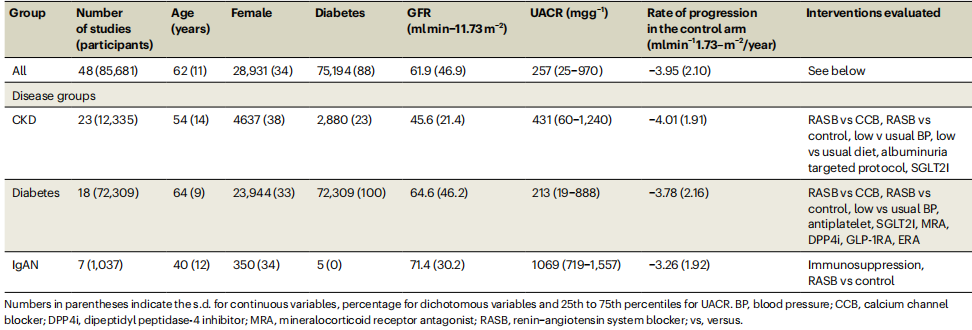
作者采用两阶段贝叶斯模型:首先利用个体参与者数据计算每项试验的6个月UACR几何均数比(GMR)与硬终点风险比(HR),再以试验为单元进行荟萃回归,评估斜率、截距、决定系数(R2)及残差均方(RMSE),并定义R2<0.49、0.49~0.72、>0.72分别为弱、中、强替代证据。硬终点统一为“肾衰竭[eGFR<15 ml/(min·1.73㎡)、长期透析或肾移植]或血清肌酐持续倍增”;敏感性分析采用“单纯肾衰竭”。
研究结果
结果显示,48项试验中,治疗导致UACR较基线降低25%(GMR 0.75;95%CI:0.71~0.79),硬终点风险降低24%(HR 0.76;95%CI:0.71~0.82)。meta回归斜率0.68(95% BCI 0.17~1.19),提示几何平均数UACR每降低30%,硬终点风险平均降低19%(95% BCI 5~30%)。R2中位数0.66(95% BCI 0.06~0.98),后验概率45%达到“强替代”,28%为“弱替代”,截距-0.05,基本通过零点,符合“无UACR变化即无平均临床获益”的因果前提。
亚组分析表明,糖尿病肾病18项(n=72 309)、非糖尿病CKD 23项(n=12 335)、IgA肾病7项(n=1037)中,UACR变化与临床终点的治疗效益的关联性(HR)依次为0.65、0.66、1.35(图1),IgA肾病点估计最高,但95%贝叶斯可信区间(BCI)宽泛,尚不能认定异质性。以基线eGFR 45、60、75 ml/(min·1.73㎡)分层,斜率随肾功能改善而增大(0.58→1.57),R2亦升高(0.67→0.94),提示肾功能较好人群白蛋白尿变化对远期结局预测价值更高;基线UACR水平及eGFR年下降速率未显著改变斜率。

图1. UACR的治疗效益与临床终点的治疗效益的关联性分析
药物类别层面,RAAS阻断剂/内皮素拮抗剂(RAASB-E)类82%的硬终点获益可通过UACR下降解释;SGLT2i、免疫抑制剂、RASI vs. 钙通道阻滞剂分别解释45%、41%、34%(表2),提示后者存在非白蛋白尿途径的肾保护机制。以200例样本为例,若治疗组UACR下降30%,硬终点HR预测中位数0.75,95%预测区间0.57~0.95,临床获益(HR<1)概率>99%;如要求97.5%的把握度,UACR降幅需达约27%。
研究意义和总结
作者指出,Ⅱ期试验若观察到25%以上UACR下降,可高概率推断Ⅲ期获益,为剂量选择、Go/No-go决策提供量化阈值;在IgA肾病或儿科人群中,可将6个月UACR变化作为条件终点,结合后续安全性与硬终点事件,实现“先批准后验证”。对于抗炎、抗纤维化等机制未明药物,建议同步测量UACR与eGFR斜率,采用近期发表的“双终点”贝叶斯框架,提高预测精度。RAASB-E类获益与UACR下降高度重合,可优先采用白蛋白尿作为主要终点;SGLT2i、GLP-1受体激动剂、nsMRA等药物需关注血糖、血流动力学、炎症等多通路效应,白蛋白尿仅部分反映疗效。
研究优势在于个体水平数据保证终点定义一致;覆盖新机制药物及不同病因;贝叶斯方法量化不确定度;提供样本量-预测区间-获益概率一站式表格,直接服务试验设计。局限包括部分试验因数据共享限制未纳入;女性、青少年及进展较慢(eGFR年下降<2 ml/(min·1.73㎡))人群代表性不足;白蛋白尿检测方法、随访时长存在异质;R2置信区间仍宽,需继续积累试验。
综上,该研究在迄今最大规模、最多样化的CKD试验荟萃中证实:6个月UACR降低30%与肾衰竭风险降低19%稳健相关,跨病因、跨药物类别一致。未来工作将纳入更多IgA肾病、局灶节段性肾小球硬化及儿童试验,结合eGFR斜率与生物标志物组学,建立多维度、动态更新的替代终点体系,为CKD新药快速上市与精准治疗奠定循证基础。
Heerspink HJL, et al. Nature Medicine. Published online: 06 November 2025. https://doi.org/10.1038/s41591-025-04057-z
- 推荐文章
ERA 2026前沿 | 突破诊疗壁垒,迈向全程管理:构建以SGLT2i为核心的CKD早筛早诊早治新格局
ERA 2026十佳摘要丨中国台湾长庚医院单细胞图谱揭秘多囊肾发病源头,锁定全新靶向治疗靶点
ERA 2026丨突破9个月疗程,布地奈德肠溶胶囊长程治疗,为IgA肾病患者带来持久肾功能保护
ERA 2026 | 香港大学研究揭示:脂联素经线粒体重塑途径改善糖胖病相关肾损伤
杨淑敏教授:被忽视的20%——内分泌性高血压筛查专家共识解读
ERA 2026格拉斯哥正式启幕!以开放思维锚定肾病未来,《柳叶刀》重磅数据敲响CKD全球防控警钟
ERA 2026重磅丨IgA肾病尽早对因治疗:锚定蛋白尿≥0.5 g/d肾病进展风险人群,早用早达标、护肾更及时
ERA 2026前沿 | 突破“5.0时代”,迈向长期管理:真实世界研究驱动高钾血症诊疗变革
血液透析患者高血压管理的十个核心建议:基于ERA共识的临床实践指导
陈莉明教授:糖尿病慢性肾脏病的修正策略——从流行病学到多靶点治疗 | PUDF 2026
会议报道:聚焦临床痛点 共谋全程管理丨“肾英无界”中外IgA肾病学术前沿对话北京站成功举办
从AI到异种移植:ERA 2026最值得关注的五大未来技术
CIC 2026 | 任景怡教授:醛固酮介导心衰进展,nsMRA带来全新突破——从机制到临床的精准制导
ERA 2026三大临床试验专场:IgA肾病、CKD与罕见肾病治疗格局或将迎来新变化
何娅妮教授:糖尿病肾病治疗策略新进展——GDMT四大支柱筑牢心肾防线
Vadadustat(每周三次)对比不同基线剂量的甲氧基聚乙二醇促红素β治疗透析依赖型慢性肾病贫血患者的疗效与安全性分析
CCBPC 2026|涂晓文教授:血浆净化技术及其临床应用新进展
ERA 2026开幕在即!“Open your mind”背后,肾脏病学正在发生哪些改变?
ERA 2026|布地奈德肠溶胶囊23项全新研究闪耀登场,多维夯实对因、尽早、长期治疗临床证据体系
“生命之河”堵塞,肾脏告急!警惕“堵”出来的肾病——梗阻性肾病
中美双队列研究:不合并ASCVD的CKD患者,他汀治疗降低死亡风险26%~39%
会议报道:开放视野 探索前沿丨“肾英无界”中外IgA肾病学术前沿对话上海站圆满落幕
学术纵横丨常染色体显性多囊肾病(ADPKD)最新学术进展:风险评估、人群特征与创新药物探索
病例分享 | 血糖不高却频发酮症!这例糖尿病背后藏着双重隐秘病因,解密糖尿病胃轻瘫与肾糖阈减低的恶性循环
张宏教授:立足机制,解析B细胞靶向治疗IgA肾病的最新进展
肾移植术后膜性肾病研究:首个覆盖复发、未复发与新发类型的系统回顾与Meta分析核心结论与临床启示
压力与心血管疾病:成人期的隐形杀手
周晓霜教授:临床常规代谢指标与IgA肾病肾功能及病理损伤程度显著相关
非典型溶血尿毒综合征(aHUS)多学科诊疗专家共识要点,补体抑制剂为一线首选治疗
崔兆强教授:从“单纯降压”到“综合获益”——深度解析高血压治疗新趋势
以问破局 以共识远——《IgA肾病临床实践60问(2026版)》重磅发布,直击临床痛点,全面解锁IgA肾病对因治疗
开放思维,共探肾学前沿——第63届ERA大会即将启幕!26项中国研究入选最佳/优秀摘要
孙宁玲教授:破局“高容量”——从评估到干预,高血压管理如何走出困境?
CCBPC 2026|马坤岭教授:肠道菌群介导DKD肾损伤机制及转化应用新进展
北大医院近期科研新发现,速览!
【会议预热】三地联动,大咖云集:肾英无界・中外IgA肾病学术前沿对话即将启幕
聚焦重症肾脏病前沿 交流血液净化新进展——中华医学会肾脏病学分会第二十届重症肾脏病与血液净化大会在合肥开幕
两例罕见病例:FSGS顶端变异型合并IgA肾病及肾内B细胞浸润1例,产后IgA肾病与TMA的重叠1例
汪年松教授:2026年ADA糖尿病肾脏病指南核心解读
重新审视CKD尿蛋白检测——迈向白蛋白尿评估的全球共识
IgA肾病“双联治疗”真实世界结果:双重内皮素-血管紧张素受体拮抗剂联合靶向释放布地奈德,蛋白尿下降、eGFR趋稳
赵建荣教授:新时期慢性肾脏病的防控与设计
破译黏膜免疫“指挥棒”:浆细胞样树突状细胞通过TLR9-APRIL轴驱动IgA肾病的关键致病分子
狼疮足细胞病激素依赖、频繁复发:传统激素节约方案失败,奥妥珠单抗能否破局?
万建新教授:乳酸代谢异常与糖尿病肾病
揭秘心肾共病密码!miRNAs既可致心脏损伤,又能预警肾病进展
全球首例病例报道!甘草诱发罕见急性间质性肾炎一例
周晓霜教授:人工智能——从眼睛看肾脏
IgAN进入“机制优先时代”——重塑诊断、治疗与缓解的临床新格局
替那帕诺可降低透析高磷血症慢性肾脏病患者血磷水平且不影响其他血清电解质
北京大学第一医院杨莉教授团队原创AI体系开启肾病智能诊疗新时代
全球原发性肾小球肾炎流行病学、临床特征及预后解析
登顶《新英格兰医学杂志》!北大医院肾脏内科张宏/吕继成教授团队开创IgA肾病治疗“中国方案”
肾例明鉴|婴幼儿多饮多尿需警惕,不及时诊治可致死,不可忽视的婴幼儿肾小管罕见病
直击源头、AI赋能——锚定CKM早期,筑牢全生命周期防线
